Что такое хпз в желудке расшифровка
Актуальность проблемы
Дуодено-гастральный рефлюкс (ДГР) — одна из самых распространенных патологий верхних отделов желудочно-кишечного тракта, по данным разных источников, данное нарушение занимает 50-90% от всех заболеваний ЖКТ. Более того, за последние годы прослеживается рост количества заболевших. У пациентов с дуоденогастральным рефлюксом нередко также диагностируется хронический гастрит, в том числе рефлюкс-гастрит типа С, щелочной гастрит, язвенная болезнь желудка, функциональная диспепсия, грыжа пищеводного отверстия диафрагмы и ГЭРБ, пищевод Барретта, дуоденостаз, дисфункция сфинктера Одди, постхолецистэктомический синдром, рак желудка и целый ряд других заболеваний.
Следует знать, что ДГР способен привести к тяжелому гастриту и эзофагиту, стать причиной метаплазии желудка и пищевода, а также плоскоклеточного рака пищевода, который развивается на фоне метаплазии; это подтверждено клиническими исследованиями.
Таким образом, в результате патологического рефлюкса дуоденального содержимого в желудок течение многих органических и функциональных патологий ЖКТ может осложняться. Поэтому огромное значение должно уделяться своевременной диагностике, правильной клинической интерпретации и адекватной медикаментозной терапии.
При неэффективности консервативной коррекции показано хирургическое вмешательство, целью которого является укрепление пилорического жома, а также снижение количества забрасываемой желчи в желудок.
Есть данные о том, что на фоне ДГР желудка часто развиваются симптомы поражения системы дыхания, появляется синдром боли в грудной клетке, который не связан с коронарной патологией. Кроме того, у некоторых пациентов дуоденогастральный рефлюкс может вызвать рецидивирующий катаральный фарингит и пароксизмальный ларингоспазм. Однако у трети больных диагностируется «чистый» дуодено-гастральный рефлюкс, в этом случае можно говорить об изолированном диагнозе.
Причины дуодено-гастрального рефлюкса
Патогенетический механизм развития осложнений при ДГР
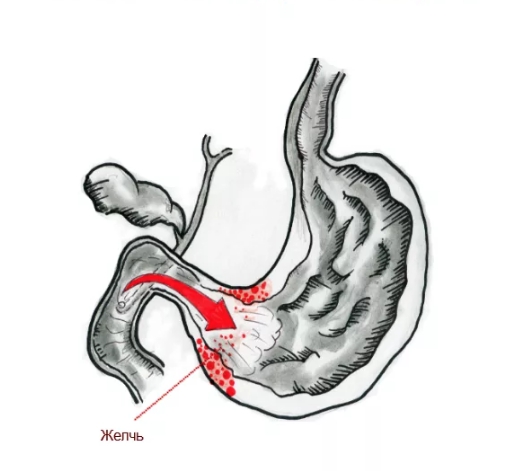
Желчь в составе рефлюксата при патологическом дуодено-гастральном рефлюксе ретроградно поступает из ДПК в органы, расположенные выше — желудок с пищеводом. Желчные кислоты, трипсин, лизолецитин — составляющие дуоденального содержимого — повреждают слизистую оболочку. Наиболее агрессивным действием при забросе дуоденального содержимого обладают желчные кислоты. Сегодня уже доказано, что при кислом рН среды лизолецитин и конъюгированные желчные кислоты (прежде всего тауриновые конъюгаты) сильнее повреждают слизистую желудка и пищевода, что определяет синергизм этих компонентов с соляной кислотой в развитии эзофагита и гастрита.
Неконъюгированные желчные кислоты и трипсин обладают более токсичным действием при слабощелочном и нейтральном рН, повреждающий эффект при дуодено-гастральном рефлюксе увеличивается при медикаментозном подавлении кислого рефлюкса. Их токсичность большей частью вызвана ионизированной формой, благодаря чему кислоты легко проникают через слизистую пищевода и желудка. Исходя из этого вполне объяснимо отсутствие адекватного ответа у 15-20% пациентов при монотерапии антисекреторными препаратами, если не будет учтен имеющийся дуодено-гастральный рефлюкс.
В результате действия на слизистую желудка желчных кислот, содержащихся в желчи, в течение длительного времени возникают изменения поверхностного эпителия желудка дистрофического и некробиотического характера, что ведет к развитию рефлюксгастрита — гастрита С. При имеющейся инфекции Нelicobacter pylori повреждающее действие рефлюксата на слизистую желудка возрастает. При наличии ДГР происходит заброс агрессивного содержимого в вышележащие отделы, что становится причиной нарушений в работе пищеварительной системы, воздействию подвергается мембранное и полостное пищеварение, возможность всасывания пищевых ингредиентов с микроэлементами и витаминами, изменяется водный баланс.
Признаком негативного воздействия ДГР являются признаки атрофии, метаплазии и дисплазии, это представляет опасность из-за риска развития рака желудка или пищевода. Кроме того, желчь в сочетании с панкреатическим соком из-за своей агрессивности разрушающе действует на слизистый барьер в желудке, при этом обратная диффузия водородных ионов усиливается. В результате этих процессов возникают эрозивные и язвенные поражения слизистой оболочки желудка.
Клинические проявления и диагностика дуодено-гастрального рефлюкса
Для ДГР характерно преобладание диспептических проявлений, пациента беспокоит отрыжка кислым содержимым или воздухом, изжога, тошнота, возможна рвота желчью, также появляется горечь во рту, которая не исчезает и даже усиливается при приеме ингибиторов протонной помпы.
Периодические боли в животе чаще схваткообразного характера, они могут возникать вследствие стресса или физической нагрузки.
Чаще дуоденогастральный рефлюкс сочетается с другими заболеваниями ЖКТ, в первую очередь с язвой желудка и ДПК, ГПОД, хроническим холециститом, панкреатитом и др. Соответственно, это отражается на симптоматике рефлюкса, существенно ее маскируя. В «чистом» виде ДГР появляется не так часто.
Дуодено-гастральный рефлюкс, в отличие от «классического» — желудочно-пищеводного рефлюкса кислой природы с изжогой, дисфагией и регургитацией — сопровождается не столь яркими клиническими проявлениями, но чаще проявляются признаки диспепсии. Кроме того, больных беспокоит боль в эпигастральной области, которая становится сильнее после приема пищи.
Диагностика основывается на результатах инструментальных методов обследования.
Лечение дуодено-гастрального рефлюкса
Консервативное лечение ДГР желудка отличается сложностью, целью терапии является нейтрализация агрессивного воздействия дуоденального содержимого на слизистую желудка и пищевода. Также в задачи лечения входит нормализация пропульсивной способности пищеварительного тракта. Назначения включают прокинетики, антациды, сорбенты, препараты урсодезоксихолевой кислоты (УДХК). При желчном рефлюксе терапия сочетается с базисным лечением основного заболевания. При этом огромное значение уделяется соблюдению диеты.
Медикаменты, используемые для устранения ДГР и восстановления моторики ЖКТ:
Следует учесть, что эритромицин в качестве прокинетика не рекомендован из-за побочных эффектов, цизаприд — не показан в клинической практике из-за вероятности нарушения сердечной проводимости, тегасерод — увеличивает вероятность инфаркта миокарда.
Фармакологическое действие домперидона (D2 антагонист) и метоклопрамида (5 НТ4 агонист и D2 антагонист) связано с блокадой рецепторов дофамина, антагонисты которых вызывают повышение тонуса нижнего сфинктера пищевода, увеличивают сократительную функцию желудка, а также препятствуют релаксации. Кроме того, благодаря антагонистам дофаминовых рецепторов улучшаются эвакуаторная способность желудка и антродуоденальная координация, что способствует устранению дуодено-гастрального рефлюкса.
Важно учесть, что клинические проявления рефлюкса с использованием медикаментозных препаратов уменьшаются, однако носят симптоматический характер. Добиться хороших результатов можно только при функциональных нарушениях, которые привели к ДГР. В остальных случаях консервативная терапия должна сочетаться с хирургическим лечением, способным устранить причину рефлюкса и укрепить пилорический клапан.
Хирургическое лечение дуодено-гастрального рефлюкса
При неэффективности консервативной терапии рекомендовано оперативное лечение, операция при этом проводится в нескольких направлениях:
При всех вышеперечисленных методиках используется лапароскопический доступ — через несколько (3-4) проколов на брюшной стенке.
Техника лапароскопической пилоропликации для уменьшения дуодено-гастрального рефлюкса
Прежде всего проводится ревизия пилородуодальной зоны, и оценивается выраженность спаечного процесса в зоне луковицы ДПК и привратника. Затем необходимо осмотреть связку Трейца, в случае необходимости она пересекается, тем самым улучшается прохождение пищи по двенадцатиперстной кишке. После ее мобилизации по Кохеру, что сделает ее более подвижной и снизит напряжение, накладываются швы в области привратника, что служит для профилактики несостоятельности.
Для пилоропликации поочередно накладываются серозно-мышечные швы симметрично к осе привратника, благодаря подобной методике передняя стенка луковицы ДПК сдвигается в проксимальном направлении, передняя полуокружность привратника погружается в просвет луковицы ДПК. Обычно четырех швов достаточно. Созданный антирефлюксный механизм способен препятствовать ДГР, не нарушая при этом эвакуации из желудка.
При необходимости проводится коррекция ГПОД или выполняется вмешательство на билиарном тракте. Следует помнить, что при лапароскопии возможно выполнение нескольких симультанных операций при наличии патологий в брюшной полости, малого таза или в забрюшинном пространстве, требующих оперативного лечения (киста почки, яичника, нефроптоз, миома и др.).
К настоящему времени нашими специалистами проведено более чем 600 оперативных вмешательств по поводу ГПОД и рефлюкс-эзофагита, а также связанных с хроническим нарушением дуоденальной проходимости. Накопленный опыт обобщен в 4-х монографиях: «Симультанные лапароскопические оперативные вмешательства в хирургии и гинекологии», «Грыжи пищеводного отверстия диафрагмы», «Ручной шов в эндоскопической хирургии» и «Технология дозированного лигирующего– электротермического воздействия на этапах лапароскопий». Кроме того, информация опубликована в многочисленных научных публикациях в разных профессиональных рецензируемых научных изданиях — российских и зарубежных.
После вмешательства на коже живота останется лишь несколько разрезов, длина которых не превышает 10 мм. Уже в день операции пациенты могут вставать, разрешается пить, на следующий день можно принимать теплую пищу в жидком виде. Клинику можно покинуть на 1-3 день — возможность выписки зависит от тяжести состояния. Но уже спустя 2-3 недели человек может вернуться к привычному образу жизни. Соблюдение строгой диеты необходимо в ближайшие два месяца, более мягкая разрешена через полгода после вмешательства. В дальнейшем человек, перенесший операцию, может обходится без медикаментов и не нуждается в строгом соблюдении диеты.
По желанию наши пациенты могут перед оперативным лечением пройти полное обследование, по результатам которого будет подобрана оптимальная тактика лечения и метод хирургического вмешательства.
На все ваши письма я отвечаю всегда только сам. Я помню, что вы доверяете мне самое ценное — свое здоровье, свою судьбу, свою семью, своих близких и делаю все возможное, чтобы оправдать ваше доверие. Каждый день я по нескольку часов отвечаю на ваши письма. Направляя мне письмо с вопросом, вы можете быть уверены, что я внимательно изучу вашу ситуацию, при необходимости запрошу дополнительные медицинские документы. Огромный клинический опыт и десятки тысяч успешных операций помогут мне разобраться в вашей проблеме даже на расстоянии.
Многим пациентам требуется не хирургическая помощь, а правильно подобранное консервативное лечение, в то время как другие нуждаются в срочной операции. И в том, и в другом случае я намечаю тактику действий и при необходимости порекомендую прохождение дополнительных обследований или неотложную госпитализацию. Важно помнить, что некоторым больным для успешной операции требуется предварительное лечение сопутствующих заболеваний и правильная предоперационная подготовка.
В письме обязательно (!) укажите возраст, основные жалобы, место проживания, контактный телефон и адрес электронной почты для прямой связи. Чтобы я мог детально ответить на все ваши вопросы, прошу высылать вместе с вашим запросом сканированные заключения УЗИ, КТ, МРТ и консультаций других специалистов. После изучения вашего случая, я направлю вам либо подробный ответ, либо письмо с дополнительными вопросами.
В любом случае я постараюсь вам помочь и оправдать ваше доверие, которое является для меня наивысшей ценностью.
Протокол диагностики и лечения пациентов с хроническим гастритом в РБ
Хронический гастрит – это хронический воспалительный процесс слизистой оболочки желудка, характеризующийся нарушением ее физиологической регенерации, уменьшением количества железистых клеток, при прогрессировании – атрофией железистого эпителия с развитием кишечной метаплазии, а в последующем – дисплазии. Хронический гастрит обычно вызывается микроорганизмом Нр.
Согласно МКБ-10 хронический гастрит классифицируется как:
Клиническими критериями хронического гастрита являются:
Диагностика при хронических гастритах
Обязательная диагностика:
Дополнительная диагностика:
Примечание:
Диагностические критерии хронического гастрита
При хроническом гастрите используют следующие критерии оценки степени тяжести:
| Выраженность атрофии (метаплазии)* | Тело желудка | ||||
|---|---|---|---|---|---|
| нет | легкая | умеренная | тяжелая | ||
| Антрум | нет | стадия 0 | стадия I | стадия II | стадия II |
| легкая | стадия I | стадия I | стадия II | стадия III | |
| умеренная | стадия II | стадия II | стадия III | стадия IV | |
| тяжелая | стадия III | стадия III | стадия IV | стадия IV | |
* Выраженность атрофии (метаплазии) определяется по проценту атрофированных и (или) метаплазированных желез с учетом всех биоптатов из данного отдела желудка: менее 30 % – легкая атрофия (метаплазия), 30–60 % – умеренная атрофия (метаплазия), более 60 % – тяжелая атрофия (метаплазия).
легкий атрофический гастрит – стадия I;
умеренный атрофический гастрит – стадия II;
тяжелый атрофический гастрит – стадии III, IV.
Наличие и степень тяжести дисплазии определяется по следующим критериям:
Хронический гастрит классифицируется в соответствии с Хьюстонско- Сиднейской системой следующим образом:
Формулировка диагноза хронического гастрита включает:
Цели лечения хронического гастрита
Показания для госпитализации пациента с хроническим гастритом
Лечение пациента с хроническим гастритом
Пациенты с хеликобактерным атрофическим гастритом умеренной или тяжелой степени, гастритом с метаплазией или дисплазией, аутоиммунным атрофическим гастритом и особыми формами гастрита относятся к группе диспансерного наблюдения Д(III) и подлежат диспансерному наблюдению у врача-терапевта участкового (врача общей практики) постоянно.
Объем и частота обследования при диспансерном наблюдении составляют:
Критериями эффективности лечения и диспансерного наблюдения пациента являются: исчезновение инфекции Нр, уменьшение воспалительных изменений слизистой оболочки желудка, отсутствие прогрессирования атрофии, метаплазии и дисплазии, отсутствие анемии при аутоиммунном атрофическом гастрите.
Хронические сосудистые болезни кишечника (K55.1)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Клинические понятия, включенные в данную подрубрику:
1. Хронический ишемический:
— колит;
— энтерит;
— энтероколит.
2. Ишемическое сужение кишечника.
3. Мезентериальный (ая):
— атеросклероз;
— сосудистая недостаточность.
Примечания
2. В последние годы было введено такое понятие, как «хроническая ишемическая болезнь органов пищеварения» (Звенигородская Л. А., 2001).
Хроническая ишемическая болезнь органов пищеварения – заболевание, возникающее при нарушении кровообращения по непарным висцеральным ветвям брюшной аорты (чревному стволу, верхней и нижней брыжеечной артериям), клинически проявляющееся болями в животе, обычно возникающими после приема пищи, нарушениями моторно-секреторной и абсорбционной функции кишечника и у части больных – прогрессирующим похуданием.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
II стадия – характеризуется выраженным нарушением функции кишечника и болью в животе после приема пищи.
III стадия – проявляется нарушением функции кишечника, постоянными болями в животе, прогрессирующим похудением.
Классификация развития хронической ишемической болезни органов пищеварения (ХИБОП)
I – стадия компенсации:
— IA – стадия бессимптомного течения; на УЗИ выявляются локальные изменения гемодинамики;
— IБ – стадия микросимптоматики; наблюдается возникновение ишемического синдрома вследствие функциональной перегрузки (развиваются локальные гемодинамические нарушения с тенденцией к снижению уровня функциональной и коллатеральной компенсации).
II – стадия субкомпенсации. Ишемия возникает вследствие функциональной нагрузки на органы пищеварения. С помощью УЗИ выявляют локальные гемодинамические сдвиги с различным поражением сосудов. При приеме пищи отсутствует гиперемическая реакция или она носит парадоксальный характер.
III – стадия декомпенсации. При УЗИ диагностируются различные поражения сосудов брюшной полости с развитием локальных и системных гемодинамических нарушений при выраженном снижении уровня функциональной и коллатеральной компенсации.
IV – стадия язвенно-некротических изменений органов пищеварения. При УЗИ диагностируются различные поражения сосудов брюшной полости с развитием локальных и системных гемодинамических нарушений и отсутствием функциональной и коллатеральной компенсации.
Клиническая классификация ишемического колита (считается наиболее приемлемой в настоящий момент):
— обратимая ишемическая колонопатия;
— преходящий язвенный ишемический колит;
— хронический язвенный ишемический колит;
— стриктура толстой кишки;
— гангрена толстой кишки.
Этиология и патогенез
Общее представление о хронической ишемии кишечника (Марстон А.)
Клиника ишемического энтероколита или колита возникает при поражении 2-3 мезентериальных артерий. Поскольку поражения тонкой кишки встречаются реже, в большей половине случаев речь идет о колите. Поражается, как правило, селезеночный угол толстой кишки и верхняя часть сигмовидной, что обусловлено анатомическими особенностями кровоснабжения толстой кишки.
Наиболее частые локализации:
— прямая и сигмовидная кишка (20%);
— нисходящая ободочная кишка (20%);
— селезеночный угол (11%);
— сочетание вышеперечисленных локализаций (14%);
— только прямая кишка (6%);
— восходящая ободочная кишка (8%).
Эпидемиология
Возраст: преимущественно пожилой
Соотношение полов(м/ж): 1
Примерно 1 из 2000 случаев госпитализации приходится на ишемический колит. Ишемический колит обнаруживается примерно в 1 из 100 эндоскопий. Мужчины и женщины страдают в равной степени. Более чем 90% случаев приходится на людей в возрасте старше 60 лет.
Частота возникновения абдоминального ишемического синдрома достаточно высока: выявляется в 75,5% случаев при аутопсии умерших от ишемической болезни сердца, вследствие атеросклероза церебральных артерий и/или сосудов нижних конечностей, также выявляют атеросклероз брюшной аорты и ее непарных висцеральных ветвей.
Частота стенозирующих поражений висцеральных ветвей брюшной аорты по данным аутопсии варьируется от 19,2% до 70%, по данным ангиографии – от 4,1% до 53,5%.
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
— боли могут купироваться нитроглицерином и/или папаверином.
2. Дисфункция кишечника
Отмечается в 88% случаев и проявляется нарушением секреторной и абсорбционной функций тонкого кишечника (метеоризм, неустойчивый стул, частый жидкий стул), а также нарушением эвакуаторной функции толстой кишки с упорными запорами.
4. Кровотечение из нижних отделов кишечника
Встречается в 62% случаев, но более характерно для острой ишемии. Эпизоды скрытой кровопотери могут длиться от суток до нескольких месяцев, что усугубляет анемию, возникающую вследствие недостаточности питания. Кровотечение в 85% случаев бывает незначительным и в 90% купируется самостоятельно.
При физикальном обследовании обнаруживаются:
— признаки недостаточности питания;
— боль, непропорциональная усилиям при пальпации;
— легкая, диффузная болезненность в той или иной области живота;
— отсутствие симптомов раздражения брюшины (защитных, охранительных симптомов);
— наличие систолического шума в эпигастральной области;
— признаки атеросклеротического поражения периферических сосудов (шумы над сонной артерией, изменения пульса, признаки ишемии сосудов ног, признаки церебральной ишемии, ишемической болезни сердца).
Диагностика
5. УЗИ (чувствительность 50-75%). На начальной стадии, ишемии кишечника может показать усиление перистальтики, которое затем нормализуется. Стенки кишки становятся утолщенными и узловатыми. Очаги кровоизлияния и отеки приводят к выявлению области (-ей) пониженной эхогенности в стенках кишечника.
6. УЗДГ (чувствительность 80%). Метод особенно эффективен при подозрении на стеноз нескольких сосудов.
УЗДГ не рекомендуется проводить при острой ишемии, ожирении, кишечной непроходимости, когда нарушение кровотока можно выявить только в проксимальных отделах.
Высокую прогностическую ценность имеют отклонения от нормы пиковой систолической скорости кровотока (S), которая ориентировочно составляет более 275 см/с для ВБА или 200 см/с для НБА (по некоторым данным > 300 см/с).
Нормальная скорость после приема пищи должна увеличиться примерно на 20% и более.
Ненормальный постпрандиальный ответ интерпретируется как увеличение пиковой систолической скорости менее чем на 20%.
Тяжелым считает стеноз артерий, составляющий более чем 60-70%, который выявляется при триплексном сканировании. При этом на допплерограмме ниже места поражения ламинарный поток исчезает и появляется турбулентный поток.
11. Алиментарные провокационные пробы основаны на тесной взаимосвязи болевого синдрома или дисфункции кишечника с приемом пищи.
Проба Миккельсена – пациенту выпивает литр молока в течение часа, появление болей при этом свидетельствует об ишемическом генезе заболевания.
Проба регулярного приема пищи обычной калорийности с исключением острых блюд (4-разовое питание).
Некоторые авторы предлагают проводить физические пробы – поднятие тяжестей, длительный физический труд в наклонном положении (стирка белья, мытье полов), быстрая ходьба, бег, подпрыгивание на месте, велоэргометрическую пробу для выявления экстравазальной компрессии чревного ствола.
Существуют также лекарственные пробы, провоцирующие проявления ИК (вазоспастические средства) и ликвидирующие его (вазодилататоры).
Диагноз брыжеечной ишемии часто является вызовом для клиницистов и рентгенологов. Пациенты с воспалительными заболеваниями кишечника и инфекционными колитами могут иметь сходные признаки и симптомы, в том числе спазмы, боли в животе, диарею, примесь крови в стуле. Утолщение стенки кишки является общей находкой для всех трех видов заболеваний, однако, структура сосудистого распределения кровотока иногда может сузить круг дифференцируемых заболеваний.
Что такое хпз в желудке расшифровка
Сочинский городской онкологический диспансер
Кубанский государственный медицинский университет, Краснодар
Кубанский государственный медицинский университет, Краснодар
Кубанский государственный медицинский университет, Краснодар
Диагностические критерии эндоскопической диагностики грыжи пищеводного отверстия диафрагмы
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2014;(1): 85-87
Вовненко М. И., Славинский А. А., Горбов Л. В., Сухинин А. А. Диагностические критерии эндоскопической диагностики грыжи пищеводного отверстия диафрагмы. Хирургия. Журнал им. Н.И. Пирогова. 2014;(1):85-87.
Vovnenko M I, Slavinskiĭ A A, Gorbov L V, Sukhinin A A. Diagnostic criteria for endoscopic diagnosis of hiatal hernia. Khirurgiya. 2014;(1):85-87.
Сочинский городской онкологический диспансер
Сочинский городской онкологический диспансер
Кубанский государственный медицинский университет, Краснодар
Кубанский государственный медицинский университет, Краснодар
Кубанский государственный медицинский университет, Краснодар
В последние годы внимание хирургов, гастроэнтерологов и врачей других специальностей приковано к гастроэзофагеальной рефлюксной болезни. Причина этого кроется в чрезвычайной распространенности этого заболевания, многообразии симптоматики и большой частоте осложнений [18, 19]. В последние годы отмечен рост заболеваемости гастроэзофагеальной рефлюксной болезнью (особенно в промышленно развитых странах [5]), морфологическим признаком которой является рефлюкс-эзофагит. Нужно отметить, что его причиной в 90% наблюдений служит грыжа пищеводного отверстия диафрагмы (ГПОД) [7, 17]. Это указывает на то, что при выполнении операций по поводу гастроэзофагеальной рефлюксной болезни необходимо учитывать наличие ГПОД у данной группы больных.
Бесспорно, что в последнее время в качестве метода исследования при заболеваниях желудочно-кишечного тракта наиболее часто применяется эндоскопия. Однако до сих пор нет единого мнения относительно эндоскопической диагностики ГПОД. Разные авторы опираются на различные прямые и косвенные признаки наличия грыжи.
В 20 проанализированных нами работах, так или иначе затрагивающих проблему эндоскопической диагностики ГПОД, удалось встретить 19 признаков, которые, по мнению авторов, могут явиться диагностическими критериями. Такое многообразие описательных характеристик свидетельствует об отсутствии попыток систематизации эндоскопической картины при данном заболевании. Приводим описанные в литературе признаки ГПОД и наши критические замечания, посвященные правомерности использования некоторых из них.
5. Гастроэзофагеальный пролапс [11, 13]. Считается, что он очень часто сопровождает ГПОД, но, по мнению авторов, больше свидетельствует о чрезмерной подвижности подслизистого слоя [13]. Значение его в диагностике ГПОД неизвестно [2].
6. Гастроэзофагеальный рефлюкс [11, 13] малоинформативен, поскольку зачастую возникает как рефлекторная реакция на столь нефизиологичную процедуру, какой является эзофагогастродуоденоскопия.
8. Грыжевой гастрит [11, 13] не стоит серьезно рассматривать в качестве диагностического признака, поскольку имеет место логическое несоответствие: грыжевым гастрит может называться только после диагностированной ГПОД. Кроме того, в современной эндоскопии вообще пытаются уйти от использования термина «гастрит», считая его не визуальным, а гистологическим [4].
11. Дилатация пищевода в области IX сегмента [14]. Согласно стандартной эндоскопической анатомической классификации, предложенной OMED, деление пищевода на сегменты не предусмотрено [4]. Это деление было предложено Brombart для рентгенологической анатомии пищевода [16]. В связи с этим выявление эндоскопистом расширения в IX сегменте пищевода (брюшной сегмент), с трудом обнаруживаемого и рентгенологическим методом, некорректно и не несет никакой информации о действительном наличии грыжи.
12. Уменьшение длины абдоминального отдела пищевода [14]. Этот признак не дает никакой информации, поскольку не отражает реальных анатомических взаимоотношений. На сегодняшний день общепринятая точка зрения состоит в том, что во время эзофагогастродуоденоскопии в норме зубчатая линия, ХС и кардиальное отверстие находятся на одном уровне, т.е. абдоминальный отдел пищевода не визуализируется [8].
13. Отсутствие или слабая визуализация, размытость зубчатой линии [14]. Этот признак также малоинформативен, поскольку если невозможно визуализировать зубчатую линию, являющуюся, согласно ОМЕD, анатомическим ориентиром и точкой отсчета для герниометрии [4], то невозможно судить, какой отдел пищеварительной трубки находится над диафрагмой, следовательно, невозможно достоверно судить о наличии ГПОД.
14. Уплощение складки кардиоэзофагеального перехода и сглаженность угла Гиса при инверсионном осмотре кардии [14]. Информативность этих признаков невысока, поскольку информативным считается увеличение угла Гиса более 90° [6, 20]. Оценить количественно эти параметры непрямым способом, анализируя глазом двухмерное изображение, полученное с помощью искажающей оптики эндоскопа, без измерительных приборов и специальных компьютерных программ в настоящее время невозможно.
16. Уходящие в кардиальное отверстие радиальные складки [2]. На наш взгляд, этот признак является всего лишь другой формулировкой предыдущего признака (наличия желудочных складок в области ХС).
17. При инверсионном осмотре видны желудочные складки, уходящие в грыжу [2]. По сути этот признак повторяет предыдущие два для ретроградного осмотра.
19. Втяжение грыжи вверх на вдохе при ретроградном осмотре [2]. Этот признак, на наш взгляд, также служит дополнительным признаком ГПОД.
Таким образом, критический анализ 19 существующих эндоскопических признаков грыжи пищеводного отверстия диафрагмы позволил нам выделить только 6 из них, которые в полном смысле можно считать информативными и не дублирующими друг друга. К этим признакам мы отнесли:
1) наличие желудочной слизистой над хиатальным сужением протяженностью не менее 2 см;
2) наличие желудочных складок в области хиатального сужения при прямом и ретроградном осмотре;
3) наличие грыжевой полости при прямом и ретроградном осмотре;
4) наличие пищеводных колец;
5) гастроэзофагеальный пролапс;
Предлагаемый метод диагностики базируется на принципах построения классификации дисплазий соединительной ткани, когда наличие заболевания подтверждается при регистрации определенного числа симптомов, одни из которых могут быть «большими», а другие «малыми» [9]. Показана успешность использования такого принципа диагностики и классификации патологических процессов при выявлении заболеваний с малоспецифичными симптомами, что в известной степени можно сказать и о грыже пищеводного отверстия диафрагмы.
Можно надеяться, что использование предлагаемого подхода позволит улучшить эндоскопическую диагностику грыжи пищеводного отверстия диафрагмы, в том числе у больных с диспепсическими явлениями и болью в грудной клетке (псевдокоронарные боли).