что такое бурая опухоль кости
Саркома костей
Вам поставили диагноз: саркома костей?
Наверняка Вы задаётесь вопросом: что же теперь делать?
Подобный диагноз всегда делит жизнь на «до» и «после». Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать».
Что такое саркома костей?
Филиалы и отделения, где лечат саркомы костей
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Хирургическое отделение онкологической ортопедии
Контакты: (495) 150 11 22
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отделение комбинированного лечения опухолей костей, мягких тканей и кожи
Заведующий отделения: Александр Александрович Курильчик
Контакты: 8 (484) 399 31 30
Введение
Опухоли костей – это обобщающее понятие, которое включает в себя все доброкачественные и злокачественные новообразования, поражающие скелет человека.
Статистика саркомы костей (эпидемиология)
Первичные злокачественные опухоли костей составляют 0,001% от всех впервые выявленных злокачественных новообразований. В России заболеваемость первичными злокачественными опухолями костей составляет 1,03 случая на 100 тыс. населения, что соответствует данным по заболеваемости в других странах.
Морфологическая классификация опухолей костей:
Стадии и симптоматика саркомы костей
Клиническая классификация TNM
Боль – самый ранний признак. Для начала болезни характерна тупая, ноющая боль без четкой локализации в кости. Дальнейшее развитие заболевания приводит к появлению невыносимо сильной боли, пик приходится на ночное время, не купируется обычными анальгетиками. У более чем половины пациентов на месте роста опухоли пальпируется припухлость по плотности мягче костной ткани. Пораженная конечность отекшая, может быть покраснение кожи.
Причины возникновения саркомы костей и факторы риска
К факторам риска развития сарком костей можно отнести предшествующую лучевую терапию, состояние иммунодефицита, болезнь Педжета, болезнь Олье, доброкачественные опухолевые поражения кости так же могут приводить к злокачественной трансформации. Однако, у большинства пациентов специфических этиологических факторов не выявляется.
Диагностика саркомы костей
·Компьютерная томография легких. Наиболее часто саркомы костей метастазируют в легкие, а разряжающая возможность флюорографии и рентгеновского исследования невелика, поэтому пациентам с саркомами костей необходимо выполнение компьютерной томографии органов грудной клетки.
·Компьютерная томография или магнитно-резонансная томография первичного очага опухоли. Эти исследования позволяют адекватно оценить распространенность опухолевого процесса, прилежание опухоли к магистральным сосудисто-нервным структурам, степень вовлечения прилежащих мягких тканей.
·Ультразвуковое исследование брюшной полости, печени, прилежащих зон регионарного лимфооттока. Саркомы костей редко метастазируют в печень и регионарные лимфотические коллекторы (3-5%) и наличие метастазов в них является неблагоприятным прогностическим фактором, однако проводить исследование этих областей так же необходимо.
·Сцинтиграфия костей. Второй по частоте развития метастазов сарком костей точкой являются кости, поэтому проведение сцинтиграфии для таких пациентов обязательно.
·Так же необходимо диагностировать и вовремя назначить коррегириующую терапию сопутствующих хронических либо впервые выявленных заболеваний – сахарный диабет, различные кардиальные патологии, нарушения дыхания, нарушения работы почек и прочие.
Лечение саркомы костей
В первую очередь следует рассматривать возможность выполнения органосохранных операций. Главным условием операбельности пациентов является радикальность и абластичность удаления опухоли, что гарантирует отсутствие местного рецидива.
Сотрудники ФГБУ «НМИЦ радиологии» Минздрава России владеют всеми современными методиками органосохранной хирургии опорно – двигательного аппарата:
· Эндопротезирование онкологическим эндопротезом плечевого сустава.
· Эндопротезирование онкологическим эндопротезом тазобедренного сустава.
· Эндопротезирование онкологическим эндопротезом коленного сустава.
· Тотальное эндопротезирование бедренной кости.
· Модульное эндопротезирование вертлужной впадины после удаления опухолей костей таза.
· Эндопротезирование тел позвонков на всех уровнях позвоночного столба.
· Эндопротезирование онкологическим эндопротезом лучезапястного сустава.
· Эндопротезирование онкологическим эндопротезом локтового сустава.
· Реконструкция удаленных фрагментов костей при помощи ауто/аллопластики.
· Резекция костей плечевого пояса (лопатка, ключица).
· Резекции ребер и грудной стенки.
· Использование собственной кости пациента для замещения дефекта после операции.
· Онкологическое эндопротезирование, металлолстеосинтез.
· Расширенные операции при массивных опухолях плечевого пояса (межлопаточно-грудная ампутация).
При невозможности выполнения органосохранных операций необходимо выполнение калечащих операций в радикальном объеме. Ампутация или экзартикуляция конечности выполняются в следующих случаях:
Так же в клинической практике лечения злокачественных поражений костей применятся лучевая и химиотерапия.
Осложнения противоопухолевого лечения саркомы костей и их коррекция
Особенности реабилитации после лечения саркомы костей
Реабилитация пациентов, которым было проведено хирургическое лечение по поводу опухолевого поражения костей в нашем отделении – является одной из приоритетных задач для врачей нашего центра. Этот процесс включает себя большое количество специалистов: онкологов, врачей ЛФК, неврологов и даже психологов. Хорошее психоэмоциональное состояние пациента, является одним из главных факторов для более быстрой реабилитации больного. Для каждого пациента подбирается индивидуальный план реабилитационных мероприятий. Как правило на 2-3 сутки после операции пациент встает на ноги и начинает получать минимальные нагрузки. C каждым днем нагрузка увеличивается, под чутким контролем врачей. В большинстве случаев пациент, получивший у нас лечение, покидает нас на своих ногах и с огромной мотивацией на быстрое выздоровление.
Прогноз заболевания саркомы костей
Важно понимать, что течение болезни индивидуально и не всегда возможно предугадать его течение. Оно может благоприятным или неблагоприятным, но бывают исключения из правил, как их плохих, так и из хороших. Неблагоприятными факторами, которые могут влиять на выживаемость являются: высокая степень злокачественности, размеры первичной опухоли, локализация опухоли в костях таза и позвоночнике, слабая реакция опухоли не проводимую химиотерапию, выраженная сопутствующая патология. При проведении правильного лечения общая пятилетняя выживаемость больных с высокозлокачественными саркомами костей составляет до 75%. При опухолях низкой степени злокачественности она выше и может достигать 90%.
Филиалы и отделения, в которых лечат саркомы костей
ФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, лекарственного и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.
Контакты: (495) 150 11 22
Заведующий отделения: Александр Александрович Курильчик
Остеобластокластома, гигантоклеточная опухоль
Термин «остеобластокластома» был предложен А. В. Русаковым в 1959 году. В Международной гистологической классификации первичных опухолей и опухолеподобных заболеваний костей принят термин «гигантоклеточная опухоль».
До настоящего времени существуют различные наименования гигантоклеточной опухоли: гигантоклеточная опухоль типа эпулида, бурая опухоль, гигантома, гигантоклеточная саркома, остеокластома, местная фиброзная остеодистрофия.
В этиологии данной опухоли, по мнению ряда авторов, существенную роль играет травма кости. Гигантоклеточные опухоли относят к истинным опухолям — бластомам. В настоящее время и хирургами, и патологоанатомами данные опухоли признаны доброкачественными, хотя и склонными к рецидивированию. Это привело к замене терминов «гигантоклеточная саркома», «гигантоклеточная опухоль» термином «гигантома». Гигантоклеточная опухоль может принимать саркоматозное строение.
Остеобластокластома является доброкачественной остеогенной опухолью. Возникает в челюстных костях. Опухоль развивается преимущественно у лиц молодого возраста, чаще у женщин 11–30 лет. По данным Ю. И. Бернадского, остеобластокластомы составляют 20,7 % от числа опухолей костей лица.
Остеобластокластома может располагаться по периферии кости и в толще костной ткани. При локализации на альвеолярном отростке челюсти её рассматривают как гигантоклеточный эпулид. В нижней челюсти опухоль чаще всего выявляется в области премоляров и моляров, в верхней челюсти — в области премоляров. К редким локализациям относится поражение скуловой кости.
Остеобластокластома— клиника образования
Незаметно для больного появляется равномерное утолщение на одном из участков нижней или верхней челюсти, часто безболезненное. Рост опухоли продолжается в течение 3–10 лет, но иногда бывает и более интенсивным.
При пальпации образования его плотные участки чередуются с размягчёнными. Форма его выпуклая, куполообразная, иногда происходит истончение стенок челюсти, что проявляется в виде симптома Дюпюитрена (крепитация). Зубы в зоне образования подвижны, электровозбудимость их понижена, в очаге поражения отмечается резорбция корней зубов на 1/3 длины. Слизистая над опухолью либо не изменена, либо слегка анемична, бывает расширена венозная сеть слизистой оболочки в области опухоли.
При возникновении одонтогенного воспалительного процесса превалируют признаки острого воспаления. Диагноз может быть установлен при комплексном клинико-рентгенологическом исследовании.
На основании клинико-рентгенологических данных и морфологической картины различают три основные формы остеобластокластом: ячеистую, кистозную, литическую.
Ячеистая форма чаще наблюдается в зрелом и пожилом возрасте, характеризуется очень медленным развитием. При обследовании больного определяется плотная припухлость с бугристой поверхностью, отграничить опухоль от здоровых участков кости клинически не удаётся; челюсть часто имеет веретенообразную форму. Зубы, расположенные в зоне опухоли, редко меняют своё положение. Электровозбудимость пульпы интактных зубов не нарушена. Слизистая оболочка, покрывающая опухоль, несколько анемична.
При кистозной форме опухоли первыми симптомами заболевания в большинстве случаев являются жалобы на зубную боль. При пальпаторном обследовании отдельные участки опухоли податливы при надавливании (симптом «пергаментного хруста»); истончённая кость над опухолью имеет гладковыпуклую, куполообразную форму.
Литическая форма встречается редко, чаще в детском и юношеском возрасте, и составляет 10 % от всех остеобластокластом челюстей. Развитие данной формы остеобластокластомы происходит довольно быстро. В ряде случаев первый признак развивающейся опухоли — боль. При истончении кортикального слоя, наряду с самостоятельными болями в покое, появляется боль при пальпации. Венозная сеть сосудов слизистой оболочки, покрывающей опухоль, расширена. Зубы нередко смещаются и
становятся подвижными, электоровозбудимость пульпы понижается. В области поражения могут происходить патологические переломы челюсти; при локализации на верхней челюсти возможно прорастание в верхнечелюстную пазуху, носовую полость и другие кости лицевого скелета. При пункции образования обнаруживается жидкость бурого или желтоватого цвета, что связано с распадом эритроцитов и образованием гемосидерина, иногда с кровью. Пунктат не включает в себя кристаллов холестерина, что обычно встречается при кисте.
Остеобластокластома — рентгенологическая картина
Рентгенологически при ячеистой форме опухоли на месте очага поражения отмечается тень от множества мелких и более крупных полостей или ячеистых образований, отделённых друг от друга костными перегородками различной толщины. Реакции со стороны надкостницы не наблюдается. Картина во многом сходна с рентгенологической картиной амелобластомы.
Кистозная форма на рентгенограмме напоминает одонтогенную кисту челюсти и амелобластому. Отличие кистозной формы амелобластомы в том, что её граница с костью нередко имеет мелкофестончатые очертания в виде чрезвычайно маленьких бухточек.
При литической форме остеобластокластомы опухоль даёт бесструктурный очаг просветления.
Остеобластокластома — макроскопическая картина
Макроскопически опухоль имеет пёстрое строение: участки бурого цвета перемежаются с участками красно-серого цвета и желтоватыми полями некроза. Зона фиброзной ткани имеет белесоватую окраску. В толще опухоли различают одиночные или множественные мелкие полости, содержащие кровянистую бурую жидкость. Встречаются очаги оссификации. В периферических отделах опухоли может наблюдаться костеобразование в виде уплотнений. Иногда опухоль солидная, без полостей.
Остеобластокластома — микроскопическая картина
Микроскопически в остеобластокластоме различают большое количество мелких, слегка вытянутых клеток с округлым ядром (типа остеобластов), среди которых определяются массивные скопления гигантских многоядерных клеток (остеокластов). В одноядерных клетках отмечаются митозы, в многоядерных они отсутствуют. Форменные элементы опухоли
представлены также фибробластами и ксантомными клетками. Участки кровоизлияний подвергаются макрофагальной реакции соответствующими фагоцитарными клетками.
В некоторых участках опухоли обнаруживаются островки остеоидной ткани. Опухоль насыщена распавшимися эритроцитами и имбибирована кровяным пигментом — гемосидерином, который придаёт ей бурую окраску. Наличие последнего и множественных кровоизлияний, часто в виде кровяных кист, обусловлено особенностью кровотока в опухоли.
Кровь в остеобластокластоме циркулирует вне сосудистого русла по межтканевым щелям. Отсутствие эндотелия позволяет ей проникать в ткань опухоли и скапливаться там. При этом форменные элементы крови разрушаются, образуя скопление гемосидерина. Иногда в опухоли может обнаруживаться обилие фиброзной ткани.
Остеобластокластома — дифференциальная диагностика
Остеобластокластому (кистозная и ячеистая формы) необходимо дифференцировать с амелобластомой и радикулярной кистой, литическую форму — с остеогенной саркомой (в
отличие от остеолитической саркомы в остеобластокластоме отмечаются истончение и вздутие коркового слоя челюсти) и фиброзной остеодисплазией (характерен медленный рост и сохранение на рентгенограмме непрерывности коркового слоя челюсти), фибромиксомой, центральными фибромами челюстей.
Клинико-рентгенологическое обследование без гистологического сопоставления бывает недостаточным для установления точного диагноза остеобластокластомы. Частота расхождения клинического диагноза с патогистологическим составляет 30%; наиболее частые расхождения возникают при дифференцировании остеобластокластомы с амелобластомой — 16 %
Остеобластокластома — лечение
Лечение остеобластокластом челюстей — хирургическое. При кистозной и ячеистой формах обычно достаточно тщательного выскабливания очага поражения. Если опухоль занимает значительные участки челюстной кости, возможно проведение резекции нижней челюсти, при необходимости — с одномоментной костной пластикой. При литической форме чаще используется частичная резекция челюсти без нарушения непрерывности нижнечелюстной кости (континуитальная резекция) или резекция фрагмента челюсти с одномоментной костной пластикой. Лучевая терапия не даёт достаточного лечебного эффекта. Однако данный метод лечения назначается больным, которым любое оперативное вмешательство
противопоказано по общесоматическому статусу. Обычно используют короткофокусную рентгенотерапию, дистанционную гамма-терапию, тормозное и электронное излучение высоких энергий. Средняя доза облучения колеблется в пределах 30–50 Гр/кг. Прогноз лечения благоприятный, однако возможность малигнизации и метастазирования опухоли при доброкачественном характере новообразования не исключается. К рецидивам опухолевого процесса обычно приводит неправильная лечебная тактика.
Бурые опухоли – проявление неконтролируемого гиперпаратиреоза
Костная ткань в течение жизни претерпевает малозаметную нашему глазу, но крайне важную в биологическом отношении перестройку структуры – ремоделирование. Ремоделирование сводится к локальному удалению старой костной ткани остеокластами и замещении этого участка новой тканью – остеобластами. Этот процесс позволяет костям адаптироваться к механическим нагрузкам, которым скелет подвергается ежедневно, и восстанавливать микроповреждения в костной ткани. Именно так обеспечивается прочность костей. Разрушение старой костной ткани остеокластами и образование новой костной ткани остеобластами –сбалансированный процесс, и лишь к старости это равновесие постепенно смещается в сторону разрушения старой костной ткани. Однако существует ряд нефизиологических причин, способных резко и преждевременно сместить равновесие в сторону разрушения костной ткани, и одним из наиболее значимых патологических состояний в этом отношении является гиперпаратиреоз.
Что такое гиперпаратиреоз?
Гиперпаратиреоз – состояние чрезмерно высокой и неконтролируемой продукции (высвобождения в кровь) паратиреоидного гормона (ПТГ) паращитовидными железами. ПТГ играет важную роль в регуляции концентрации кальция – важнейшего макроэлемента, необходимого для адекватного функционирования скелетной, нервной ткани, для обеспечения прочности костей скелета и целого ряда физиологических процессов в организме. Именно ПТГ способствует повышению концентрации кальция в крови. Одним из механизмов, по которому это происходит, является усиление интенсивности процессов резорбции, разрушения костной ткани.
Значение ПТГ в контексте ремоделирования костной ткани сводится к активации остеокластов и тем самым к активации процессов разрушения костной ткани. Биологический смысл такого влияния заключается в увеличении концентрации кальция в крови, когда его становится мало. Костная ткань является единственным резервуаром кальция в организме, и достать кальций из костей можно только, разрушив костную ткань. При гиперпаратиреозе такая активация является неконтролируемой, биологически нецелесообразной, и сам процесс резорбции приобретает деструктивный характер, приводящий к уменьшению плотности и прочности костей. Однако еще одним важным следствием гиперпаратиреоза и чрезмерно высокой активацией остеокластов является образование в ряде случаев так называемых бурых опухолей (остеокластом).
Несмотря на свое название – «бурые опухоли», данный патологический процесс по своей природе не является опухолевым. Бурыми опухолями или остеокластомами называют очаговые реактивные скопления активно делящихся остеокластов и разрастание соединительной ткани в костях как ответ на длительный и неконтролируемый гиперпаратиреоз.
Как это происходит?
В результате длительного и неконтролируемого воздействия ПТГ на остеокласты, происходит гиперплазия (увеличение количества клеток) и активация последних. Из-за неконтролируемой активации остеокластов происходит такое же неконтролируемое разрушение костной ткани и разрастание соединительной ткани. Зачастую данный процесс приобретает кистозно-фиброзный характер: костная ткань замещается замкнутыми полостями, среди которых прослеживается скопление клеток (остеокластов, фибробластов) и волокон соединительной ткани.
Почему их называют «бурые опухоли»?
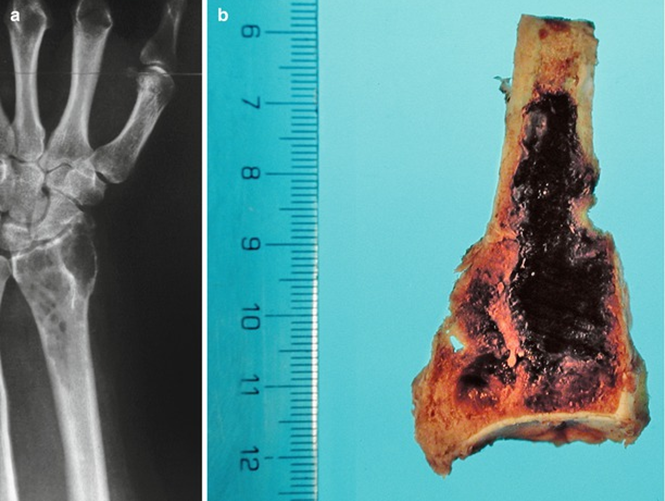
В очагах остеокластом зачастую происходит кровотечение и кровоизлияние в область разрастания остеокластов. Кровоизлияние приводит к накоплению гемосидерина, образующегося при распаде гемоглобина и придающего данным очагам бурый цвет (Рис. 1):
Наиболее часто возникновение бурых опухолей описывают в контексте гиперпаратиреоза. Первичный гиперпаратиреоз, связанный с неконтролируемой продукцией ПТГ клетками опухолей паращитовидных желёз, является причиной образования бурых опухолей в 3–20 % случаев. При первичном гиперпаратиреозе бурые опухоли наиболее часто поражают пациентов с единичными или множественными аденомами паращитовидных желёз и крайне редко (до 0,5 % случаев) это происходит при раке паращитовидных желёз.
Между тем вторичный гиперпаратиреоз – адаптивное разрастание тканей паращитовидных желёз в ответ на длительную гипокальциемию (наиболее часто – при хронической болезни почек (ХБП) является не менее важной причиной возникновения бурых опухолей, что происходит у данной группы пациентов в 1,5 % случаев.
Проблема вторичного гиперпаратиреоза и бурых опухолей наиболее актуальна для пациентов с хронической почечной недостаточностью, обусловленной ХБП. Многими авторами фиброзно-кистозные изменения костей, возникающих при ХБП, описывается как форма почечной остеодистрофии. Но почему?
В регуляции концентрации кальция крови большое значение имеет не только ремоделирование костей. Кальций поступает в кровь в результате его реабсорбции (повторного всасывания в кровь) в почечных канальцах, но и на этом функция почек здесь не ограничивается. Почка является местом биохимической активации активной формы витамина D (кальциферола), и при ХБП активация витамина D, способствующего возвращению кальция в кости, также нарушается. Другим следствием является уменьшение усвоения кальция и его всасывания в кровь из желудочно-кишечного тракта. Все это приводит к активации паращитовидных желёз, высвобождению высоких уровней ПТГ и развитию вторичного гиперпаратиреоза.
Проявления и симптомы
Бурые опухоли могут поражать различные отделы скелета. Наиболее часто происходит поражение рёбер, ключиц, тазовых костей, трубчатых костей нижних конечностей несколько реже описываются поражения костей лицевого скелета и костей верхних конечностей, а также костей позвоночника.
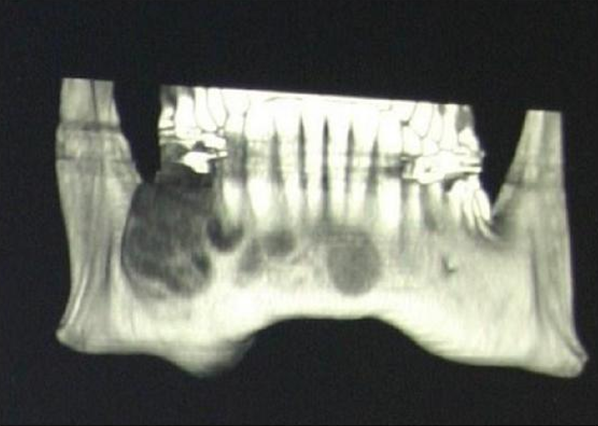
Рис.2: Бурые опухоли нижней челюсти, определяющиеся на рентгенограмме как очаги пониженной плотности в толще кости
Клиническое течение бурых опухолей может быть бессимптомным, однако по мере прогрессирования процесса они могут обнаруживаться как болезненные, уплотнённые массы в области поражённого участка скелета. Помимо этого, бурые опухоли могут вызывать ряд осложнений и неотложных состояний в виде патологических переломов (нарушение целостности костей без чрезмерного травмирующего фактора), компрессию спинного мозга, а при поражении лица могут вызывать его деформацию, неврологические нарушения из-за сдавления нервных волокон.
При лабораторном обследовании главными изменениями являются проявления гиперпаратиреоза: рост содержания ПТГ и кальция крови (при первичном гиперпаратиреозе), нормо- или гипокальциемия в сочетании с гиперфосфатемией при вторичном гиперпаратиреозе, а также рост содержания щелочной фосфатазы – важного лабораторного маркера, отражающего активность процессов костной резорбции.
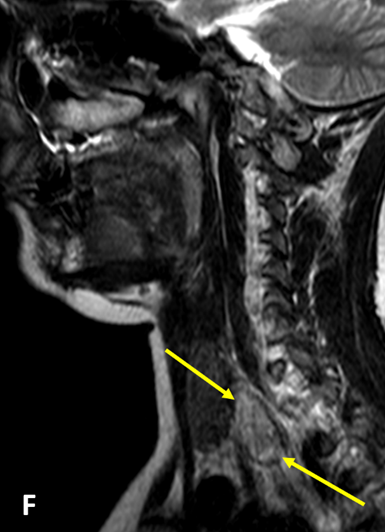
Помимо прочего, лабораторные и клинические признаки гиперпаратиреоза диктуют необходимость оценки состояния паращитовидных желёз. Для этих целей применяется УЗИ мягких тканей и МРТ мягких тканей шеи. При выполнении данных исследований обнаруживаются признаки новообразований паращитовидных желёз – аденомы или карциномы паращитовидных желёз.
Рис. 3: Прослеживается гиперденсное увеличение размеров паращитовидной железы, свидетельствующее об опухолевом процессе в данной железе
Диагностика
Диагностика бурых опухолей, помимо выявления гиперпаратиреоза, заключается главным образом в применении различных методов визуализации поражённых участков скелета.
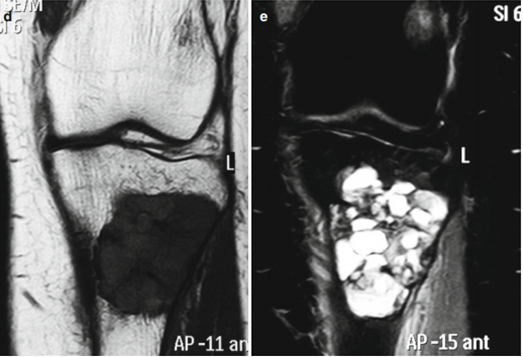
Рис.4: Компьютерная томография: визуализируются образования большеберцовой кости в виде гиподенсных масс, в которых прослеживается кистозная структура
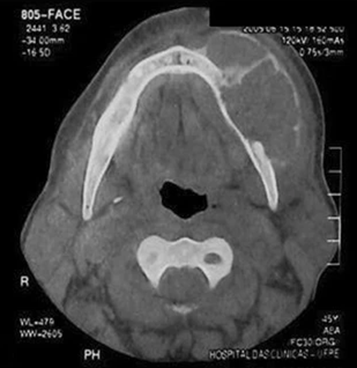
Рис. 5: КТ – признаки бурой опухоли верхней челюсти: гиподенсный литический очаг с расслоением надкостницы
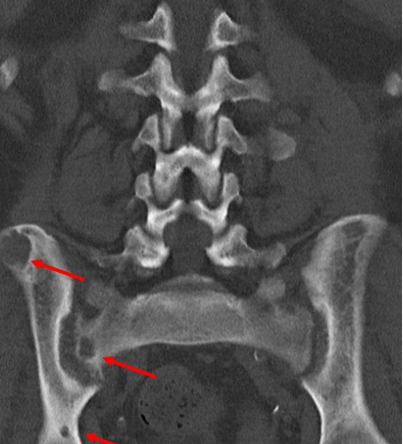
Рис. 6: Магнитно-резонансная томография (МРТ) – множественные гиподенсные очаги костей таза, имеющие кистозный характер
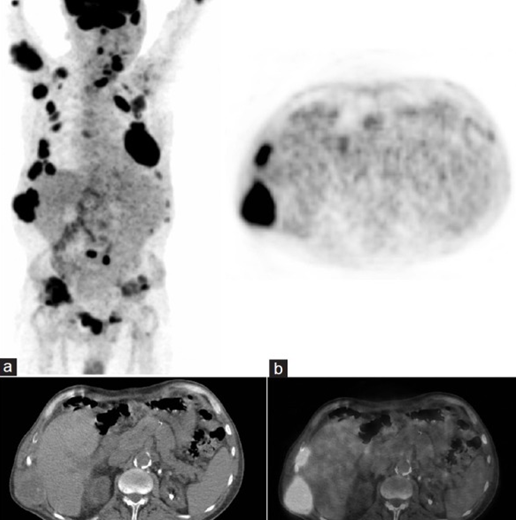
Рис. 7: ПЭТ/КТ и визуализация бурых опухолей при гиперпаратиреозе. Ограниченные данные свидетельствуют о высокой чувствительности, но низкой специфичности ПЭТ/КТ в диагностике бурых опухолей
Инструментальные проявления бурых опухолей имеют крайне неспецифический характер. Активное свечение на ПЭТ/КТ делает их похожими на метастатические опухолевые очаги, а литический характер поражения костей, прослеживаемый во многих случаях бурых опухолей, делает их похожими на миеломную болезнь. Это подтверждает целесообразность морфологической верификации бурой опухоли.
Лечение
В случае первичного гиперпаратиреоза наиболее целесообразным является хирургическое удаление новообразования паращитовидной железы (аденомы, рака паращитовидных желёз). Об этом говорится в большинстве литературных описаний клинических случаев пациентов с бурыми опухолями различной локализации. В серии из 22 случаев было продемонстрировано успешное (частичное или полное) разрешение бурых опухолей в виде уменьшения или исчезновения очагов остеокластомы после хирургического лечения первичного гиперпаратиреоза (частичная паратиреоидэктомия).
Существуют единичные сообщения об эффективности кальцитонина и бифосфонатов при бурой опухоли, сопряжённой с первичным гиперпаратиреозом, которые не позволяют уверенно судить о значении данных препаратов в ведении таких пациентов.
В случае вторичного гиперпаратиреоза, наиболее часто ассоциированного с ХБП, приходится ограничиваться консервативными терапевтическими мероприятиями, иначе говоря, медикаментозной коррекцией имеющихся метаболических нарушений. Эксперты UptoDate рекомендуют применение холекальциферола при вторичном гиперпаратиреозе у пациентов с ХБП. В конце прошлого века на выборке в 176 пациентов было продемонстрировано, что применение препаратов витамина D способствует предотвращению выраженных костно — дистрофических изменений у пациентов с лёгкой и средней степенью выраженности хронической почечной недостаточности (такое понятие, как ХБП тогда ещё не выделяли), однако данные о применение препаратов витамина D при бурых опухолях ограничены, и не совсем понятно, можно ли экстраполировать данные имеющегося исследования на группу пациентов с развившимися остеокластомами. Применение данной группы препаратов ограничено и в силу риска развития гиперкальциемии.
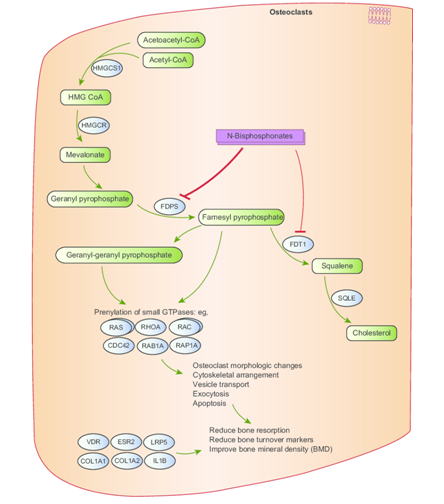
Недостаточно данных и в отношении роли бифосфонатов при остеокластомах. Существующие теоретические данные о механизме действия бифосфонатов позволяют лишь предполагать наличие потенциальной пользы этих препаратов при данном патологическом состоянии. Известно, что бифосфонаты подавляют фарнезилдифосфонат синтазу в пути биосинтеза мевалоната, тем самым нарушая важный в отношении развития и выживания остеокластов и резорбции костной ткани биохимический каскад, и наибольшую активность проявляет золедроновая кислота.
Рис. 8: Иллюстрация механизма действия бифосфонатов. Продемонстрировано угнетение фарнезилфосфат-синтазы, приводящее к накоплению фарнезилпирофосфата в остокластов с последующей реализацией апоптоза и уменьшение выраженности костной резорбции
Применение золедроновой кислоты у пациентов с бурыми опухолями, возникшими на фоне вторичного гиперпаратиреоза, выглядит патогенетически оправданным. Однако в силу отсутствия клинических исследований, оценивающих применение данного препарата при бурых опухолях, вопрос о назначении золедроновой кислоты должен решаться индивидуально, и, по-видимому, путём проведения врачебной комиссии и назначении данного препарата офф-лейбл, то есть не по инструкции.
Между тем в РФ для лечения пациентов со вторичным гиперпаратиреозом, возникшим на основе ХБП, зарегистрирован кальций – миметический препарат цинакальцет. Цинакальцет является агонистом кальций-чувствительных рецепторов на поверхности клеток паращитовидной железы. Цинакальцет имитирует воздействие кальция на эти рецепторы, тем самым восстанавливая нарушенную отрицательную обратную связь, при которой повышение концентрации кальция в крови приводит к снижению активности клеток паращитовидных желёз и снижению выработки ПТГ. Цинакальцет демонстрирует сопоставимую эффективность в сравнении с препаратами витамина D, а по данным крупного метаанализа цинакальцет способствует снижению необходимости в проведении паратиреоидэктомии у пациентов со вторичным гиперпаратиреозом. Это актуально, потому что именно паратиреоидэктомия зачастую может стать единственным методом лечения у пациентов со вторичным гиперпаратиреозом, когда медикаментозная терапия не позволяет достичь коррекции данного патологического состояния.
Наблюдение и прогноз
Прогноз таких пациентов обусловливается успешностью коррекции гиперпаратиреоза. На сегодняшний день отсутствуют достоверные данные об отдалённых исходах у таких пациентов, однако есть ограниченные данные, свидетельствующие о высокой вероятности регресса бурых опухолей после хирургического лечения первичного гиперпаратиреоза. В отношении пациентов со вторичным гиперпаратиреозом на фоне ХБП прогноз также определяется течением основного заболевания, и, по-видимому, возможность лечения бурых опухолей ограничивается медикаментозным лечением или трансплантацией почки.
После гемипаратиреоидэктомии, а также при проведении медикаментозного лечения (цинкальцетом, золедроновой кислотой, препаратами витамина D) необходима динамическая оценка лабораторных показателей, отражающих метаболизм костной ткани, в частности, ПТГ, кальций крови (общий и ионизированный), щелочная фосфатаза, фосфаты. Допустимым методом оценки лечебного эффекта гемипаратиреоидэктомии является ПЭТ/КТ при доказанном отсутствии первичной опухоли, которая может быть источником костных метастазов и при условии проведённого ПЭТ/КТ – исследования перед началом лечения.
Примечательно, что встречаемость бурых опухолей за последние десятки лет снижается в силу улучшения методов диагностики и своевременного выявления гиперпаратиреоза у пациентов. Чрезвычайно редкая встречаемость бурых опухолей в общей популяции затрудняет создание чётких гайдлайнов ведения таких пациентов, и в каждом конкретном случае мы являемся субъектами своеобразного эксперимента с ограниченным количеством известных данных и лечебных возможностей. Тем не менее в таких условиях очевидна необходимость профилактики и своевременной коррекции гиперпаратиреоза как единственно возможного метода борьбы с бурыми опухолями.
Список литературы:
Авторская публикация:
Г.А. Чиж
ординатор НМИЦ онкологии им. Н.Н. Петрова