что такое атопический дерматит у новорожденных
Атопический дерматит у детей
Что такое атопический дерматит
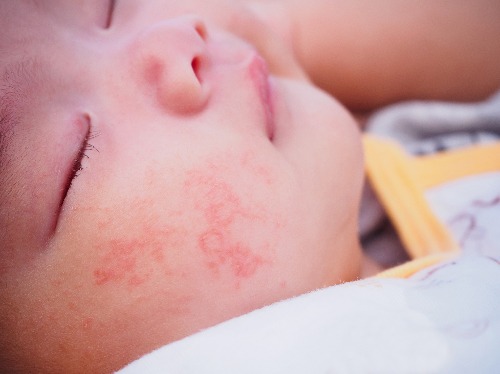
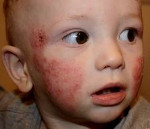
Атопический дерматит — это хроническое заболевание кожи, которое характеризуется рецидивирующим течением. Малышей с атопическим дерматитом беспокоят зуд и сухость кожных покровов. Очаги воспаления могут располагаться по всему телу, но особенно “любят” детские щечки и складочки, а также зону под подгузником.
Статистика отмечает, что атопический дерматит встречается у каждого пятого малыша [1]. Чем он опасен? Отсутствие лечения может привести к развитию тяжелых форм атопического дерматита, распространению воспаления и атопическому маршу. При этом состоянии болезнь начинает “маршировать” по организму ребенка, провоцируя появление или обостряя сопутствующие заболевания. В 20-43% случаев возможно развитие бронхиальной астмы, вдвое чаще — аллергического ринита или экземы [2].
Кроме того, нарушение гидролипидного барьера, возникающее при атопическом дерматите у детей, может стать причиной присоединения вторичной инфекции.
К сожалению, атопический дерматит невозможно “перерасти”.
Симптомы атопического дерматита у детей
Согласно последним исследованиям [3] у 45% малышей атопический дерматит дебютирует в возрасте от двух до шести месяцев. У 60% пациентов в течение первого года жизни.
При атопическом дерматите у детей клинические симптомы и локализация воспалений во многом зависят от возраста. Выделяют младенческую (до полутора лет), детскую (от полутора лет до полового созревания) и взрослую фазы. Общими для всех фаз являются следующие симптомы:
По характеру течения различают острую и хроническую стадии атопического дерматита, которые выражены разными признаками (симптомами):
● Острая стадия. На коже малыша могут появиться шершавые красные пятна (эритема), узелковые высыпания (папулы), припухлости, а также корочки (в том числе с мокнутием).
● Хроническая стадия. Сопровождается лихенизацией (утолщением кожи), трещинками на подошвах и ладонях, расчесами, усилением пигментации кожи век.
Причины атопического дерматита у детей
Атопический дерматит можно считать наследственным заболеванием, потому что важнейшую роль в его возникновении играет генетический фактор [3]:
Спровоцировать атопический дерматит у малыша могут и некоторые дородовые факторы: например, неправильное питание будущей мамы, контакт с токсичными веществами, перенесенные во время беременности инфекции, а также вредные привычки и стрессы.
Кроме того, атопический дерматит чаще развивается у малышей, которые перенесли кислородное голодание во время родов, родились недоношенными и находились на искусственном вскармливании (перинатальные факторы).
Диагностика атопического дерматита у детей
Долгое время считалось, что атопический дерматит у детей — это преимущественно аллергическое заболевание. Однако в настоящее время доказано, что это, в первую очередь, заболевание с нарушением функции эпидермиса! А пищевая аллергия выявляется лишь у 30-40% детей с атопическим дерматитом.
На проявление признаков атопического дерматита почти всегда влияют определенные триггеры внешней среды. Это могут быть хлорированная или “жесткая” вода, мыло, контакт с аллергеном, неблагоприятный климат и даже стресс. Еще один распространенный триггер — бактерии, которые проникают в кожу через поврежденный эпидермальный барьер.
Поставить диагноз “атопический дерматит у детей” может только врач (педиатр, дерматолог, аллерголог)! Он учитывает наличие внешних признаков заболевания и зуда, а также наследственный фактор. Для проведения диагностики детям могут быть назначены лабораторные исследования. Например:
Лечение атопического дерматита у детей
В современной медицине выделяют три степени тяжести атопического дерматита у детей:
Обращайте внимание на состав, желательно, чтобы эмоленты не вызывали привыкания. Их главные задачи — помочь коже вырабатывать собственные липиды, обеспечивая эффективное увлажнение и смягчение. Кроме того, постоянное применение эмолентов продлевает периоды ремиссий и облегчает симптоматику атопического дерматита.
Лечение (применение гормональных препаратов) при атопическом дерматите у детей может назначать только врач с учетом возраста, симптоматики, сопутствующих заболеваний и результатов анализов. Самолечение может быть опасно!
Профилактика атопического дерматита у детей
При атопическом дерматите различают первичные, вторичные и третичные профилактические меры.
1. Первичная профилактика
направлена на предупреждение возникновения атопического дерматита у малышей.
2. Вторичная профилактика
направлена на устранение факторов риска, которые при определенных условиях (стресс, ослабление иммунитета и т.п.) могут привести к возникновению, обострению и рецидиву атопического дерматита.
3.Третичная профилактика
— это комплекс мероприятий, направленных на предотвращение обострений или развития осложнений атопического дерматита.
Атопический дерматит у детей
Атопический дерматит у детей – это воспалительное заболевание кожи хронического рецидивирующего течения, возникающее в раннем детском возрасте вследствие повышенной чувствительности к пищевым и контактным аллергенам. Атопический дерматит у детей проявляется высыпаниями на коже, сопровождающимися зудом, мокнутием, образованием эрозий, корок, участков шелушения и лихенизации. Диагноз атопического дерматита у детей основан на данных анамнеза, кожных проб, исследования уровня общего и специфических IgE. При атопическом дерматите у детей показаны диета, местная и системная медикаментозная терапия, физиолечение, психологическая помощь, санаторно-курортное лечение.
МКБ-10
Общие сведения
Атопический дерматит является самым ранним и наиболее частым проявлением реакции гиперчувствительности организма на действие аллергенов окружающей среды: на его долю приходится 80-85% случаев аллергии у детей раннего возраста. Как правило, атопический дерматит у ребенка проявляется уже в течение первого года жизни; может протекать с периодическими обострениями и временным стиханием кожных проявлений до пубертатного периода и даже сохраняться в зрелом возрасте.
Проблема атопического дерматита у детей, в виду своей актуальности, нуждается в пристальном внимании со стороны педиатрии, детской дерматологии, аллергологии-иммунологии, детской гастроэнтерологии, диетологии.
Причины
К более частому развитию атопического дерматита у детей приводит гипоксия плода, перенесенная во внутриутробном периоде или во время родов. В первые месяцы жизни ребенка симптомы атопического дерматита могут быть вызваны пищевой аллергией вследствие раннего перевода на искусственные смеси, неправильного введения прикорма, перекармливания, имеющихся нарушений процесса пищеварения и частых инфекционно-вирусных заболеваний. Атопический дерматит чаще возникает у детей с гастритом, энтероколитом, дисбактериозом, гельминтозами.
Нередко к развитию атопического дерматита у детей приводит чрезмерное потребление высокоаллергенных продуктов матерью в период беременности и лактации. Пищевая сенсибилизация, связанная с физиологической незрелостью пищеварительной системы и особенностями иммунного ответа новорожденного, оказывает значительное влияние на формирование и последующее развитие всех аллергических заболеваний у ребенка.
Причинно-значимыми аллергенами могут выступать пыльца, продукты жизнедеятельности домашних клещей, пылевой фактор, бытовая химия, лекарственные средства и др. Спровоцировать обострение атопического дерматита у детей могут психоэмоциональное перенапряжение, перевозбуждение, ухудшение экологической ситуации, пассивное курение, сезонные изменения погоды, снижение иммунной защиты.
Классификация
В развитии атопического дерматита у детей различают несколько стадий: начальную, стадию выраженных изменений, стадию ремиссии и стадию клинического выздоровления. В зависимости от возраста манифестации и клинико-морфологических особенностей кожных проявлений выделяют три формы атопического дерматита у детей:
Эти формы могут переходить в одна в другую или заканчиваться ремиссией с уменьшением симптомов. Различают легкое, средней степени и тяжелое течение атопического дерматита у детей. Клинико-этиологические варианты атопического дерматита по причинно-значимому аллергену включают кожную сенсибилизацию с преобладанием пищевой, клещевой, грибковой, пыльцевой и другой аллергии. По степени распространенности процесса атопический дерматит у детей может быть:
Симптомы
Клиническая картина атопического дерматита у детей достаточно многообразна, зависит от возраста ребенка, остроты и распространенности процесса, тяжести течения патологии.
Младенческая форма атопического дерматита характеризуется острым воспалительным процессом – отеком, гиперемией кожи, появлением на ней эритематозных пятен и узелковых высыпаний (серозных папул и микровезикул), сопровождающихся резко выраженной экссудацией, при вскрытии – мокнутием, образованием эрозий («серозных колодцев»), корочек, шелушением.
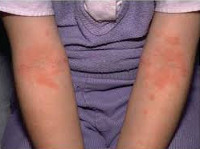
Для детской формы атопического дерматита свойственны эритематосквамозное и лихеноидное кожное поражение. У детей наблюдается гиперемия и выраженная сухость кожи с большим количеством отрубевидных чешуек; усиление кожного рисунка, гиперкератоз, обильно шелушение, болезненные трещины, упорный зуд с усилением в ночное время. Кожные изменения располагаются преимущественно на сгибательных поверхностях конечностей (локтевых сгибах, подколенных ямках), ладонно-подошвенной поверхности, паховых и ягодичных складках, тыльной поверхности шеи. Характерно «атопическое лицо» с гиперпигментацией и шелушением век, линией Денье-Моргана (складкой кожи под нижним веком), вычесываем бровей.
Проявления атопического дерматита у детей подросткового возраста характеризуются резко выраженной лихенизацией, наличием сухих шелушащихся папул и бляшек, локализующихся преимущественно на коже лица (вокруг глаз и рта), шеи, верхней части туловища, локтевых сгибах, вокруг запястий, на тыльной стороне кистей и ступней, пальцах рук и ног. Для этой формы атопического дерматита у детей характерно обострение симптомов в холодное время года.
Диагностика
Диагностика атопического дерматита у ребенка проводится детским дерматологом и детским аллергологом-иммунологом. Во время осмотра специалисты оценивают общее состояние ребенка; состояние кожных покровов (степень влажности, сухости, тургор, дермографизм); морфологию, характер и локализацию высыпаний; площадь поражения кожи, выраженность проявлений. Диагноз атопического дерматита подтверждается при наличии у детей 3-х и более обязательных и дополнительных диагностических критериев.
Вне обострения атопического дерматита у детей применяют постановку кожных проб с аллергенами методом скарификации или прик-теста для выявления IgE-опосредованных аллергических реакций. Определение содержания общего и специфических IgE в сыворотке крови методами ИФА, РИСТ, РАСТ предпочтительно при обострении, тяжелом течении и постоянных рецидивах атопического дерматита у детей.
Атопический дерматит у детей необходимо дифференцировать с себорейным дерматитом, чесоткой, микробной экземой, ихтиозом, псориазом, розовым лишаем, иммунодефицитными заболеваниями.
Лечение атопического дерматита у детей
Лечение направленно на уменьшение выраженности аллергического воспаления кожи, исключение провоцирующих факторов, десенсибилизацию организма, предотвращение и снижение частоты обострений и инфекционных осложнений. Комплексное лечение включает диету, гипоаллергенный режим, системную и местную фармакотерапию, физиотерапию, реабилитацию и психологическую помощь.
В лечении атопического дерматита у детей используют фототерапию (УФA и УФB облучение, ПУВА-терапию), рефлексотерапию, гипербарическую оксигенацию, курорто- и климатотерапию. Детям с атопическим дерматитом нередко требуется помощь детского психолога.
Прогноз и профилактика
Наиболее выраженные в раннем возрасте проявления атопического дерматита могут уменьшаться или полностью исчезать по мере роста и развития детей. У большинства пациентов симптомы атопического дерматита сохраняются и рецидивируют в течение всей жизни.
Неблагоприятными прогностическими факторами являются: ранний дебют заболевания в возрасте до 2-3 мес., отягощенная наследственность, тяжелое течение, сочетание атопического дерматита у детей с другой аллергической патологией и персистирующей инфекцией.
Цель первичной профилактики атопического дерматита – предотвращение сенсибилизации детей из групп риска путем максимального ограничения высоких антигенных нагрузок на организм беременной и кормящей матери и ее ребенка. Исключительно грудное вскармливание в первые 3 месяца жизни ребенка, обогащение рациона матери и ребенка лактобактериями снижает риск раннего развития атопического дерматита у предрасположенных к нему детей.
Вторичная профилактика заключается в предупреждении обострений атопического дерматита у детей за счет соблюдения диеты, исключения контакта с провоцирующими факторами, коррекции хронической патологии, десенсибилизирущей терапии, санаторно-курортного лечения.
При атопическом дерматите важен правильный ежедневный уход за кожей детей, включающий очищение (непродолжительные прохладные ванны, теплый душ), смягчение и увлажнение специальными средствами лечебной дерматологической косметики; выбор одежды и белья из натуральных материалов.
Проблемы терапии атопического дерматита у грудных детей
Атопический дерматит (АД) представляет собой заболевание кожи, возникающее, как правило, в раннем детстве у лиц с наследственной предрасположенностью к атопии и имеющее тенденцию к хроническому рецидивирующему течению [1]. В пользу
Атопический дерматит (АД) представляет собой заболевание кожи, возникающее, как правило, в раннем детстве у лиц с наследственной предрасположенностью к атопии и имеющее тенденцию к хроническому рецидивирующему течению [1].
В пользу наследственной предрасположенности говорят многочисленные данные о высокой частоте семейных случаев заболевания. В 60–75% случаев в семьях детей с АД выявляются атопические болезни, такие как бронхиальная астма, аллергический ринит, нейродермит и др. [1, 2, 3, 4]. Следует отметить, что примерно у 10% пациентов установить аллергическую природу АД не удается — и механизмы развития этой формы болезни остаются пока не ясными [5, 6, 7].
Под нашим наблюдением в течение двух первых лет жизни находились дети с высокой степенью риска развития атопии [8]. Все матери этих детей страдали бронхиальной астмой или сочетанием бронхиальной астмы с другим атопическим заболеванием. 19,4% отцов также имели атопические заболевания, причем 8,3% из них страдали АД. Более чем у половины старших братьев и сестер наших пациентов (53,8%) также отмечались заболевания атопической природы, при этом в 23% случаев — АД. Наконец, у 24,3% из 252 близких и дальних родственников имелись атопические заболевания, а АД был отмечен в 10,4% случаев.
АД развился у наблюдаемых нами детей более чем в половине случаев (58,3%). Еще у 16,7% детей диагностировался дерматореспираторный синдром. Таким образом, атопический дерматит в «чистом виде» или в сочетании с бронхообструктивным синдромом был зарегистрирован у 75% детей с отягощенной по атопии наследственностью.
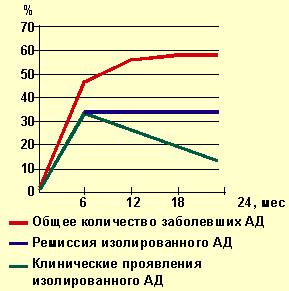 |
| Рисунок 1. Динамика заболеваемости атопическим дерматитом |
На рисунках 1, 2 представлена динамика выявления клинических проявлений АД и дерматореспираторного синдрома у наблюдаемых нами детей с отягощенной наследственностью. Характерно, что в подавляющем большинстве наблюдений АД клинически манифестировал на первом году жизни, т. е. в грудном возрасте. К 6 мес АД страдали 47,2% детей, к 12 мес — 55,6% всех детей, на втором году жизни заболевание клинически проявилось только у 2,7% детей.
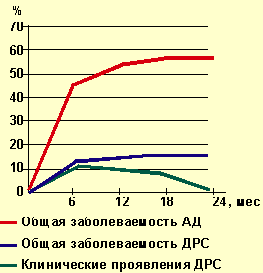 |
| Рисунок 2. Динамика заболеваемости атопическим дерматитом и дермореспираторным синдромом |
К окончанию второго года жизни почти у половины детей с АД отмечалась ремиссия клинических проявлений, а при дерматореспираторном синдроме ремиссия к концу второго года жизни регистрировалась в 2/3 случаев.
Из приведенных данных видно, что максимальной частоты клинические проявления АД достигают в первые 6 мес жизни, причем впервые признаки заболевания выявляются в основном от 8 до 12 нед жизни. Грудной возраст, таким образом, является основным «плацдармом» для развития этой патологии. Обычно заболевание начинается с эритематозного и эритематозно-сквамозного поражения кожи лица в виде «молочной корки». Через 1–2 нед появляются зуд и общая сухость кожных покровов, особенно наружных поверхностей.
И еще через 1–3 нед процесс может распространиться на кожу рук, бедер и голеней. Изменение последовательности высыпаний и появление первичных элементов в начале заболевания на теле, а затем на лице или на теле и на лице одновременно отмечается редко. Но, как правило, прогностически данный признак считается более неблагоприятным: именно у этой группы грудных детей атопический дерматит принимает распространенный и тяжелый характер поражения кожных покровов. К началу второго года жизни обычно наблюдается эволюция высыпаний в виде постепенного формирования синдрома лихенизации с максимальной локализацией в складках суставов конечностей и на шее.
Характерно, что у детей с отягощенным по атопии анамнезом симптомы АД появлялись не только достаточно рано (6–8-я нед жизни), но, как правило, и возникали на фоне грудного вскармливания, так как более 70% наблюдаемых нами детей получали в этот период жизни грудное молоко. Тщательно проанализировав характер и качество вскармливания, мы отметили, что на фоне грудного вскармливания более чем 30% матерей вводили в рацион детей фруктовые соки, пюре и другой прикорм, чтобы «витаминизировать питание». Однако статистически достоверного различия в качестве питания по отношению к группе контроля (дети без отягощенной по атопии наследственности) выявлено не было. Более того, значительная часть матерей практиковали преимущественно грудное вскармливание.
Таким образом, проведенные нами наблюдения показали, что у детей группы высокого риска по развитию АД одной из серьезных проблем является ранняя клиническая манифестация заболевания, которая развивается в большинстве случаев на фоне естественного вскармливания.
Следует отметить, что на практике диагноз АД в подавляющем большинстве случаев устанавливается клинически, так как в грудном возрасте отмечается физиологически более высокий уровень JgE, чем во все последующие периоды жизни. Так, исследование уровня JgE в динамике на протяжении первых 24 мес жизни показало, что в группе риска по развитию атопии уровень JgE был отчетливо выше, чем в контрольной группе. Но и в контрольной группе этот показатель был повышен, а выявленные критерии в целом не имели статистически и диагностически значимых различий. Следует отметить, что среди детей, у которых атопический дерматит или дерматореспираторный синдром клинически выявились в первые два года жизни, уровень JgE оказался наиболее высоким и имел статистически значимое различие с группой контроля. Этот показатель у них был даже выше, чем у детей, также родившихся от матерей, страдающих бронхиальной астмой, но не имевших в первые два года жизни клинических проявлений атопического заболевания. Это согласуется с положением о JgE-опосредованном генезе АД при генетически детерминированной предрасположенности к атопии, но, к сожалению, не обеспечивает надежного лабораторного критерия диагностики АД у детей первых лет жизни.
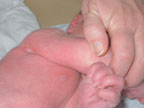 |
| Рисунок 3. Эритематозное поражение кожи при кандидозе |
Наиболее распространенной диагностической ошибкой является ситуация, когда за проявления АД принимают кандидоз кожи у грудных детей. Кандидоз — одно из часто встречающихся инфекционных заболеваний кожи, его распространенность среди грудных детей может достигать 10–24% [9]. Первая отличительная черта кандидоза — более раннее начало, обычно на 2–3-й нед жизни. Вторая — преобладание эритематозного поражения кожи. Оно может проявляться интертригинозным дерматитом, который локализуется в крупных складках и характеризуется наличием эритематозных, отечных участков с мелкими пузырьками и пустулами по периферии (рис. 3). Эту форму кандидоза нередко принимают за опрелости. В отличие от опрелостей эрозивные поверхности имеют четко контурированные, фестончатые края с подрытым эпидермальным венчиком. Поверхность эрозий гладкая, блестящая, напряженная. Другим вариантом поражения является кандидозный пеленочный дерматит. Обычно он развивается у детей, которые являются носителями грибов Candida в кишечнике. Заболевание проявляется эритематозными бляшками с бахромчатой границей и четко выраженным краем. Они формируются при слиянии многочисленных папул и везикул. Пустулы-сателлиты, локализующиеся на окружающей коже, представляют собой очаги локализованной кандидозной инфекции. Обычно в процесс вовлекается кожа перианальной области, паховых складок, промежности и нижней части брюшной стенки (рис. 4). У мальчиков может быть поражена кожа мошонки и полового члена. Третьим вариантом кандидоза кожи является везикулезное и эритематозное поражение гладкой кожи, для которого характерно преобладание влажных эрозивных, гладких, напряженных, блестящих участков темно-красного цвета (эритематозное поражение) или наличие значительного количества мелких дряблых пузырьков (везикулезная форма). Таким образом, особенностями кандидоза являются темно-красный цвет и лаковый блеск, влажная, а не мокнущая поверхность, отчетливые границы и фестончатые очертания; узкая периферическая каемка, представленная воротничком тонкого белого, мацерированного рогового слоя эпидермиса; наличие вокруг основных больших эрозий свежих пузырьков, пустул и мелких эрозий.
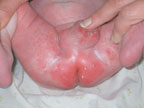 |
| Рисунок 4. Кандидозный пеленочный дерматит |
Третьей отличительной чертой является отсутствие сухости кожи и отсутствие зуда даже при распространенном поражении кожи.
Лечение АД в грудном возрасте — одна из самых сложных и неблагодарных задач для врача-педиатра. Так как клинический дебют АД в большинстве случаев приходится на период грудного вскармливания, многие специалисты — нутрициологи, педиатры и аллергологи рекомендуют назначать матерям строгую элиминационную диету с ограничением не только высокоаллергенных продуктов, таких как шоколад, клубника, цитрусовые и т. д., но и сахара, соли, цельного молока, жирного, копченого, острого и т. д. Нередко дело доходит до того, что кормящей женщине предписывают соблюдение диеты, крайне бедной не только микроэлементами и витаминами, но и основными нутриентами — белками, жирами и углеводами. Это, естественно, отражается на составе грудного молока, которое теряет свое основное назначение — обеспечивать растущий организм ребенка всем необходимым для нормального роста и развития [11]. При этом многочисленные исследования последних лет показали, что четкой зависимости между проведением элиминационной диеты матери и выраженностью АД не существует, поэтому держать мать «на голодном пайке» нет никакой необходимости.
Диета кормящей женщины при развитии АД у ребенка должна оставаться полноценной и разнообразной, с незначительным ограничением основных продуктов питания (табл. 1). Исключение составляют только высокоаллергенные продукты, являющиеся облигатными аллергенами, — шоколад, какао, натуральный кофе, орехи, мед, цитрусовые, красная икра. Их применять не следует. Необходимо также избегать избыточного потребления сахара, конфет и других сладостей, так как при этом возрастает содержание сахара в грудном молоке. Лук, чеснок, редька, редис, пряности, острые приправы, а также крепкие бульоны — мясные, рыбные, куриные и грибные — могут изменять вкус грудного молока, поэтому их вводят в рацион любой кормящей женщины в ограниченном количестве. В то же время кормящим женщинам можно порекомендовать включить в свой рацион специальные продукты: быстрорастворимые молочные напитки «Фемилак» (Россия), «Энфа-мама» (США), «Думил Мама плюс» (Дания) и др., которые способствуют обогащению грудного молока витаминами и микронутриентами. Эти напитки используются как отдельно, так и для приготовления различных блюд. Количество напитков устанавливается индивидуально, с учетом характера питания и состояния здоровья женщины, и составляет, как правило, 1–2 порции (200–500 мл) в день.
Если АД развивается у ребенка, находящегося на искусственном или смешанном вскармливании, особенно в том случае когда установлена пищевая аллергия к белкам коровьего молока, целесообразно перевести малыша на лечебное питание. При этом возможны, по крайней мере, три варианта: использование смесей, основанных на высокой степени гидролиза белков коровьего молока; применение смесей на соевой основе и использование молока других животных или смесей, приготовленных на основе молока других животных. Каждый из этих вариантов имеет свои достоинства и недостатки. Однако у них есть один общий недостаток — ни одна из смесей не служит адекватной заменой грудного вскармливания по своим протективным, биологическим и социальным свойствам.
Смеси, созданные на основе соевого белка, в течение последних десятилетий довольно широко использовались с лечебной целью у детей с непереносимостью белков коровьего молока. Таких смесей довольно много: Алсой (Нестле, Швейцария), Бона-соя (Кюмос, Финляндия), Вайсоя (Вайт Лабораториз, Великобритания), Нутрилак-соя (Россия), Нутрисоя (Нутриция, Голландия), Симилак-изомил (Эббот Лабораториз, США), СМА Нурсой (Вайт Ледерле, США), Соя Семп (Семпер, Швеция), Фрисосой (Фризленд, Голландия), Хумана ЛП (Хумана, Германия), Хайнц-соевая смесь (Хайнц, США), Энфамил-соя (Мид Джонсон, США) и др.
Белковый субстрат этих продуктов представлен изолятом соевого белка. При этом он лишен таких компонентов, как ингибитор трипсина. Нет в соевых смесях и трудно перевариваемых углеводов (рафиноза и стахиоза), которые содержатся в соевых бобах и вызывают у детей метеоризм и диарею. Жировой компонент смесей формируется за счет растительных масел (подсолнечного, соевого, кокосового, кукурузного, рапсового и др.), обеспечивающих оптимальное соотношение полиненасыщенных жирных кислот. Углеводный компонент чаще представлен декстрин-мальтозой, оказывающей благоприятное воздействие на микробный пейзаж кишечника. В отдельных смесях углеводный компонент может быть представлен также глюкозой, сахарозой или фруктозой в различных соотношениях. Все соевые смеси лишены лактозы, поэтому они используются не только при непереносимости белков коровьего молока, но и для лечебного питания детей с лактазной недостаточностью, алактазией и галактоземией. Смеси на соевой основе обогащены витаминами, минералами, микроэлементами, таурином, т. е. максимально адаптированы для питания детей первого года жизни.
Нежелательным эффектом смесей на соевой основе является появление у детей склонности к запорам и нарастающая в последние годы аллергия к белкам сои.
Наиболее радикальным лечебным эффектом при непереносимости белков коровьего молока обладают продукты для искусственного вскармливания на молочной основе с высокой степенью гидролиза белков. К ним относятся такие смеси, как Алфаре (Нестле, Швейцария), Нутрамиген и Прегестимил (Мид Джонсон, США), Пепти-Юниор (Нутриция, Голландия).
Имеются также гипоаллергенные смеси типа Хумана ГА 1, Хумана ГА 2 (Хумана, Германия), ХИПП ГА (Хипп, Австрия), Фрисопеп (Фризленд, Голландия), которые характеризуются низкой степенью гидролиза белков коровьего молока. Показания к назначению смесей с высокой и низкой степенью гидролиза различны:
Молочная основа этих смесей подвергается ферментативному гидролизу, что позволяет существенно снизить антигенный потенциал белкового компонента. Причем чем выше степень гидролиза и меньше размер пептидов, полученных в результате гидролиза, тем ниже антигенный потенциал белкового компонента смеси. В качестве белкового субстрата используются различные источники белка: казеин и сывороточные белки молока, белки мяса, бычий коллаген и др. Специальные технологии (обработка на адсорбентах) предусматривают очистку их от нежелательных продуктов гидролиза. В состав этих лечебных смесей также входят растительные масла, среднецепочечные триглицериды, полимеры глюкозы, витаминно-минеральный комплекс, таурин. Аминокислотный состав таких смесей приближен к таковому у женского молока.
Эти смеси обладают очень низкими антигенными свойствами, легко усваиваются организмом ребенка первого года жизни, не требуют напряжения ферментативной и соковыделительной функций его желудочно-кишечного тракта. Включение полимеров глюкозы (модифицированных крахмалов) способствует снижению осмолярности, а также стимулирует рост нормальной микрофлоры в кишечнике.
Отрицательной особенностью лечебных смесей с высокой степенью гидролиза белков являются неудовлетворительные органолептические свойства. Смеси имеют запах и привкус подгоревшего или прогорклого молока и дети привыкают к ним с большим трудом, даже в первые дни жизни. Необходимы большое терпение, а порой и изобретательность (вплоть до введения различных фруктовых, овощных и иных добавок) со стороны родителей и медицинского персонала, чтобы приучить ребенка к данному продукту питания.
Наконец, существует, как уже говорилось, третий вариант. Можно попытаться заменить коровье молоко в питании ребенка на молоко других животных (козье, кобылье, верблюжье). Но необходимо помнить, что это будет неполноценная замена (неадаптированное питание), которая при большом объеме и/или длительном применении неизбежно приведет к отрицательным последствиям, свойственным использованию неадаптированных смесей (перегрузка белками, жирами, диапедезное желудочно-кишечное кровотечение). Следует отметить, что в настоящее время появились попытки создания адаптированной смеси на основе козьего молока (Нэнни, Новая Зеландия).
К сожалению, при генетически детерминированном АД у детей грудного возраста диетотерапия оказывает весьма ограниченное воздействие. Значительно более эффективна она при АД, ассоциированном с пищевой аллергией. В этом случае диетотерапия является решающей.
Системная терапия АД у грудных детей крайне затруднена в силу возрастных ограничений, накладываемых на использование большинства противоаллергических препаратов. К применению у детей первого года жизни разрешены только некоторые антигистаминные лекарственные средства I поколения. Это димедрол, супрастин, фенистил, пипольфен и кетотифен (табл. 2). Назначение их показано при выраженном зуде у ребенка. При этом следует обратить внимание на две особенности антигистаминов I поколения. Во-первых, все препараты I поколения назначаются на ограниченный период времени — не более 7–10 дней, так как после 7–8-го дня начинается падение их фармакологического эффекта. Во-вторых, в раннем детском возрасте эта группа лекарственных средств может вызывать парадоксальную реакцию — возбуждение, нарушение сна, беспокойство. Особенно часто парадоксальная реакция отмечается при использовании дифенгидрамина (димедрола). Появление такой реакции является поводом к отмене препаратов.
 |
| Таблица 2. Антигистаминные препараты, разрешенные к применению у детей грудного возраста |
Таким образом, основное место в терапии АД у грудных детей занимает местное лечение, которое направлено на уменьшение сухости и зуда кожных покровов и местное противовоспалительное воздействие.
Уменьшение сухости, отчасти способствующее также облегчению зуда, достигается благодаря широкому использованию увлажняющих и смягчающих средств. С этой целью прежде всего показано проведение ежедневных ванн с температурой воды, не превышающей 36°С, при этом исключается использование мыла, моющих гелей и пенок.
Процедуру приема гигиенической ванны у детей с АД следует проводить не чаще 1 раза в 10 дней, при этом необходимо использовать специальные мыла, например обогащенное липидами «мыло с кольд-кремом», мыло с нейтральной реакцией pH. Обычное туалетное мыло, мыло «Детское» и другие способны значительно усилить сухость кожи.
Помимо ежедневных ванн, следует в течение дня дополнительно орошать кожу ребенка, используя спреи термальных вод. Появление мокнутий не исключает орошения кожи и даже купания. Однако в этих случаях после купания необходима дополнительная обработка участков, на которых возникли мокнутия, примочками и влажно-высыхающими повязками.
При отсутствии мокнутий сразу после ванны необходимо обработать кожу ребенка смягчающими лечебными кремами, например кремом «Мюстела», применять который рекомендуется с периода новорожденности, или «Атодерм».
В первые дни терапии АД необходимо обрабатывать кожу ребенка смягчающим кремом многократно, до 5–10 раз. Желательно сочетать эти процедуры с орошением кожи и последующим промоканием мягкой пеленкой или салфеткой, а также нанесением смягчающего крема.
Второе направление местной терапии — назначение противовоспалительных средств. Долгое время в лечении грудных детей использовались местные средства, приготовленные на основе нафталана, дегтя, АСД III фракции и т. д. Эти препараты обладают невысокой эффективностью и в большинстве случаев представляют собой нестандартизованные лекарственные средства. Большим шагом вперед явилось появление в последние годы нового нестероидного противовоспалительного препарата — пимекролимуса (ингибитора кальциневрина) в виде 1% крема элидел. Использование этого нестероидного препарата разрешено с
3-месячного возраста. Поэтому не случайно в настоящее время местная терапия АД строится следующим образом [7]:
Следует отметить, что назначение наружных глюкокортикостероидов грудным детям также имеет ряд особенностей: во-первых, используются нефторированные препараты; во-вторых, накладываются ограничения на дозирование препаратов (табл. 3). Это позволило значительно повысить безопасность современных наружных глюкокортикостеродов и использовать их длительное время, необходимое для полного исчезновения кожных проявлений АД.
Также нельзя не отметить совершенствование наружной терапии АД в грудном возрасте: широкое использование увлажнения и смягчения кожных покровов как основу терапии; своевременное (раннее) введение в схему терапии АД нестероидного препарата 1% крема элидел, сдерживающее развитие симптомов АД и существенно сокращающее потребности в использовании глюкокортикостероидных препаратов у детей грудного возраста.
Г. А. Самсыгина, доктор медицинских наук, профессор
РГМУ, Москва
По вопросам литературы обращайтесь в редакцию.