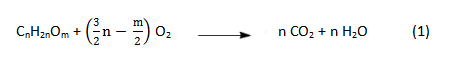в каком месте пламя самое горячее
Температура открытого пламени и огня в зажигалке

Виды пламени
Свечение огня делится на два вида:
Почти каждое свечение видимо для человеческого глаза, но не каждое способно испускать нужное количество светового потока.
Свечение пламени обуславливается следующими факторами.
Наиболее общая причина свечения — это присутствие в пламени твёрдого вещества.
Температура пламени

Некоторое количество горючего вещества при сжигании выделяет определённое количество теплоты. Если строение вещества известно, то можно рассчитать объём и состав полученных продуктов горения. А если знать удельную теплоту этих веществ, то можно рассчитать ту максимальную температуру, которую достигнет пламя.
Стоит помнить о том, что если вещество горит в воздухе, то на каждый объём вступающего в реакцию кислорода приходится четыре объёма инертного азота. А так как в пламени присутствует азот, он нагревается теплотой, которая выделяется при реакции. Исходя из этого можно сделать вывод о том, что температура пламени будет состоять из температуры продуктов горения и азота.
Невозможно точно определить температуру, но можно это сделать приблизительно, так как удельная теплота изменяется с температурой.
Вот некоторые показатели по температуре открытого огня в разных материалах.
Пламя свечи

За счёт диффузии в центр поступает немного больше кислорода. Там происходит последующее окисление топлива и температурный показатель растёт. Но для полного сгорания топлива этого недостаточно. Внизу и в центре содержатся частицы угля и несгоревшие капельки. Они светятся из-за сильного нагревания. А вот испарившееся топливо, а также продукты сгорания, вода и углекислый газ практически не светятся. В самом верху наибольшая концентрация кислорода. Там не догоревшие частицы, которые в центре светились, догорают. Именно по этой причине эта зона практически не светится, хотя там наиболее высокий температурный показатель.
Классификация пламени
Классифицируют свечение огня следующим образом.
В диффузном ламинарном пламени выделяют три оболочки (зоны). Внутри конуса пламени существует:

По реально существующим смесям газовоздушным распространение всегда осложнено возмущающими внешними воздействиями, которые обусловлены трением, конвективными потоками, силами тяжести и прочими факторами.
Именно из-за этого реальная скорость распространения от нормальной всегда отличается. В зависимости от того, какой характер носит скорость распространения, различают такие диапазоны:
Пламя окислительное
Оно располагается в самой верхней части огня, которая имеет наибольший температурный показатель. В этой зоне горючие вещества почти полностью превращены в продукты горения. Здесь наблюдается недостаток топлива и избыток кислорода. Именно по этой причине вещества, которые помещены в эту зону, окисляются интенсивно.
Пламя восстановительное
Эта часть наиболее близка к центру или находится чуть ниже его. Здесь мало кислорода для горения и много топлива. Если в эту область внести вещество, в котором имеется кислород, то он отнимется у вещества.
Температура огня в зажигалке
Зажигалка — это устройство портативное, которое предназначено для получения огня. Она может быть бензиново или газовой, в зависимости от применяемого топлива. Ещё существуют зажигалки, в которых собственного топлива нет. Они предназначаются для поджига газовой плиты. Качественная турбозажигалка — это прибор относительно сложный. Температура огня в ней может достигать 1300 градусов.
Химический состав и цвет пламени
У карманных зажигалок небольшой размер, это позволяет их переносить без каких-либо проблем. Довольно редко можно встретить настольную зажигалку. Ведь они из-за своих больших размеров для переноски не предназначены. Их дизайн разнообразен. Есть зажигалки каминные. Они имеют небольшую толщину и ширину, но довольно длинные.
На сегодняшний день становятся популярными рекламные зажигалки. Если в доме нет электроэнергии, то невозможно ей поджечь газовую плиту. Газ поджигает образующаяся электрическая дуга. Достоинствами этих зажигалок являются следующие качества.
Ускорилось развитие зажигалок в период Первой мировой войны. Солдаты начали применять спички для того, чтобы видеть в темноте дорогу, но их местоположение выдавала интенсивная вспышка при поджиге. Необходимость в огне без значительной вспышки способствовало развитию зажигалок.
В то время лидерами производства зажигалок «кремнёвых» были Германия и Австрия. Такое портативное устройство, которое предназначено для получения огня, находящиеся в кармане многих курильщиков, при неправильном обращении может таить в себе немало опасностей.
Зажигалка в период работы не должна вокруг себя разбрызгивать искры. Огонь должен быть стабильным и ровным. Температура огня в зажигалках карманных достигает примерно 800−1000 градусов. Свечение красного или оранжевого цвета вызвано частицами углерода, которые раскалились. Для бытовых горелок и турбозажигалок применяется в основном газ бутан, который легко сжигается, не имеет запаха и цвета. Бутан получают путём переработки при высоких температурах нефти, а также её фракций. Бутан — это легковоспламенимые углеводороды, но он абсолютно безопасен в конструкциях современных зажигалок.
Подобные зажигалки в быту очень полезны. Ими можно поджечь любой воспламеняющийся материал. В комплект турбозажигалок входит настольная подставка. Цвет пламени зависит от горючего материала и температуры горения. Пламя костра или камина в основном имеет пёстрый вид. Температура горения дерева ниже температуры горения фитиля свечи. Именно из-за этого цвет костра не жёлтый, а оранжевый.
Электрическая зажигалка была изобретена в 1770 году. В ней водородная струя воспламенялась от искры машины электрофорной. Со временем бензиновые зажигалки уступили место газовым, которые более удобные. В них обязательно должна находиться батарейка — источник энергии.
Не очень давно появились зажигалки сенсорные, в которых без механического воздействия происходит зажигание газа воздействием на сенсорный датчик. Сенсорные зажигалки карманного типа. В основном, в них содержится информация рекламного типа, которая нанесена при помощи тампонной или шелкотрафаретной печати.
Где самая горячая часть пламени
Люди с незапамятных времен покланялись и будут поклонятся огню в самых разных его ипостасях. На минутку задумайтесь пламя свечи отличается от пламя костра только размером и температурой! Во всем остальном их суть и строение одинаково. Всмотритесь внимательно в пламя свечи и Вы увидите строго определенные зоны пламени. Визуально их выделяют три. Разные зоны окрашены по разному и идентичны от свечи к свече в любом уголке мира в независимости от используемого свечного материала*. Без сомнения такое строение имеет сакральный смысл!
В этой статье мы кратко и просто расскажем о известных физических свойствах пламени свечи, данная информация будет особенно полезна тем, кто хочет стать настоящих профессионалом в изготовлении свечей (см. статью ошибки в горении фитиля).
*Примечание: обычные условия, а не лабораторные условия.
С химической точки зрение горение выглядит так:
В процессе горения происходит расщепление сложных углеводородов (парафин, стеарин, воск и т.д) под действием кислорода до углекислого газа и воды. Процесс горения происходит непрерывно за счет подъема (как в капилляре) по фитилю расплавленного свечного материала с последующим его сжиганием.
Примечание: Пламя – светящаяся зона образующаяся при горении.
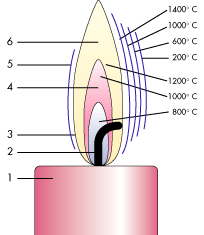
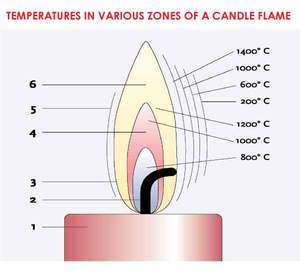
Пламя свечи разделено на различные светящиеся и температурные области, которые легко видны невооруженным глазом:
1 – свеча
2 – фитиль, изогнутый к краю пламени со светящимся кончиком
3 – синяя зона горения:
4 – «темная» зона горения:
5 – основная зона реакции (сжигания):
6 – светящаяся зона
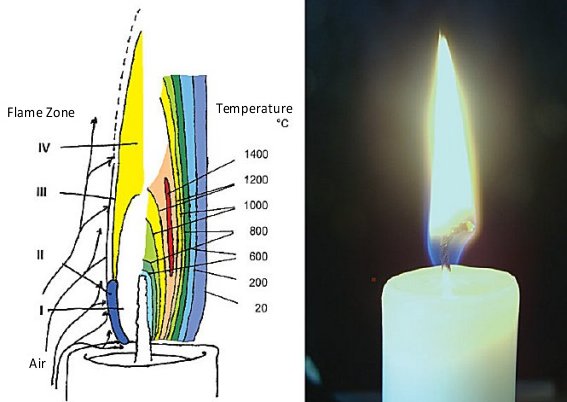
Примечание: считается, что самое горячее пламя на кончике свечи, это не совсем так. Самая горячая часть пламени в основной зоне реакции или чуть ниже.

Виды пламени
Свечение огня делится на два вида:
Почти каждое свечение видимо для человеческого глаза, но не каждое способно испускать нужное количество светового потока.
Свечение пламени обуславливается следующими факторами.
Наиболее общая причина свечения — это присутствие в пламени твёрдого вещества.
Температура пламени

Некоторое количество горючего вещества при сжигании выделяет определённое количество теплоты. Если строение вещества известно, то можно рассчитать объём и состав полученных продуктов горения. А если знать удельную теплоту этих веществ, то можно рассчитать ту максимальную температуру, которую достигнет пламя.
Стоит помнить о том, что если вещество горит в воздухе, то на каждый объём вступающего в реакцию кислорода приходится четыре объёма инертного азота. А так как в пламени присутствует азот, он нагревается теплотой, которая выделяется при реакции. Исходя из этого можно сделать вывод о том, что температура пламени будет состоять из температуры продуктов горения и азота.
Невозможно точно определить температуру, но можно это сделать приблизительно, так как удельная теплота изменяется с температурой.
Вот некоторые показатели по температуре открытого огня в разных материалах.
Пламя свечи

За счёт диффузии в центр поступает немного больше кислорода. Там происходит последующее окисление топлива и температурный показатель растёт. Но для полного сгорания топлива этого недостаточно. Внизу и в центре содержатся частицы угля и несгоревшие капельки. Они светятся из-за сильного нагревания. А вот испарившееся топливо, а также продукты сгорания, вода и углекислый газ практически не светятся. В самом верху наибольшая концентрация кислорода. Там не догоревшие частицы, которые в центре светились, догорают. Именно по этой причине эта зона практически не светится, хотя там наиболее высокий температурный показатель.
Классификация пламени
Классифицируют свечение огня следующим образом.
В диффузном ламинарном пламени выделяют три оболочки (зоны). Внутри конуса пламени существует:

По реально существующим смесям газовоздушным распространение всегда осложнено возмущающими внешними воздействиями, которые обусловлены трением, конвективными потоками, силами тяжести и прочими факторами.
Именно из-за этого реальная скорость распространения от нормальной всегда отличается. В зависимости от того, какой характер носит скорость распространения, различают такие диапазоны:
Пламя окислительное
Оно располагается в самой верхней части огня, которая имеет наибольший температурный показатель. В этой зоне горючие вещества почти полностью превращены в продукты горения. Здесь наблюдается недостаток топлива и избыток кислорода. Именно по этой причине вещества, которые помещены в эту зону, окисляются интенсивно.
Пламя восстановительное
Эта часть наиболее близка к центру или находится чуть ниже его. Здесь мало кислорода для горения и много топлива. Если в эту область внести вещество, в котором имеется кислород, то он отнимется у вещества.
Температура огня в зажигалке
Зажигалка — это устройство портативное, которое предназначено для получения огня. Она может быть бензиново или газовой, в зависимости от применяемого топлива. Ещё существуют зажигалки, в которых собственного топлива нет. Они предназначаются для поджига газовой плиты. Качественная турбозажигалка — это прибор относительно сложный. Температура огня в ней может достигать 1300 градусов.
Химический состав и цвет пламени
У карманных зажигалок небольшой размер, это позволяет их переносить без каких-либо проблем. Довольно редко можно встретить настольную зажигалку. Ведь они из-за своих больших размеров для переноски не предназначены. Их дизайн разнообразен. Есть зажигалки каминные. Они имеют небольшую толщину и ширину, но довольно длинные.
На сегодняшний день становятся популярными рекламные зажигалки. Если в доме нет электроэнергии, то невозможно ей поджечь газовую плиту. Газ поджигает образующаяся электрическая дуга. Достоинствами этих зажигалок являются следующие качества.

Ускорилось развитие зажигалок в период Первой мировой войны. Солдаты начали применять спички для того, чтобы видеть в темноте дорогу, но их местоположение выдавала интенсивная вспышка при поджиге. Необходимость в огне без значительной вспышки способствовало развитию зажигалок.
В то время лидерами производства зажигалок «кремнёвых» были Германия и Австрия. Такое портативное устройство, которое предназначено для получения огня, находящиеся в кармане многих курильщиков, при неправильном обращении может таить в себе немало опасностей.
Зажигалка в период работы не должна вокруг себя разбрызгивать искры. Огонь должен быть стабильным и ровным. Температура огня в зажигалках карманных достигает примерно 800−1000 градусов. Свечение красного или оранжевого цвета вызвано частицами углерода, которые раскалились. Для бытовых горелок и турбозажигалок применяется в основном газ бутан, который легко сжигается, не имеет запаха и цвета. Бутан получают путём переработки при высоких температурах нефти, а также её фракций. Бутан — это легковоспламенимые углеводороды, но он абсолютно безопасен в конструкциях современных зажигалок.
Подобные зажигалки в быту очень полезны. Ими можно поджечь любой воспламеняющийся материал. В комплект турбозажигалок входит настольная подставка. Цвет пламени зависит от горючего материала и температуры горения. Пламя костра или камина в основном имеет пёстрый вид. Температура горения дерева ниже температуры горения фитиля свечи. Именно из-за этого цвет костра не жёлтый, а оранжевый.

Электрическая зажигалка была изобретена в 1770 году. В ней водородная струя воспламенялась от искры машины электрофорной. Со временем бензиновые зажигалки уступили место газовым, которые более удобные. В них обязательно должна находиться батарейка — источник энергии.
Не очень давно появились зажигалки сенсорные, в которых без механического воздействия происходит зажигание газа воздействием на сенсорный датчик. Сенсорные зажигалки карманного типа. В основном, в них содержится информация рекламного типа, которая нанесена при помощи тампонной или шелкотрафаретной печати.
Чем проклинать тьму,
лучше зажечь хотя бы
одну маленькую свечу.
Конфуций
В начале
Первые попытки понять механизм горения связаны с именами англичанина Роберта Бойля, француза Антуана Лорана Лавуазье и русского Михаила Васильевича Ломоносова. Оказалось, что при горении вещество никуда не «исчезает», как наивно полагали когда-то, а превращается в другие вещества, в основном газообразные и потому невидимые. Лавуазье в 1774 году впервые показал, что при горении из воздуха уходит примерно пятая его часть. В течение XIX века ученые подробно исследовали физические и химические процессы, сопровождающие горение. Необходимость таких работ была вызвана прежде всего пожарами и взрывами в шахтах.
Существуют два вида пламени. Топливо и окислитель (чаще всего кислород) могут принудительно или самопроизвольно подводиться к зоне горения порознь и смешиваться уже в пламени. А могут смешиваться заранее — такие смеси способны гореть или даже взрываться в отсутствие воздуха, как, например, пороха, пиротехнические смеси для фейерверков, ракетные топлива. Горение может происходить как с участием кислорода, поступающего в зону горения с воздухом, так и при помощи кислорода, заключенного в веществе-окислителе. Одно из таких веществ — бертолетова соль (хлорат калия KClO3); это вещество легко отдает кислород. Сильный окислитель — азотная кислота HNO3: в чистом виде она воспламеняет многие органические вещества. Нитраты, соли азотной кислоты (например, в виде удобрения — калийной или аммиачной селитры), легко воспламеняются, если смешаны с горючими веществами. Еще один мощный окислитель, тетраоксид азота N2O4 — компонент ракетных топлив. Кислород могут заменить и такие сильные окислители, как, например, хлор, в котором горят многие вещества, или фтор. Чистый фтор — один из самых сильных окислителей, в его струе горит вода.
Цепные реакции
Основы теории горения и распространения пламени были заложены в конце 20-х годов прошлого столетия. В результате этих исследований были открыты разветвленные цепные реакции. За это открытие отечественный физикохимик Николай Николаевич Семенов и английский исследователь Сирил Хиншельвуд были в 1956 году удостоены Нобелевской премии по химии. Более простые неразветвленные цепные реакции открыл еще в 1913 году немецкий химик Макс Боденштейн на примере реакции водорода с хлором. Суммарно реакция выражается простым уравнением H2 + Cl2 = 2HCl. На самом деле она идет с участием очень активных осколков молекул — так называемых свободных радикалов. Под действием света в ультрафиолетовой и синей областях спектра или при высокой температуре молекулы хлора распадаются на атомы, которые и начинают длинную (иногда до миллиона звеньев) цепочку превращений; каждое из этих превращений называется элементарной реакцией:
Cl + H2 → HCl + H,
H + Cl2 → HCl + Cl и т. д.
На каждой стадии (звене реакции) происходит исчезновение одного активного центра (атома водорода или хлора) и одновременно появляется новый активный центр, продолжающий цепь. Цепи обрываются, когда встречаются две активные частицы, например Cl + Cl → Cl2. Каждая цепь распространяется очень быстро, поэтому, если генерировать «первоначальные» активные частицы с высокой скоростью, реакция пойдет так быстро, что может привести к взрыву.
Таким образом, за ничтожный промежуток времени одна активная частица (атом H) превращается в три (атом водорода и два гидроксильных радикала OH), которые запускают уже три цепи вместо одной. В результате число цепей лавинообразно растет, что моментально приводит к взрыву смеси водорода и кислорода, поскольку в этой реакции выделяется много тепловой энергии. Атомы кислорода присутствуют в пламени и при горении других веществ. Их можно обнаружить, если направить струю сжатого воздуха поперек верхней части пламени горелки. При этом в воздухе обнаружится характерный запах озона — это атомы кислорода «прилипли» к молекулам кислорода с образованием молекул озона: О + О2 = О3, которые и были вынесены из пламени холодным воздухом.
Возможность взрыва смеси кислорода (или воздуха) со многими горючими газами — водородом, угарным газом, метаном, ацетиленом — зависит от условий, в основном от температуры, состава и давления смеси. Так, если в результате утечки бытового газа на кухне (он состоит в основном из метана) его содержание в воздухе превысит 5%, то смесь взорвется от пламени спички или зажигалки и даже от маленькой искры, проскочившей в выключателе при зажигании света. Взрыва не будет, если цепи обрываются быстрее, чем успевают разветвляться. Именно поэтому была безопасной лампа для шахтеров, которую английский химик Хэмфри Дэви разработал в 1816 году, ничего не зная о химии пламени. В этой лампе открытый огонь был отгорожен от внешней атмосферы (которая могла оказаться взрывоопасной) частой металлической сеткой. На поверхности металла активные частицы эффективно исчезают, превращаясь в стабильные молекулы, и потому не могут проникнуть во внешнюю среду.
Полный механизм разветвленно-цепных реакций очень сложен и может включать более сотни элементарных реакций. К разветвленно-цепным относятся многие реакции окисления и горения неорганических и органических соединений. Таковой же будет и реакция деления ядер тяжелых элементов, например плутония или урана, под воздействием нейтронов, которые выступают аналогами активных частиц в химических реакциях. Проникая в ядро тяжелого элемента, нейтроны вызывают его деление, что сопровождается выделением очень большой энергии; одновременно из ядра вылетают новые нейтроны, которые вызывают деление соседних ядер. Химические и ядерные разветвленно-цепные процессы описываются сходными математическими моделями.
Что надо для начала
Чтобы началось горение, нужно выполнить ряд условий. Прежде всего, температура горючего вещества должна превышать некое предельное значение, которое называется температурой воспламенения. Знаменитый роман Рэя Брэдбери «451 градус по Фаренгейту» назван так потому, что примерно при этой температуре (233°C) загорается бумага. Это «температура воспламенения», выше которой твердое топливо выделяет горючие пары или газообразные продукты разложения в количестве, достаточном для их устойчивого горения. Примерно такая же температура воспламенения и у сухой сосновой древесины.
Температура пламени зависит от природы горючего вещества и от условий горения. Так, температура в пламени метана на воздухе достигает 1900°C, а при горении в кислороде — 2700°C. Еще более горячее пламя дают при сгорании в чистом кислороде водород (2800°C) и ацетилен (3000°C). Недаром пламя ацетиленовой горелки легко режет почти любой металл. Самую же высокую температуру, около 5000°C (она зафиксирована в Книге рекордов Гиннесса), дает при сгорании в кислороде легкокипящая жидкость — субнитрид углерода С4N2 (это вещество имеет строение дицианоацетилена NC–C=C–CN). А по некоторым сведениям, при горении его в атмосфере озона температура может доходить до 5700°C. Если же эту жидкость поджечь на воздухе, она сгорит красным коптящим пламенем с зелено-фиолетовой каймой. С другой стороны, известны и холодные пламена. Так, например, горят при низких давлениях пары фосфора. Сравнительно холодное пламя получается и при окислении в определенных условиях сероуглерода и легких углеводородов; например, пропан дает холодное пламя при пониженном давлении и температуре от 260–320°C.
Только в последней четверти ХХ века стал проясняться механизм процессов, происходящих в пламени многих горючих веществ. Механизм этот очень сложен. Исходные молекулы обычно слишком велики, чтобы, реагируя с кислородом, непосредственно превратиться в продукты реакции. Так, например, горение октана, одного из компонентов бензина, выражается уравнением 2С8Н18 + 25О2 = 16СО2 + 18Н2О. Однако все 8 атомов углерода и 18 атомов водорода в молекуле октана никак не могут одновременно соединиться с 50 атомами кислорода: для этого должно разорваться множество химических связей и образоваться множество новых. Реакция горения происходит многостадийно — так, чтобы на каждой стадии разрывалось и образовывалось лишь небольшое число химических связей, и процесс состоит из множества последовательно протекающих элементарных реакций, совокупность которых и представляется наблюдателю как пламя. Изучать элементарные реакции сложно прежде всего потому, что концентрации реакционно-способных промежуточных частиц в пламени крайне малы.
Внутри пламени
Оптическое зондирование разных участков пламени с помощью лазеров позволило установить качественный и количественный состав присутствующих там активных частиц — осколков молекул горючего вещества. Оказалось, что даже в простой с виду реакции горения водорода в кислороде 2Н2 + О2 = 2Н2О происходит более 20 элементарных реакций с участием молекул О2, Н2, О3, Н2О2, Н2О, активных частиц Н, О, ОН, НО2. Вот, например, что написал об этой реакции английский химик Кеннет Бэйли в 1937 году: «Уравнение реакции соединения водорода с кислородом — первое уравнение, с которым знакомится большинство начинающих изучать химию. Реакция эта кажется им очень простой. Но даже профессиональные химики бывают несколько поражены, увидев книгу в сотню страниц под названием «Реакция кислорода с водородом», опубликованную Хиншельвудом и Уильямсоном в 1934 году». К этому можно добавить, что в 1948 году была опубликована значительно большая по объему монография А. Б. Налбандяна и В. В. Воеводского под названием «Механизм окисления и горения водорода».
Современные методы исследования позволили изучить отдельные стадии подобных процессов, измерить скорость, с которой различные активные частицы реагируют друг с другом и со стабильными молекулами при разных температурах. Зная механизм отдельных стадий процесса, можно «собрать» и весь процесс, то есть смоделировать пламя. Сложность такого моделирования заключается не только в изучении всего комплекса элементарных химических реакций, но и в необходимости учитывать процессы диффузии частиц, теплопереноса и конвекционных потоков в пламени (именно последние устраивают завораживающую игру языков горящего костра).
Откуда все берется
Основное топливо современной промышленности — углеводороды, начиная от простейшего, метана, и кончая тяжелыми углеводородами, которые содержатся в мазуте. Пламя даже простейшего углеводорода — метана может включать до ста элементарных реакций. При этом далеко не все из них изучены достаточно подробно. Когда горят тяжелые углеводороды, например те, что содержатся в парафине, их молекулы не могут достичь зоны горения, оставаясь целыми. Еще на подходе к пламени они из-за высокой температуры расщепляются на осколки. При этом от молекул обычно отщепляются группы, содержащие два атома углерода, например С8Н18 → С2Н5 + С6Н13. Активные частицы с нечетным числом атомов углерода могут отщеплять атомы водорода, образуя соединения с двойными С=С и тройными С≡С связями. Было обнаружено, что в пламени такие соединения могут вступать в реакции, которые не были ранее известны химикам, поскольку вне пламени они не идут, например С2Н2 + О → СН2 + СО, СН2 + О2 → СО2 + Н + Н.
Постепенная потеря водорода исходными молекулами приводит к увеличению в них доли углерода, пока не образуются частицы С2Н2, С2Н, С2. Зона сине-голубого пламени обусловлена свечением в этой зоне возбужденных частиц С2 и СН. Если доступ кислорода в зону горения ограничен, то эти частицы не окисляются, а собираются в агрегаты — полимеризуются по схеме С2Н + С2Н2 → С4Н2 + Н, С2Н + С4Н2 → С6Н2 + Н и т. д.