можно ли вылечить цитомегаловирус у детей
Цитомегаловирусная инфекция у детей
Цитомегаловирусная инфекция у детей — это инфекционное заболевание, которое вызвано цитомегаловирусом и поражает слюнные железы, внутренние органы, ЦНС. В детстве патология чаще возникает при трансплацентарном или интранатальном заражении. Локализованные формы проявляются сиаладенитом, гепатитом, нефритом и т. д., распространенный вариант инфекции характеризуется поражением головного мозга, легких, почек и органов ЖКТ. Диагностика предполагает идентификацию возбудителя цитологическими, гистологическими, серологическими и молекулярно-биологическими методами. Лечение цитомегаловирусной болезни проводится специфическим иммуноглобулином и противовирусными препаратами.
МКБ-10
Общие сведения
Заражение цитомегаловирусной инфекцией (ЦМВИ) наблюдается у 20%‒60% всего детского населения, но в большинстве случаев оно протекает бессимптомно. Внутриутробное инфицирование вирусом от больной матери происходит в 30-50% случаев, при этом до 18% младенцев после рождения имеют клинические симптомы. Учитывая полиморфизм клинической картины, ранняя диагностика и лечение у детей затруднены. Цитомегаловирусная инфекция представляет серьезную опасность, особенно для плода и новорожденного, у которых заболевание, как правило, вызывает необратимые осложнения.
Причины
Болезнь вызвана герпесвирусом 5 типа — Cytomegalovirus hominis. Он имеет 6 штаммов: Davis, AD 169, Kerr, C-87, Esp, Towne, причем ребенок может быть инфицирован сразу несколькими подтипами возбудителя. Цитомегаловирус (ЦМВ) имеет ДНК-геном, отличается медленной репликацией и сравнительно низкой вирулентностью. Он термолабилен, уничтожается при температуре более 56°С, но длительно сохраняет жизнеспособность в комнатных условиях.
При врожденной ЦВМИ передача вируса к плоду происходит трансплацентарно, при перинатальной инфекции — путем контакта с вагинальными выделениями матери, грудным молоком или препаратами крови. Риск заражения увеличивается, если мать с острой формой болезни не получает специфическое лечение. В постнатальном периоде ребенок чаще всего заражается от ближайших родственников и сверстников воздушно-капельным или контактно-бытовым путем.
Патогенез
Попадая в кровь, вирус реплицируется в лейкоцитах, моноцитах и макрофагах и в дальнейшем он пожизненно сохраняется в лимфоцитарных органах. Зачастую процесс выражается в виде латентной инфекции, при которой у ребенка нет симптомов, и ему не требуется лечение. Активность цитомегаловируса зависит от состояния иммунитета: при физиологической иммунной недостаточности, которая наблюдается у детей раннего возраста, риск манифестной цитомегаловирусной инфекции возрастает в разы.
При угнетении защитных факторов организма (системы интерлейкинов, Т-лимфоцитов) возбудитель разносится с кровью к разным органам. К нему наиболее чувствительны клетки слюнных желез, где часто происходят специфические патоморфологические изменения. Заболевание характеризуется образованием крупных цитомегаловирусных клеток («совиный глаз»). Кроме того, при ЦМВИ возможен фиброз железистых органов, отложение кальцификатов.
Классификация
В детской инфектологии различают врожденную (внутриутробную) и приобретенную формы патологии. По течению инфекция бывает острой (до 3 месяцев), подострой (3-6 месяцев), затяжной (6-12 месяцев) и хронической (более 1 года). По клиническим признакам выделяют локализованный (сиаладенит, нефрит, гепатит, энцефалит) и генерализованный вариант. С учетом тяжести течения цитомегаловирусную болезнь делят на 3 степени:
Симптомы
Врожденная ЦМВИ
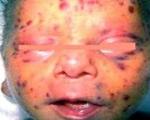
У пациентов с манифестной врожденной форме цитомегаловирусной болезни признаки наблюдаются с первых дней жизни. Типичный комплекс симптомов у новорожденных детей включает недоношенность и/или низкую массу тела, поражение гепатобилиарной системы (увеличение печени, желтуха, гепатиты и циррозы), лимфаденопатии и геморрагическую сыпь на коже. Если инфицирование произошло на ранних сроках беременности, ребенок рождается с аномалиями — микроцефалией, гипоплазией легких, атрезией пищевода.
Приобретенная ЦМВИ
Приобретенная цитомегаловирусная болезнь обычно протекает в субклинической или латентной форме, когда у ребенка возникают гриппоподобные симптомы, субфебрильная температура без видимой причины. После заражения инфекция может длительное время себя не проявлять и давать обострения при снижении иммунного статуса, действии неблагоприятных эндо- или экзогенных факторов.
Течение манифестной приобретенной формы напоминает инфекционный мононуклеоз. У ребенка внезапно появляется слабость, повышается температура, беспокоят недомогание, головные боли, отсутствует аппетит. Позже присоединяются сильные боли в горле, увеличиваются подчелюстные и шейные лимфоузлы. Если цитомегаловирусная инфекция проявляется сиаладенитом, наблюдается резкое увеличение и болезненность слюнных желез на фоне фебрильной лихорадки.
Генерализованная ЦМВИ
При генерализованном варианте течения инфекции у детей поражается бронхолегочная система (пневмонии, дыхательная недостаточность), ЖКТ (энтероколит, мальабсорбция), печень (желтуха, цитомегаловирусный гепатит, билиарный цирроз). Особенно опасно вовлечение в процесс нервной системы, что проявляется судорожным синдромом, парезами и параличами, задержкой психомоторного развития.
Осложнения
Негативные последствия выявляются преимущественно у детей, страдающих врожденной цитомегаловирусной инфекцией. В 58% случаев после тяжелой формы заболевания остаются неврологические нарушения (парезы, соматосенсорная недостаточность), 28% детей отстают в умственном развитии. Для ЦМВИ характерно поражение слуха вплоть до глухоты (25% случаев) и необратимое снижение зрения (8-15%).
Поражение клеток при цитомегаловирусной болезни создает благоприятные условия для возникновения аутоиммунных поражений — системной красной волчанки, рассеянного склероза, гломерулонефрита. Иногда после малосимптомной врожденной цитомегаловирусной инфекции осложнения наблюдаются в отдаленном периоде (в возрасте ребенка 2-5 лет). В основном они проявляются неврологическими расстройствами и поражением органов чувств.
Диагностика
Цитомегаловирусная инфекция отличается многообразием клинических признаков и часто протекает под маской других патологий, что затрудняет работу детского инфекциониста. На первичном приеме, помимо стандартного физикального осмотра, врач собирает детальный акушерский анамнез, чтобы выявить факторы риска антенатального инфицирования. Диагноз ЦМВИ правомочен только при лабораторном подтверждении, для чего используют следующие методы:
Инструментальные методы подбираются соответственно форме заболевания. Для оценки структурно-функциональных особенностей печени и билиарного тракта назначают УЗИ органов брюшной полости. КТ и МРТ головного мозга информативны для выявления врожденных пороков и кальцификатов. Рентгенография ОГК необходима при симптомах дыхательных расстройств. По показаниям ребенка направляют на консультации к профильным специалистам— кардиологу, неврологу, отоларингологу.
Лечение цитомегаловирусной инфекции у детей
Препаратом выбора у новорожденных и детей первого года жизни является специфический антицитомегаловирусный иммуноглобулин, который имеет повышенную концентрацию IgG. Лечение начинают при манифестных формах заболевания и проводят по схеме: вначале вводится высокая доза препарата, а спустя 9-10 дней дозировку постепенно уменьшают, контролируя степень ответа на терапию и активность процесса.
В старшем возрасте перечень препаратов, применяемых при цитомегаловирусной инфекции, значительно расширяется. Лечение включает противовирусные средства из группы нуклеозидов и нуклеотидов (ганцикловир, валганцикловир), производные ортофосфорной кислоты (фоскарнет). При легкой и среднетяжелой формах назначают интерфероны, иммуностимуляторы.
Для купирования интоксикации показано обильное питье (при легких формах), при среднетяжелых и тяжелых клинических вариантах рекомендована инфузионная терапия. Патогенетическая терапия подбирается в соответствии с характером течения болезни и может включать пищеварительные ферменты, ингибиторы протеиназ, гемостатики. Для предупреждения вторичных бактериальных осложнений используют антибиотики (макролиды, цефалоспорины, гликопептиды).
Прогноз и профилактика
При малосимптомных приобретенных вариантах цитомегаловирусная болезнь протекает без осложнений, зачастую у ребенка выявляется только латентное носительство. Угрозу для жизни и здоровья представляют тяжелые генерализованные инфекции, которые в 50-60% случаев сопровождаются осложнениями, несмотря на проводимое лечение. Особо опасно поражение цитомегаловирусом для детей с иммунодефицитными состояниями.
Основу профилактики врожденной ЦМВИ составляет обязательное лабораторное обследование женщин на носительство цитомегаловируса, которое проводится при планировании зачатия и во время беременности. Если в семье есть пациент с цитомегаловирусной инфекцией, необходимо ограничить его общение с ребенком и обеспечить лечение. Карантинно-изоляционные мероприятия в отношении заболевших и контактных лиц не производятся.
Цитомегаловирус у детей

Цитомегаловирусная инфекция (ЦМВИ, цитомегалия) – широко распространенное вирусное заболевание, характеризующееся многообразными проявлениями, которые могут отличаться бессимптомным течением или же приводить к тяжелым генерализованным формам болезни с поражением внутренних органов и центральной нервной системы, что у детей нередко приводит к инвалидизации. i Поэтому педиатров во всем мире волнует важный вопрос – как лечить цитомегаловирус у детей.
Особенности возбудителя инфекции
Возбудителем ЦМВИ является ДНК-содержащий вирус Cytomegalovirus hominis, который был открыт в средине прошлого века. Согласно международной классификации, ЦМВ относится к группе Human Herpesvirus-5 (вирус герпеса 5 типа) и обладает свойствами, общими для всех представителей семейства Herpesviridae. Геном ЦМВ человека – самый крупный из всех геномов представителей герпесвирусов.
Инфицированность цитомегаловирусом в разных странах достаточно высокая. От 20 до 60 % детей и от 40 до 95% взрослых в мире инфицировано этим вирусом. Среди беременных женщин частота выявления антител к ЦМВ по разным исследованиям колеблется от 40 до 90%. Первичная ЦМВИ развивается примерно в 1%. Внутриутробное инфицирование плода у будущих матерей с первичной ЦМВИ во время беременности достигает 30-50%. ii Но только у 5-18% наблюдается манифестная врожденная ЦМВИ, которая характеризуется тяжелым течением и может привести к летальному исходу.
Попав однажды в организм, ЦМВ персистирует в нем пожизненно. При этом большая часть людей даже не подозревает о его наличии. По мнению исследователей, ЦМВ-инфекция наиболее широко распространена в развивающихся странах, а в развитых странах – в регионах с низким социально-экономическим статусом. Заболеваемость ЦМВ эндемична и не подвержена сезонным колебаниям. Эндемичность – это постоянная приуроченностъ инфекционных болезней или их групп к определенным территориям, обусловленная специфическими локальными природно-географическими условиями. Европейским региональным бюро ВОЗ ЦМВИ отнесена к группе болезней, которые определяют будущее инфекционной патологии.
В настоящее время рост заболеваемости цитомегаловирусом отмечается во всех странах мира, что связано как с повышением качества диагностики, так и с истинным ростом заболевания. Установлено, что многие серонегативные женщины (с отсутствием в крови антител к ЦМВ) детородного возраста имеют высокий риск заражения во время беременности и рождения ребенка с врожденной ЦМВ-инфекцией.
Пути заражения ЦМВИ
Источником вируса могут служить моча, секрет из носоглотки, цервикальная слизь и влагалищный секрет, сперма, грудное молоко, слезы, слюна, кровь. Иначе говоря, ЦМВ может передаваться при кормлении, трансфузии крови и ее препаратов, контактах с секретами и экскретами, оседающими на игрушках и предметах обихода, а также через все биологические жидкости и выделения организма (слюна, моча и др.), при кашле (контактно-бытовой путь заражения).
Ученые в жизни человека выделяют два наиболее уязвимых периода, когда цитомегаловирус передаётся от человека к человеку. Прежде всего, это период жизни ребенка до 5 лет. Также передача вируса малышу может произойти внутриутробно через плаценту во время беременности, при грудном вскармливании, контактным и воздушно-капельным путями.[iii] Вторым критическим периодом является возраст 16-30 лет, когда инфицирование чаще всего осуществляется половым путем.
У будущих матерей с латентной ЦМВ-инфекцией плод поражается далеко не всегда. Необходимым условием для этого является обострение инфекции у матери с развитием вирусемии (состояния организма, при котором вирусы попадают в кровоток и могут распространяться по всему телу) и последующим заражением плода. Вероятность внутриутробного заболевания всегда значительно выше при инфицировании матери во время беременности.
Цитомегаловирусная инфекция по МКБ 10
Согласно Международной классификации болезней, выделяют врожденную ЦМВИ и приобретенные формы, проявляющиеся в виде пневмонии, гепатита, панкреатита, инфекционного мононуклеоза, хориоретинита, тромбоцитопении и других заболеваний.
Также цитомегаловирусную инфекцию классифицируют по клиническим проявлениям:
Степень тяжести заболевания может быть легкой, среднетяжелой и тяжелой.
При легкой степени тяжести и крепком иммунитете поражения внутренних органов незначительны и не сопровождаются функциональными нарушениями. При среднетяжелой степени отмечаются поражения внутренних органов, которые сопровождаются функциональными нарушениями. Тяжелая форма характеризуется резко выраженной интоксикацией и поражениями внутренних органов с тяжелыми функциональными нарушениями.
Среди возможных исходов заболевания:
Цитомегаловирус у ребенка: симптомы
При ЦМВ инкубационный период колеблется от 2-х до 4-12 недель. О перинатальном развитии заболевания можно судить по выявлению клинических признаков болезни у новорожденного. Врожденная ЦМВИ проявляется не позже, чем в течение первых двух недель жизни ребенка. Если же симптомы наблюдаются позже, это свидетельствует о приобретенной ЦМВИ в послеродовом периоде. Причем ребенок может заразиться как от матери через слюну, грудное молоко, так и от ухаживающего персонала при воздушно-капельном пути передачи возбудителей болезни. Также инфицирование может произойти при переливании донорской крови новорожденному.
Существует три формы острой врожденной цитомегаловирусной инфекции:
Первая форма с триадой симптомов:
а) желтуха, которая по своим проявлениям напоминает гипербилирубинемию новорожденных с постепенным исчезновением в течение двух-трех месяцев;
б) гепатоспленомегалия – вторичный патологический синдром, который сопровождает течение многих заболеваний и характеризуется значительным одновременным увеличением в размерах печени и селезенки;
в) геморрагический синдром – патологическое состояние, характеризующееся повышенной кровоточивостью сосудов и проявляющееся петехиями (мелкими кровоизлияниями на коже), экхимозами (крупными кровоизлияния в кожу или слизистую оболочку), носовым и пупочным кровотечением, кровоизлияниями в склеры, кровавой рвотой и меленой – черными дегтеобразными испражнениями, которые формируются при обильных кровотечениях из разных отделов желудочно-кишечного тракта.
Вторая форма цитомегаловирусной инфекции
проявляется энцефалитом со слабовыраженной клинической симптоматикой и проявлением следующих признаков:
Третья форма ЦМВИ
проявляется поражением висцеральных органов и характеризуется высокой летальностью в первые недели жизни.
Цитомегаловирус у грудничка
По данным статистики, у большей части новорожденных ЦМВИ не развивается из-за наличия высокого уровня протективных антител у беременной или они переносят инфекцию в бессимптомной форме.
Однако, из всех врожденно инфицированных детей примерно 10% рождаются с симптомами инфекционного процесса. Характер поражения плода и новорожденного зависит от сроков инфицирования и отличается многообразием проявлений – от серьезных дефектов развития и генерализованных форм до бессимптомного течения инфекции. Конечно, чаще всего источником заражения цитомегаловирусной инфекцией новорожденных и детей первого года жизни, родившихся неинфицированными от серопозитивных по ЦМВИ матерей, являются сами матери. Наиболее значимым фактором передачи в этом случае служит грудное молоко, содержащее вирус.
Обследование новорожденного целесообразно проводить совместно с обследованием матери. Диагностика ЦМВИ проводится на основании данных специфических лабораторных исследований, в том числе анализа крови с выявлением антител IgG.
Последствия цитомегаловирусной инфекции у детей
У ребенка в ближайшие два года после рождения или позднее при наличии ЦМВ в организме могут быть выявлены дефекты зрения, слуха, зубов, нарушение поведения, отставание в умственном развитии, ДЦП. iv
Цитомегаловирус во многих случаях опасен для жизни и здоровья ребенка. При острой форме врожденной ЦМВИ гибель детей наступает в первые недели или месяцы жизни, чаще всего от присоединившихся бактериальных инфекций. У детей, перенесших острую форму заболевания, отмечается волнообразное течение хронической формы ЦМВИ. Часто формируются врожденные пороки развития ЦНС, в частности микроцефалия – почти в 40% случаев. Может развиться хронический гепатит, в редких случаях переходящий в цирроз. Изменения в легких у 25% детей характеризуются развитием пневмосклероза и фиброза.
Если в течение первых двух триместров беременности выявлена первичная ЦМВИ, в некоторых случаях может возникнуть вопрос о прерывании беременности, поскольку прогнозирование вероятных исходов беременности, осложненной вирусом, представляет собой непростую задачу. ЦМВИ отличается от других TORCH-инфекций тем, что поражения плода, вызываемые инфекцией, могут возникать в течение всех трех триместров.
Как лечить цитомегаловирус у детей
При активной ЦМВИ показан особый режим дня и соблюдение определенной диеты, которую порекомендует врач. Также необходимо комплексное медикаментозное лечение и применение противовирусных препаратов, которые борются с вирусом и не допускают развития осложнений. Один из таких препаратов, который разрешен для лечения детей с первых дней жизни, – это противовирусный препарат ВИФЕРОН, который применяется при ЦМВИ и сопутствующих заболеваниях. Противовирусные свойства позволяют ему блокировать размножение вируса, а иммуномодулирующий эффект способствует восстановлению иммунитета. Препарат разработан в результате фундаментальных исследований в области иммунологии, доказавших, что в присутствии антиоксидантов (витамины С, Е и другие) усиливается противовирусное действие основного действующего вещества – интерферона.
Инструкция по применению для новорожденных и недоношенных детей
Рекомендуемая доза препарата ВИФЕРОН Свечи для новорожденных, в т.ч. недоношенных с гестационным возрастом более 34 недель, – препарат 150 000 ME ежедневно по 1 суппозиторию 2 раза/сут через 12 ч. Курс лечения – 5 суток.
Недоношенным новорожденным с гестационным возрастом менее 34 недель назначают ВИФЕРОН 150 000 ME ежедневно по 1 суппозиторию 3 раза/сут через 8 ч. Курс лечения – 5 суток.
Рекомендуемое количество курсов для лечения цитомегаловируса у детей – 2-3 курса. Перерыв между курсами составляет 5 суток. По клиническим показаниям терапия может быть продолжена.
Инструкция по применению для беременных женщин
ВИФЕРОН также применяется для лечения цитомегаловируса у беременных женщин. Так, согласно исследованиям, применение препарата с целью сокращения развития патологических состояний у ребенка способствует снижению развития тяжелых форм внутриутробных инфекций (ВУИ) в 1,7 раза, а среднетяжелых ВУИ в 1,9 раз; сокращению числа детей с задержкой внутриутробного развития в 1,7 раза; уменьшению случаев развития асфиксии в 1,9 раз; снижению числа новорожденных с поражением ЦНС в 2,3 раза; оптимальному функциональному созреванию иммунной системы ребенка за счет антигенной стимуляции иммунитета плода. 2vi
Одно из главных преимуществ суппозиториев при лечении беременных женщин и новорожденных – бережное воздействие на организм. При использовании препарата в виде свечей печень и желудок не испытывают дополнительной нагрузки. Свечи (суппозитории) не содержат красителей и подсластителей, как сиропы и другие препараты для перорального приема. Следовательно, их применение позволяет свести к минимуму риск возникновения аллергических реакций.
Справочно-информационный материал
Автор статьи
Врач общей практики
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
История
Исходя из теории ко-эволюции вирусов с их хозяевами, считается, что герпетические вирусы появились в кембрийский период. В человеческой популяции герпетические вирусы распространены на протяжении тысячелетий. 24 ноября 1974 г. американским антропологом Д. Джохансоном в Великой рифтовой долине был обнаружен скелет афарского австралопитека Люси — предполагается, что это ветвь прародителей Homo sapiens [1]. Возраст Люси определен как 3,2–3,5 млн лет. В «слюне» Люси найдены три герпетических вируса — ЦМВ, вирус Эпштейна–Барр (ВЭБ), вирус простого герпеса 1-го типа (ВПГ 1-го типа). «Современные» люди, мигрировавшие из Африки от 60 до 100 тысяч лет назад, были уже носителями ЦМВ, ВЭБ, ВПГ 1-го типа и ВПГ 2-го типа. Человек со времен афарского австралопитека инфицировался вирусами в раннем детстве в семьях с большим количеством детей; вирусы передавались контактным путем со слюной, в грудном молоке и пр. Под воздействием, в том числе, и герпетических вирусов как компонентов комменсальной микробиоты, передаваемой от матери, эволюционировала иммунная система человека [2].
Характеристика возбудителя
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Патогенез
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
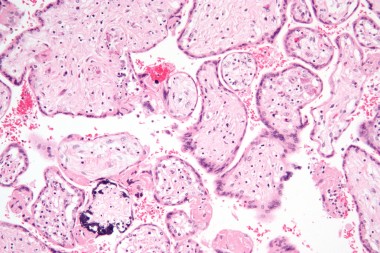
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Клиника ЦМВИ
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
У новорожденного антенатальная ЦМВИ проявляется симптомами «тяжелой инфекции» с полисистемным поражением: задержкой внутриутробного развития, часто — недоношенностью, гепатоспленомегалией, затяжной неконъюгационной и конъюгационной желтухой, тромбоцитопенической пурпурой, анемией, ДВС-синдромом с кровоизлиянием во внутренние органы, прежде всего в мозг, пневмонией, микроцефалией, хориоретинитом, увеитом, кардитом, различными вариантами поражения центральной нервной системы, в том числе продуктивным вентрикулоэнцефалитом с прогрессирующей гидроцефалией, а также — кортикальными или мозжечковыми пороками развития [13]. В дальнейшем этим детям присущи недостаточная прибавка веса, задержки психического и моторного развития, мышечная слабость, часто — длительная субфебрильная температура, стойкая анемия и тромбоцитопения, длительный гепатит с холестатическим синдромом и высоким риском фиброза и цирроза печени, мальабсорбция.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование