что такое репликация вируса гепатита с
Репликация вируса гепатита С: что это такое?
Гепатит С вызывают вирусы HCV (ВГС), которые являются антропонозными, то есть их жизненный цикл происходит только в организме человека. Они имеют высокий уровень гетерогенности генома, в результате чего постоянно мутируют на уровне последовательности нуклеотидов. Репликация вируса гепатита С происходит в печеночных клетках гепатоцитах, поэтому инфицированию подвергается именно этот орган.
Что такое репликация вируса?
ВГС представляет собой РНК-содержащий вирус. Он не имеет ДНК и вся генетическая информация закодирована в рибонуклеиновой кислоте. Для репликации (клонирования, размножения) вирусных агентов необходимы гепатоциты или клетки иммунитета лимфациты.
РНК содержится внутри вирусного агента и содержит более девяти тысяч нуклеотидов, из которых 30% могут подвергаться мутациям. Молекула находится в защитной капсуле, предохраняющую ее от разрушения. При проникновении внутрь клетки печени, она высвобождается и начинается процесс воспроизводства полноценного вирусного агента.
По сути, репликация — это стадия размножения вирусной частицы. Интенсивность репликативной фазы у гепатита С невелика по сравнению с другими типами инфекции. Именно поэтому заболевание сложно распознать даже в острой фазе. У большинства больных из-за вялого репликативного процесса оно сразу приобретает хроническое течение.
Стадии репликации HCV
Для выработки новых антител требуется время. Пока они появляются, вирионы снова мутируют. Считается, что они способны полностью изменять структуру каждую неделю. Таким образом, заболевание остается неизлечимым.
После проникновения патогенов в кровь многие из них погибают. Активная стадия репликации вируса начинается максимум через 2 недели после заражения, когда вирусные частицы достигают клеток печени. Эта фаза длиться до 3 месяцев и в некоторых случаях проявляется острыми симптомами, похожими на грипп. Если иммунная система сильная, то она способна победить заболевание.
Далее наступает носительство и латентная фаза, когда интенсивность размножения и активности вируса снижается. Длительность этого периода определяется состоянием иммунной системы и скоростью патологических изменений в печени.
На что влияет и от чего зависит показатель
Активность размножения патогена зависит от генотипа. Самая низкая интенсивность репликации у гепатита С 1b. Он практически сразу принимает хроническую форму и никак не проявляет себя. При этом вирусы размножаются и повреждают орган. В какой фазе находится заболевание можно узнать по маркерам гепатита С.
к.м.н. Альбина Белова
Имеются противопоказания. Перед применением проконсультируйтесь со специалистом.
Перед применением препаратов, указанных на сайте, проконсультируйтесь с врачом.
Вирусные гепатиты
Вирусный гепатит А
Гепатит А (ГА, hepatitis A) — острая энтеровирусная инфекция. Возбудитель — вирус гепатита А (ВГА, HAV) — энтеровирус типа 72. Геном вируса представлен однонитчатой РНК. Вирус гепатита А содержит единственный антиген (HA-Ag). Удельный вес гепатита А в суммарной заболеваемости вирусными гепатитами составляет 70–80 %. В структуре заболеваемости гепатитом А дети составляют до 80%, причем основная масса — дошкольники и школьники начальных классов.
Антитела IgM к вирусу гепатита А
Антитела IgM к вирусу гепатита А в сыворотке в норме отсутствуют. Достоверное подтверждение диагноза ГА достигается серологическими методами — обнаружением нарастания уровня специфических антител (анти-HAV), принадлежащих к иммуноглобулинам класса М (анти-HAV IgM). При гепатите А нарастание уровня антител, относящихся к IgM, начинается еще в инкубационном периоде, за 5–10 дней до появления первых симптомов болезни, и быстро прогрессирует. К моменту первичного обращения больного к врачу, уровень анти-HAV IgM успевает достичь высоких показателей, чтобы быть выявленным методом ИФА. Общепринято, что анти-HAV IgM у больных обнаруживаются в начале клинических проявлений заболевания и сохраняются до 6 мес после перенесенной инфекции.
Определение анти-HAV IgM
В настоящее время выделяют следующие формы вирусных гепатитов: гепатит А, гепатит В, гепатит С, гепатит D и гепатит Е. Для диагностики каждой из перечисленных форм вирусных гепатитов используют определенный перечень маркеров.
Определение анти-HAV IgG
Основной тест специфической диагностики гепатита А. Нарастание анти-HAV IgG происходит в более поздние сроки — в фазу реконвалесценции — и поэтому не может служить критерием ранней диагностики гепатита А. Выявление анти-HAV IgG у здоровых людей (возможно у 30–60% здорового населения) свидетельствует о предыдущей инфекции и иммунитете (ретроспективная диагностика).
Антиген гепатита А — HA-Ag
Появляется в сыворотке крови в конце преджелтушного периода. У большинства больных сохраняется в сыворотке крови на протяжение 1–2 недель заболевания. Из-за кратковременности пребывания в сыворотке крови больного для диагностических целей не используется.
Вирусный гепатит В
Гепатит В — вирусная антропонозная инфекция. Возбудитель — вирус гепатита В (ВГВ, HBV) — относится к семейству гепаднавирусов, ДНК-содержащих вирусов, поражающих клетки печени. Вирионы ВГВ имеют наружную липопротеидную оболочку и нуклеокапсид, содержащий двунитчатую циркулярную ДНК и ДНК-зависимую ДНК-полимеразу.
Поверхностный антиген (HBsAg) гепатита В в сыворотке
Поверхностный антиген гепатита В в сыворотке в норме отсутствует. Обнаружение поверхностного антигена (HBsAg) гепатита В в сыворотке подтверждает острое или хроническое инфицирование вирусом гепатита В (HBV).
При остром заболевании HBsAg выявляется в сыворотке крови в последние 1–2 недели инкубационного периода и в первые 2–3 недели клинического периода. Циркуляция HBsAg в крови может ограничиваться несколькими днями, поэтому следует стремиться к раннему первичному обследованию больных. Частота выявления HBsAg зависит от чувствительности используемого метода исследования. Метод ИФА позволяет выявить HBsAg более чем у 90% больных. Почти у 5% больных самые чувствительные методы исследования не обнаруживают HBsAg, в таких случаях этиология вирусного гепатита В подтверждается наличием анти-HBcAg IgM. Концентрация HBsAg в сыворотке крови при всех формах тяжести гепатита В в разгар заболевания имеет значительный диапазон колебаний, вместе с тем имеется определенная закономерность: в остром периоде существует обратная связь между концентрацией HBsAg в сыворотке и тяжестью болезни.
Высокая концентрация HBsAg чаще наблюдается при легких и средне-тяжелых формах болезни. При тяжелых и злокачественных формах, концентрация HBsAg в крови чаще низкая, причем у 20% больных с тяжелой формой и 30% со злокачественной антиген в крови может вообще не обнаруживаться. Появление на этом фоне у больных антител к HBsAg расценивается как неблагоприятный прогностический признак; он определяется при злокачественных формах (фульминантных) гепатита В.
При остром течении гепатита В, концентрация HBsAg в крови постепенно снижается, вплоть до полного исчезновения этого антигена. HBsAg исчезает у большинства больных в течение 3 мес от начала острой инфекции. Снижение концентрации HBsAg более чем на 50 % к концу 3-й недели острого периода, как правило, свидетельствует о близком завершении инфекционного процесса. Обычно у больных с высокой концентрацией HBsAg в разгар болезни он обнаруживается в крови в течение нескольких месяцев. У больных с низкой концентрацией HBsAg исчезает значительно раньше (иногда через несколько дней после начала заболевания). В целом, срок обнаружения HBsAg колеблется от нескольких дней до 4–5 мес. Максимальный срок обнаружения HBsAg при гладком течении острого гепатита В не превышает 6 мес от начала заболевания.
HBsAg может быть выявлен у практически здоровых людей, как правило, при профилактических или случайных исследованиях. В таких случаях исследуют другие маркеры вирусного гепатита В — анти-HBcAg IgM, анти-НВс IgG, анти-HBeAg и изучают функцию печени. При отрицательных результатах необходимы повторные исследования на HBsAg. Если повторные исследования крови в течение более 3 месяцев выявляют HBsAg, такого человека относят к хроническим носителям поверхностного антигена. Носительство HBsAg — довольно распространенное явление. В мире насчитывается более 300 млн носителей; у нас в стране — около 10 млн.
Исследование крови на наличие HBsAg применяют в следующих целях:
Антитела к поверхностному антигену гепатита В
Анти-HBsAg обнаруживаются в конце острого периода вирусного гепатита В или, чаще всего, через 3 мес от начала инфекции, изредка позже (до года) и сохраняются долго, в среднем 5 лет (Хазанов А.И., 1981). Анти-HBsAg обнаруживаются не сразу после исчезновения HBsAg. Продолжительность фазы «окна» варьирует от нескольких недель до нескольких месяцев. Антитела к поверхностному антигену гепатита В нейтрализуют вирус и рассматриваются как признак иммунитета. Они относятся к классу IgG.
Определение анти-HBsAg имеет важное значение для оценки течения гепатита В и его исходов, так как характеризует иммунный ответ конкретного больного. Это надежный критерий развития постинфекционного иммунитета и выздоровления. Выявление анти-HBsAg может служить критерием ретроспективной диагностики гепатита ранее не уточненной этиологии.
Анти-HBsAg свидетельствуют о ранее перенесенной инфекции. Выявление антител к HBsAg играет важную роль в определении контингента для вакцинации против гепатита В. Согласно рекомендациям ВОЗ, если уровень анти-HBsAg составляет менее 10 мМЕ/л, таким лицам показана вакцинация против гепатита В, при уровне 10–100 мМЕ/л вакцинация должна быть отложена на один год, при уровне более 100 мМЕ/л вакцинация показана через 5–7 лет.
Общие антитела к ядерному антигену гепатита В состоят из иммуноглобулинов класса М и G. Определение общих антител к ядерному антигену гепатита В может использоваться только для ретроспективной диагностики гепатита В, так как у 5–10 % больных исследования на HBsAg дают отрицательный результат. Для того чтобы установить, в какой стадии развития находится гепатит В, необходимо дополнительное определение антител IgM. Антитела класса IgM — маркер активной репликации вируса, т.е. острой инфекции, а антитела класса IgG — перенесенной инфекции.
Антитела IgM к ядерному антигену гепатита В (анти-HBcAg IgM) в сыворотке
Анти-HBcAg IgM в сыворотке в норме отсутствуют. Анти-HBcAg IgM обнаруживаются уже в начале острой фазы болезни, еще до появления или в первые дни желтухи, иногда даже в конце инкубации. Выявление анти-HBcAg IgM расценивают как убедительный критерий диагностики гепатита В, особенно при отрицательных результатах исследования на HBsAg. Анти-HBcAg IgM циркулируют в крови больных в течение нескольких месяцев (2–5 месяца) до периода реконвалесценции, а затем исчезают, что рассматривается как признак очищения организма от вируса гепатита В.
Установлено, что высокие концентрации HBeAg соответствуют высокой ДНК-полимеразной активности и характеризуют активную репликацию вируса. Наличие HBeAg в крови свидетельствует о высокой ее инфекциозности, т.е. присутствии в организме обследуемого активной инфекции гепатита В и обнаруживается только в случае присутствия в крови HBs-антигена. У больных хроническим активным гепатитом противовирусные препараты применяют только при обнаружении в крови HBeAg.
Наличие НВе-антигена свидетельствует о продолжающейся репликации вируса и инфекциозности больного. HBeAg-антиген — маркер острой фазы и репликации вируса гепатита В.
Анти-HBeAg в сыворотке в норме отсутствуют. Появление АHTH-HBeAg-антител указывает обычно на интенсивное выведение из организма вируса гепатита В и незначительное инфицирование больного. Эти антитела появляются в острый период и сохраняются до 5 лет после перенесенной инфекции. При хроническом персистирующем гепатите, анти-HBeAg обнаруживаются в крови больного вместе с HBsAg. Сероконверсия, т.е. переход HBeAg в анти-HBeAg при хроническом активном гепатите, чаще прогностически благоприятна, но такая же сероконверсия при выраженной цирротической трансформации печени прогноза не улучшает.
Гепатит С (ГС, hepatitis С) — вирусное заболевание, наиболее часто протекающее в виде посттрансфузионного гепатита с преобладанием безжелтушных и легких форм и склонное к хронизации процесса. Возбудитель — вирус гепатита С (ВГС) — имеет сходство с флавови-русами, содержит РНК.
Примерно 90% всех случаев посттрансфузионных гепатитов связаны с ВГС. Среди доноров антитела к вирусу гепатита С (анти-ВГС) обнаруживают в 0,2–5% случаев. У 40–75% пациентов регистрируется бессимптомная форма болезни, у 50–75% больных острым ВГС формируется хронический гепатит, у 20% из них развивается цирроз печени. Важная роль ВГС отводится и в этиологии гепатоклеточной карциномы.
Антитела к вирусу гепатита С в сыворотке
Антитела к вирусу гепатита С в сыворотке в норме отсутствуют. Диагностика гепатита С основана на обнаружении суммарных антител к ВГС методом ИФА, которые появляются в первые 2 нед заболевания и свидетельствуют о возможной инфицированности вирусом или перенесенной инфекции. Анти-ВГС-антитела могут сохраняться в крови реконвалесцентов на протяжении 8–10 лет с постепенным снижением их концентрации. Возможно позднее обнаружение антител спустя год и более после инфицирования.
При хроническом гепатите С, антитела определяются постоянно и в более высоких титрах. Существующие в настоящее время тест-системы для диагностики ВГС основаны на определении антител класса IgG, поэтому разрабатываются тест-системы нового поколения, которые позволят верифицировать активную инфекцию (определять антитела класса IgM). Антитела класса IgM могут выявляться не только при остром ВГС, но и при хроническом гепатите С. Снижение их уровня в процессе лечения больных хроническим гепатитом С может свидетельствовать об эффективности лекарственной терапии. Обнаружение антител к ВГС методом ИФА требует подтверждения способом иммуноблотинга для исключения ложно-положительного результата исследования.
Определение антител к вирусу гепатита С используют для диагностики острого и хронического гепатита С, персистирующего хронического гепатита. Вирус гепатита С может быть причиной развития цирроза и рака печени, поэтому данное исследование показано при этих заболеваниях.
Иммуноблотинг на антитела к белкам вируса гепатита С в сыворотке
Антитела к вирусу гепатита С в норме отсутствуют. Метод иммуноферментного анализа, применяемый для определения антител к ВГС, является скрининговым. В случае получения положительного результата для подтверждения его специфичности используют метод иммуноблотинга Western-blot — встречную преципитацию в геле антител в сыворотке крови больного с различными вирусными белками, подвергнутыми разделению по молекулярной массе с помощью электрофореза и нанесенными на нитроцеллюлозу. Исследование считается положительным, если выявляются антитела к белкам интенсивностью +1 к 2 или более антителам ВГС. Специфичными для ВГС являются антитела к белкам — Core, NS3-1, NS3-2, NS1, NS5.
Иммуноблотинг на вирус гепатита С служит подтверждающим тестом специфичности метода ИФА.
Вирусный гепатит D
Гепатит D — вирусная инфекция, протекающая вследствие биологических особенностей вируса исключительно в виде ко-или суперинфекции при гепатите В, характеризующаяся тяжелым течением часто с неблагоприятным исходом.
Возбудитель — вирус гепатита D (BГD) — по своим биологическим свойствам приближается к вироидам — обнаженным молекулам нуклеиновых кислот. Печень человека — единственное место репликации BГD. Известно существование двух вариантов инфекции: коинфекция (одновременное заражение ВГВ и BГD) и суперинфекция (заражение HBsAg-позитивных пациентов). Сочетание ВГВ и BГD сопровождается развитием более тяжелых форм патологического процесса, что определяется главным образом действием BГD. Летальность при суперинфекции достигает 5–20 %. Инфицирование дельта-вирусом может вызывать острое заболевание, заканчивающееся выздоровлением, или формировать хроническое носительство BГD.
При гепатите D могут отсутствовать в крови маркеры гепатита В — анти-НВс и HBs-антиген — и наблюдается угнетение ДНК-полимеразной активности, так как BГD ингибирует репликацию вируса гепатита В.
Антитела lgM к вирусу гепатита D в сыворотке
Антитела IgM к вирусу гепатита D в сыворотке в норме отсутствуют. Антитела BГD IgM (анти-BГD IgM) появляются в острый период «дельта-инфекции». По мере выздоровления при BГD происходит элиминация вируса из печени и исчезновение анти-BГD IgM. При хронизации процесса наблюдается персистирование BГD в ткани печени и анти-BГD IgM в высокой концентрации в крови. Антитела BГD IgM говорят об активной репликации вируса.
Антитела IgG к вирусу гепатита D в сыворотке
Антитела IgG к вирусу гепатита D в сыворотке в норме отсутствуют. Антитела BГD IgG (анти-BГD IgG) появляются в период реконвалесценции, и их концентрация постепенно снижается в течение нескольких месяцев. Определение антител BГD IgG может служить критерием ретроспективной диагностики гепатита ранее не уточненной этиологии.
Возбудителем вирусного гепатита Е (ВГЕ) является РНК-вирус. Для заболевания характерен фекально-оральный путь передачи, преимущественно водный. Инкубационный период болезни — около 35 сут. Клиническое течение острого ВГЕ сходно с ВГА. Существенно тяжелее заболевание протекает у беременных, особенно в III триместре.
Для специфической диагностики ВГЕ используются методы ИФА, основанные на выявлении антител класса IgM. Обнаружение в крови повышенного уровня анти-ВГЕ IgM служит лабораторным подтверждением диагноза.
ПЕРИОДЫ ОБНАРУЖЕНИЯ В КРОВИ МАРКЕРОВ ВИРУСНОГО ГЕПАТИТА В ПРИ ОСТРОМ ПРОЦЕССЕ:
1) поверхностный HBs-антиген — с инкубационного периода до периода ранней реконвалесценции (5,5–6 мес);
2) антиген НЬе обнаруживается в инкубационный и продромальный периоды (до 3,5 мес); его выявление свидетельствует о репликации вируса;
3) антитела к Hbe-антигену появляются в острый период заболевания (3–4-й месяц) и сохраняются до нескольких лет;
4) антитела класса IgM к ядерному антигену (анти-HBc-IgM) обнаруживаются в продромальном периоде и сохраняются до периода реконвалесценции (со 2-го по 6-й месяц заболевания);
5) антитела класса IgG к ядерному антигену (анти-HBc-IgG) возникают в продромальном периоде и сохраняются на протяжении всей жизни (ведущий маркер вирусного гепатита В);
6) антитела к поверхностному Hbs-антигену (анти-HBs) появляются в стадии поздней реконвалесценции (6-й месяц) и сохраняются до 5 лет.
Хронический гепатит С: клиника, диагностика, лечение
В настоящее время проблемой хронической HCV-инфекции интересуются как врачи-специалисты, так и люди, никак не связанные с медициной. От гепатита С во всем мире страдают по меньшей мере 200 млн человек.
В настоящее время проблемой хронической HCV-инфекции интересуются как врачи-специалисты, так и люди, никак не связанные с медициной.
От гепатита С во всем мире страдают по меньшей мере 200 млн человек. Последствиями перенесенного заболевания могут быть хронический гепатит, цирроз и первичный рак печени.
Эпидемиология
Распространенность хронической HCV-инфекции на земном шаре варьирует от 0,5 до 2%. Существуют регионы, для которых характерна более высокая распространенность этого заболевания: 6% в Заире и Саудовской Аравии, 16% в изолированных поселениях в Японии. В России наблюдается рост заболеваемости гепатитом С (3,2 на 100 тыс. населения в 1994 году и 19,3 в 1999 году). Источниками заражения вирусным гепатитом C служат больные острыми и хроническими формами HCV-инфекции, причем в основном это люди, у которых отсутствует желтуха и наблюдается бессимптомное или малосимптомное течение заболевания.
В настоящее время HCV чаще всего инфицируются молодые люди, преимущественно мужчины в возрасте около 20 лет, примерно 40% из них заражаются при внутривенном введении наркотиков. Основным путем инфицирования HCV является парентеральный. Так, у 6,1% больных, которым производилось переливание крови и ее компонентов во время кардиохирургических операций, развивался острый вирусный гепатит C, у 60% из них гепатит принимал хроническую форму.
Существует и риск заражения гепатитом C половым путем, однако он невелик (5-8%). Возможна передача HCV от матерей с острой или хронической формой инфекции; это также редкое явление, встречается не чаще чем в 5-6% случаев. Риск заражения вышеуказанными путями уступает таковому при гепатите В.
Приблизительно у половины больных путь инфицирования HCV установить не удается.
Вирус гепатита С
Вирус гепатита С относится к семейству флавивирусов. Геном вируса представлен однонитевой РНК протяженностью около 10 000 нуклеотидов. Вирус гепатита С вызывает заболевание только у человека. В экспериментальных условиях воспроизвести инфекцию можно у высших обезьян.
Популяция вируса неоднородна. Идентифицированы 6 генотипов (классификация по Simmonds), более 90 субтипов и множество вариантов вируса, обозначаемых как квазивиды. Зарегистрирована территориальная неравномерность циркуляции генотипов вируса гепатита С. В России чаще всего выявляются генотипы 1b и 3а этого вируса.
Определение генотипов вируса гепатита С имеет большое значение для практической медицины. Хотя до сих пор не установлено четкой корреляции между генотипами и уровнем виремии, характеристиками пациента, тяжестью течения заболевания, большинство исследователей соглашаются с выводами о значении генотипов вируса как важного фактора, влияющего на эффективность противовирусной терапии.
Вакцину против гепатита С создать пока не удалось из-за высокой изменчивости вируса гепатита С (ВГС).
Патогенез
Считают, что вирус оказывает прямое цитопатическое действие и вызывает иммуноопосредованное повреждение гепатоцитов. Высокая степень хронизации вирусного гепатита С обусловлена некоторыми особенностями действия вируса:
В течении хронической HCV-инфекции может происходить нейтрализация мажорного варианта вируса, но тогда генерируются минорные варианты. Квазивиды HCV представляют собой движущуюся мишень, которую ограничивает иммунная система хозяина. Появление нового мажорного квазивида сопровождается повышением виремии и увеличением титра Ig M антител к вирусным белкам. Постепенно и этот новый мажорный вариант заменяется. Такой процесс приводит к периодической волнообразной виремии, сопровождающейся обострением хронического гепатита С (ХГС) и повышением уровня антител.
Возможно, антивирусному Т-клеточному ответу отведена центральная роль в элиминации ВГC, так как нейтрализующие антитела, по-видимому, очень часто оказываются неэффективными. Т-хелперные (Th) лимфоциты распознают вирусные антигенные пептиды, представленные HLA-комплексом II класса на поверхностной мембране антиген-презентирующих клеток. В зависимости от типа цитокинового профиля Th-клетки делятся на две группы: Th1 и Th2. Первые продуцируют IFNg и IL2, стимулируя Т-клеточный ответ и цитотоксическую Т-лимфоцитную активность, а вторые продуцируют IL4 и IL10, стимулируя В-клеточный ответ. Таким образом, Тh-лимфоциты играют существенную роль в регуляции иммунного ответа. У пациентов, у которых болезнь перешла в хроническую стадию, в острой фазе вирус-специфический Th ответ был ниже и преобладали цитокины типа Th2.
У хронически ВГC-инфицированных пациентов значительно увеличено содержание вирусоспецифических Th2-клеток и их цитокинов. Нарушение баланса Th1/Th2 цитокиновой продукции может играть важную роль в иммунопатогенезе хронической ВГC-инфекции. Показано снижение уровня IFNg и IL12 при ХГС. Этот дефицит является следствием повышенного уровня IL10, предполагаемого отрицательного регулятора для IFNg. Повышенное содержание Th2-клеток при ХГС может снижаться при комбинированной терапии рибавирином и IFNa. Обнаружено, что у пациентов с клинико-биохимическим улучшением после лечения IFNa произошло увеличение уровня Th1-цитокинов.
Цитотоксические лимфоциты (CTL) играют, по-видимому, некоторую роль в ограничении репликации ВГС. Этот ответ недостаточен для полной элиминации вируса при хронической инфекции и, кроме того, может вызывать повреждение печени. Известно, что CTL способны быстро опознавать и направленно лизировать клетки, несущие ВГC-антигены, не провоцируя значительного воспаления, с помощью перфоринового, FasL- и TNFα-базируемых механизмов.
ТNF, как предполагается, индуцируют апоптоз клеток, опосредуя высвобождение свободных радикалов из митохондриальных электронно-транспортных путей и модуляцию синтеза некоторых белков. Взаимодействие нуклеокапсидного белка ВГC с внутрицитоплазматической частью рецептора TNFb, вероятно, представляет собой эволюционно-отобранный механизм, с помощью которого вирус препятствует преждевременному апоптозу клетки-хозяина. В отсутствие доступных модельных клеточных культур прямая цитопатичность вируса гепатита С не может быть исследована в полном объеме.
В подавляющем большинстве случаев острого гепатита С иммунной системе не удается элиминировать вирус. До сих пор нет ясного представления о том, почему это происходит. Очевидно, ВГС обладает эволюционно-закрепленными способностями, обеспечивающими ему персистенцию.
Однако иммунная система может оказывать существенное влияние на ВГC-инфекцию. В 15% случаев острого гепатита С она эффективно уничтожает вирус, а у хронически ВГC-инфицированных обеспечивает умеренное ограничение инфекции в течение почти 20 лет. Возможно, ослабление какого-либо звена антивирусных иммунных механизмов позволяет вирусу активно воздействовать на иммунную систему. Длительная ВГC-персистенция может привести к развитию В-клеточных лимфопролиферативных нарушений, таких, как смешанная криоглобулинемия, злокачественная не-Ходжкинская лимфома и появление органоспецифических и неспецифических аутоантител. Таким образом, хроническую ВГC-инфекцию следует рассматривать как мультисистемное заболевание.
Диагностика
Лабораторная диагностика гепатита С основана на выявлении специфических маркеров инфицирования ВГС (анти-ВГС-IgM/G, РНК ВГС) и должна проводиться разрешенными МЗ РФ к применению диагностическими препаратами отечественного или зарубежного производства в лабораториях, имеющих лицензию на проведение данного вида лабораторных исследований.
HCV RNA — самый ранний маркер репликации вируса, определяемый с помощью полимеразной цепной реакции (ПЦР) спустя несколько недель после заражения. Для выявления анти-ВГС применяют иммуноферментный анализ (ИФА). В настоящее время используют тест-системы третьего поколения ELISA-3. Подтверждающим методом является рекомбинантный иммуноблотинг (RIBA). У 60% больных анти-ВГС определяются в острой фазе, у 35% они появляются спустя 3-6 месяцев после инфицирования, у 5% инфицированных лиц анти-ВГС не определяются.
Болезнь может протекать бессимптомно. Наиболее распространенным симптомом является слабость. Целенаправленный опрос больных часто помогает выявить такие факторы риска, как переливание крови, внутривенное введение наркотиков, хронический гемодиализ и др. Кроме слабости больной может жаловаться на быструю утомляемость, тяжесть в правом подреберье, боли в правом верхнем квадранте живота, диспепсические явления.
Критериями постановки диагноза являются увеличение печени и селезенки, гиперферментемия и анти-ВГС в крови в течение не менее 6 месяцев.
Гепатоспленомегалия выявляется не более чем у 50% обратившихся за помощью больных, активность сывороточных трансаминаз редко превышает верхнюю границу нормы в 6 раз. Следует обратить внимание на то, что активность сывороточных трасаминаз не отражает степени изменений в печени: она может быть нормальной, несмотря на значительные морфологические изменения. Концентрация РНК ВГС в сыворотке имеет существенное значение для определения контагиозности и для мониторинга результатов лечения. При наличии в крови HCV-РНК биопсия печени, как правило, выявляет ряд изменений. Концентрация HCV-РНК в сыворотке, превышающая 105 молекулярных эквивалентов (копий) в 1 мл, наблюдается в активной фазе заболевания и совпадает с пиками активности трансаминаз.
Наличие или отсутствие РНК ВГС, как правило, не является диагностическим критерием хронического гепатита С и определяет фазу процесса (активный, неактивный).
Для раннего выявления ГЦК у больных циррозом печени, особенно у мужчин старше 40 лет, каждые 6 месяцев определяют уровень сывороточного α-фетопротеина и выполняют УЗИ печени.
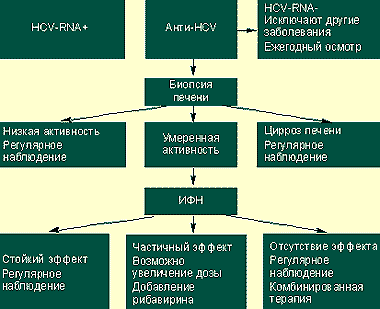 |
| Алгоритм ведения HCV-положительных больных |
Естественное течение и прогноз
Считается, что не более чем у 30% больных ВГС с минимальной морфологической активностью через 20 лет возможно развитие цирроза печени. Таким образом, больные, у которых при гистологическом исследовании биоптата печени выявляется наличие минимального воспаления и минимального фиброза, нуждаются в динамическом наблюдении.
Если персистенция РНК ВГС сохраняется более 6 месяцев, то спонтанное разрешение хронической HCV-инфекции маловероятно.
Клиническая картина
У большинства больных с хроническим гепатитом С заболевание протекает бессимптомно. Если жалобы существуют, то это чаще всего слабость, тупые боли в правом подреберье, тошнота, снижение аппетита, кожный зуд, артралгии и миалгии. Физикальный осмотр пациента помогает установить диагноз зачастую только на стадии цирроза печени.
Внепеченочные проявления HCV-инфекции
Ассоциация хронического гепатита С с различными внепеченочными проявлениями — хорошо известный врачам факт. Наиболее вероятным для большинства заболеваний и синдромов, наблюдаемых при HCV-инфекции, представляется иммунный патогенез, хотя конкретные механизмы во многом еще не выяснены. Доказанные и предполагаемые иммунные механизмы включают:
Частота иммуноопосредованных заболеваний и синдромов у больных хроническим гепатитом С достигает 23%. Наиболее характерны аутоиммунные проявления для больных с гаплотипом HLA DR4, который ассоциируется с внепеченочными проявлениями при аутоиммунном гепатите. Этот факт подтверждает гипотезу о триггерной роли вируса в инициации аутоиммунных процессов у генетически предрасположенного индивидуума.
Заболевания, ассоциированные с HCV-инфекцией
Ассоциированные с продукцией или отложением иммуноглобулинов:
Ассоциированные с неизвестным механизмом:
Выявление сывороточных аутоантител отражает наиболее частый феномен аутоиммунизации при HCV-инфекции, который диагностируют у 40-65% больных. Спектр аутоантител достаточно широк и включает ANA (до 28%), SMA (до 11%), анти-LKM-1 (до 7%), антифосфолипидные (до 25%), антитиреоидные (до 12,5%), ревматоидный фактор, анти-ASGP-R и др. Чаще всего титры этих антител не достигают диагностических значений, показательных для той или иной аутоиммунной патологии.
Анти-GOR являются антителами, специфичными для HCV-инфекции, и их выявляют не менее чем у 80% больных. Эпитоп, распознаваемый анти-GOR, локализуется на пока неидентифицированном ядерном белке, гиперэкспрессию которого наблюдают при гепатоцеллюлярной карциноме. Выработка анти-GOR ассоциирована только с HCV-инфекцией, но не с АИГ.
Аутоиммунные расстройства наблюдаются в среднем у 23% больных хроническим гепатитом С. Наиболее часто встречаются патология щитовидной железы.
Гистологическое исследование печени
Гистологическая картина не является патогномоничной, при этом достаточно часто выявляются характерные изменения. Отличительная особенность ее — лимфоидные агрегаты или фолликулы в портальных трактах, которые могут быть как изолированными, так и частью воспалительных изменений портальных трактов. По клеточному составу эти агрегаты напоминают первичные лимфоидные фолликулы в лимфатических узлах. Жировая дистрофия обнаруживается в 75% случаев. Кроме того, выявляются следующие характерные изменения: негнойный холангит с лимфоидной и плазмоклеточной инфильтрацией стенок протоков; лимфогистиоцитарная инфильтрация перипортальной зоны; слабовыраженные ступенчатые некрозы; мостовидные некрозы (обнаруживаются редко), пролиферация и активация сателлитных клеток печени, пролиферация эпителия желчных канальцев.
Отмечено, что индекс гистологической активности (ИГА) и индекс фиброза (ИФ) у больных хроническим гепатитом С с наличием жировой дистрофии достоверно выше, чем у пациентов без сопутствующей жировой дистрофии. У 93% больных с жировой дистрофией в гепатоцитах обнаруживался Core-протеин ВГС, при отсутствии жировой дистрофии — лишь у 39%. Этим фактом подчеркивается роль Core-протеина в развитии жировой дистрофии гепатоцитов.
Биопсия печени играет существенную роль в уточнении диагноза и оценке активности и стадии заболевания.
РНК ВГС можно определить в ткани печени методом ПЦР.
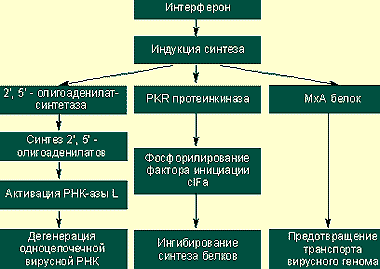 |
| Предотвращение вирусной транскрипции и трансляции |
Лечение
Основная цель лечения — предотвратить прогрессирование заболевания.
Режим отдыха, диета и прием витаминов не оказывают лечебного действия.
Отбор пациентов для лечения. Показанием к назначению терапии интерфероном служит умеренное (но не минимальное) либо тяжелое воспаление и/или фиброз. Решение о лечении пациентов с циррозом печени принимают индивидуально в каждом конкретном случае. Больные, у которых гистологическая активность минимальна, должны находиться под динамическим наблюдением, так как они имеют хороший жизненный прогноз без лечения и очень низкий риск развития цирроза печени через 10-20 лет.
Факторы, связанные с благоприятным эффектом противовирусной терапии при хронической HCV-инфекции:
Больным с нормальным уровнем АЛТ и положительным тестом на HCV RNA без результатов гистологического исследования противовирусное лечение проводить не рекомендуется.
Основной препарат, эффективность которого в лечении гепатита С доказана, — это интерферон альфа (ИФα).
В настоящее время принята оптимальная схема монотерапии ИФ: разовая доза составляет 3 млн МЕ, ее вводят подкожно или внутримышечно 3 раза в неделю в течение 3 месяцев. Через 3 месяца необходимо исследовать РНК ВГС. Если результаты ПЦР положительные схему лечения меняют. Если же РНК не выявляется, лечение продолжают до 12 месяцев. Стойкий положительный ответ в этом случае регистрируется у 15-20% больных.
Оптимальная схема лечения хронического гепатита С в настоящее время — это комбинация ИФa и рибавирина.
Согласно рекомендации согласительной конференции Европейской ассоциации по изучению печени (1999), больным с впервые установленным диагнозом «хронический гепатит С» и показаниями к лечению необходимо назначать ИФa в комбинации с рибавирином следующими курсами:
Стойкий положительный ответ при комбинированном лечении ИФa с рибавирином наблюдается в 40-60% случаев.
Суточная масса рибавирина составляет 1000-1200 мг в зависимости от массы тела.
В последние годы для повышения эффективности интерферона применяют пегилирование, которое заключается в присоединении к молекуле интерферона полиэтиленгликоля. В итоге образуется ПЭГ-интерферон, имеющий более длительный период полураспада. Предварительные данные свидетельствуют о большей эффективности такого лечения по сравнению с терапией интерфероном альфа.
Одним из наиболее перспективных пегилированных интерферонов является пегасис — ПЭГ-интерферон альфа-2а, соединенный с разветвленной молекулой полиэтиленгликоля, молекулярная масса которого составляет 40 kDa, общий вес молекулы — около 60 kDa. Особенности химической структуры данного препарата определяют его фармакокинетические свойства и клиническую эффективность. Молекула полиэтиленгликоля присоединена к альфа-интерферону посредством самой стабильной амидной связи, это делает молекулу пегасиса чрезвычайно устойчивой к действию петидаз и позволяет выпускать препарат в виде растворенной и готовой к употреблению лекарственной формы. Особенностью молекулы полиэтиленгликоля является способность активно связывать несколько молекул воды, что создает вокруг химически структурной единицы пегасиса эффект «водного облака», делая ее устойчивой во внутренней среде и сообщая препарату относительно небольшой объем распределения. Это, в свою очередь, способствует тому, что отпадает необходимость в коррекции дозы препарата в зависимости от массы тела пациента: пегасис вводится один раз в неделю в дозе 180 мкг. Существенными преимуществами препарата пегасис являются значительно лучшая переносимость и меньшая частота побочных реакций, ассоциированных с системным действием альфа-интерферона, что значительно улучшает качество жизни пациентов, получающих лечение по поводу хронического гепатита С. Кроме того, в отличие от других пегилированных интерферонов пегасис не требует существенной коррекции дозы в зависимости от функционального состояния почек, что делает препарат незаменимым у пациентов с сопутствующей хронической почечной недостаточностью.
Клиническая эффективность пегасиса оценена солидными широкомасштабными многоцентровыми рандомизированными исследованиями. Было показано, что частота доказанного ответа на лечение значительно превышает таковую по сравнению с «короткими» интерферонами как в схемах монотерапии, так и в сочетании с рибавирином. Особенно впечатляющими в этой связи являются результаты этиопатогенетической терапии с использованием пегасиса в сочетании с рибавирином у так называемой «трудной» категории пациентов, имеющих морфологические проявления цирроза печени, 1b-генотип вируса, высокую виремию: частота доказанного ответа на лечение у данной категории пациентов при использовании пегасиса в сочетании с рибавирином может составлять около 40%, у иных категорий пациентов этот показатель может превышать 75%, что ранее было практически немыслимым результатом.
Другие противовирусные препараты в лечении хронического гепатита С
Имеются данные, свидетельствующие о положительном действии таких препаратов, как ремантадин, урсодеоксихолевая кислота, пегилированные интерфероны, препараты глициризиновой кислоты, однако эта информация нуждается в дальнейшей проверке.
По вопросам литературы обращаться в редакцию