что такое протекающая вакцина
Такая корона: вакцина от COVID-19 может усугубить заболевание
Сразу в нескольких мировых лабораториях идет работа по созданию вакцины от COVID-19. Однако специалисты предупреждают: препарат должен быть тщательно протестирован перед применением, так как возможен синдром антитело-зависимого усиления инфекции. В этом случае прививка вызовет болезнь, а не предупредит ее возникновение. По мнению специалистов, проблему решит рекомбинантный, полученный с помощью генной инженерии, вариант препарата.
Время первых вакцин
Вопрос лечения и профилактики COVID-19 выходит на первый план для всей мировой фарминдустрии. В данное время в ведущих лабораториях разрабатывают различные варианты субстанций. Обсуждают схемы создания препаратов, в том числе, предложенные российскими специалистами.
Разработка вакцины — процесс трудоемкий и длительный, рассказала заведующая кафедрой инфекционных болезней с курсами эпидемиологии и фтизиатрии Медицинского института РУДН Галина Кожевникова.
— Поэтому в ближайшие месяцы, а может, и год одобренной эффективной и безопасной вакцины мы можем не увидеть. Помимо этого, не стоит забывать о изменчивости вируса, которая может встать на пути создания профилактических препаратов, — заявила эпидемиолог.
Более того, есть вероятность, что сама вакцина станет дополнительной биологической угрозой, сообщил директор Института медицинской паразитологии, тропических и трансмиссивных заболеваний им. Е.И. Марциновского Сеченовского университета Александр Лукашев.
— Сложность ее разработки связана с тем, что для коронавирусов возможен синдром антитело-зависимого усиления инфекции, то есть неправильно разработанный препарат может усугублять тяжесть болезни, — предупредил ученый.
— Ученые выяснили, что скопление антител к возбудителю лихорадки может усилить вирусную активность и спровоцировать развитие более тяжелой формы болезни — геморрагический синдром (скопление излитой из сосудов крови в кожных покровах и кровоточивость слизистых оболочек. — «Известия»), — пояснил эксперт
Антитело против тела
Суть феномена антитело-зависимого усиления инфекции (antibody-dependent enhancement, ADE) состоит в усилении процесса заражения в присутствии антител, специфических к возбудителю болезни. По идее, антитела должны купировать распространение уже известного организму патогена, но наблюдается обратный эффект.
Дело в том, что вирусы, особенно содержащие не ДНК, а РНК (к ним как раз принадлежит COVID-19), при самокопировании допускают большое количество ошибок. Это дает им возможность быстро мутировать, изменяясь при передаче от человека к человеку. Поэтому организм, который уже выработал антитела к инфицировавшему его коронавирусу и, возможно, перенесший бессимптомное заболевание, может не узнать вариант COVID-19, доставленный с помощью вакцины. А напротив, вызвать неразбериху в иммунной системе, которая закончится усилением инфекционного процесса еще до того, как концентрация антител достигнет порога, необходимого для нейтрализации вируса.
— Наличие антител к первому типу вируса при ADE не позволяет организму справиться со вторым типом, а наоборот, облегчает его проникновение в уязвимые клетки, — пояснил заведующий инфекционным отделением университетской клиники H-Clinic РУДН Данила Коннов. — Если такой феномен будет доказано характерен для нового коронавируса, то введение вакцины может спровоцировать ухудшение прогноза для заразившихся первоначальным штаммом. Эта теория возможна, но требует изучения и подтверждения.
Однако руководитель лаборатории геномной инженерии МФТИ Павел Волчков не видит большой проблемы даже при наличии данного синдрома, так как правильно сделанная вакцина должна вызывать не только гуморальный ответ (производство антител), но и запускать формирование пула клеток лимфоцитов, позволяющих избежать возможных побочных эффектов.
— Специалисты вполне способны создать вакцину от коронавируса, которая учтет наличие таких эффектов, как эффект антитело-зависимого усиления инфекции. Почему сейчас в целом в мире некоторые вакцины не очень эффективны? Потому что есть компании, которые учитывают экономические факторы и не хотят платить за новые R&D (research and development — исследования и разработки. — «Известия»). Поэтому до сих пор так мало современных рекомбинантных, а в большинстве случаев используются старые аттенуированные (живые) препараты. Тем не менее технологически мы полностью готовы разрабатывать новые, — уверен ученый.
По словам Павла Волчкова идеальная вакцина от COVID-19 должна быть рекомбинантной и доставляться в организм респираторным способом. То есть так же, как это делает сам коронавирус.
3 типа вакцин от COVID-19: в чем их особенности
По состоянию на конец 2020 года в мире разрабатывалось более 200 вакцин-кандидатов для иммунной профилактики COVID-19. Из них по меньшей мере 52 вакцины-кандидата проходили испытания на людях.
Почему так много вакцин находится в разработке?
Как правило, множество кандидатов на вакцину будет оценено перед тем, как смогут установить, что какая-либо из них является одновременно безопасной и эффективной. Например, из всех вакцин, которые изучаются в лаборатории и на лабораторных животных, примерно 7 из 100 будут соответствовать критериями, позволяющий им дойти до клинических испытаний на людях. Из вакцин, которые проходят клинические испытания, только каждая пятая оказывается успешной. Наличие большого числа вакцин в процессе разработки увеличивает шансы на то, что будет создана одна или несколько успешных вакцин, которые докажут свою безопасность и эффективность для предполагаемых приоритетных групп населения.
Разные типы вакцин
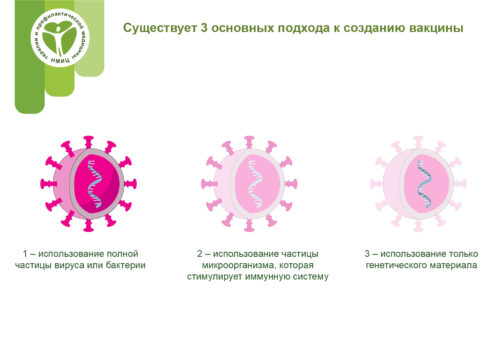
Существует три основных подхода к разработке вакцины. Их различия заключаются в том, используют ли они целый вирус или бактерию; только части микроба, которые запускают иммунную систему; или только генетический материал, который предоставляет инструкции для создания определенных белков, а не всего вируса.
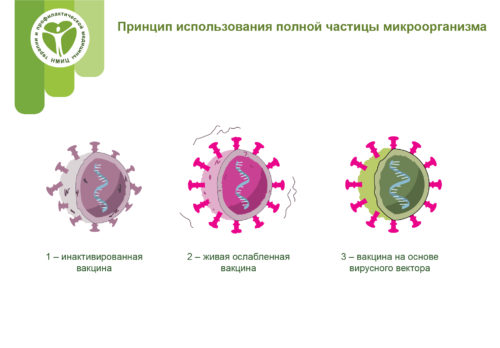
Принцип использования полной частицы микроорганизма
Инактивированные вакцины
Живые ослабленные вакцины
Живая ослабленная вакцина использует ослабленную живую вирусную частицу. Вакцина против кори, паротита и краснухи и вакцина против ветряной оспы и опоясывающего лишая являются примерами вакцины этого типа. Этот подход использует технологию, аналогичную инактивированной вакцине, и может быть изготовлен в больших масштабах. Однако подобные вакцины могут не подходить людям с ослабленной иммунной системой.
Векторные вакцины
Этот тип вакцины использует безопасный вирус для доставки определенных частиц (белков) интересующего микроорганизма, чтобы он мог вызвать иммунный ответ, не вызывая заболевания. Для этого «инструкции» по изготовлению определенных частей интересующего патогена вставляются в безопасный вирус. Затем безопасный вирус служит платформой или вектором для доставки белка в организм, а белок, в свою очередь, запускает иммунный ответ. Вакцина против Эболы является вакциной против вирусных переносчиков. Преимущество этого типа вакцин заключается в возможности быстрой разработки.
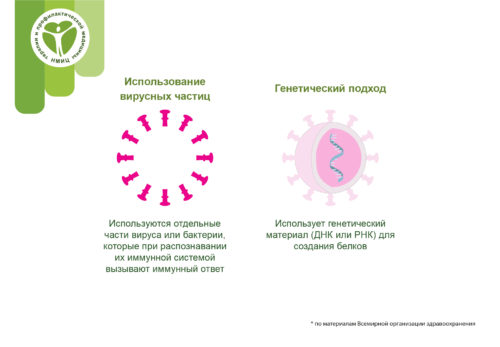
Подход использования вирусных частиц
Комментарий: используются отдельные части вируса или бактерии, которые при распознавании их иммунной системой вызывают иммунный ответ
Субъединичная вакцина – это вакцина, в которой используются только очень специфические части (субъединицы) вируса или бактерии, которые иммунная система должна распознать. Он не содержит всего микроба и не использует безопасный вирус в качестве переносчика. Субъединицами могут быть белки или сахара. Большинство вакцин в детском календаре вакцинации являются субъединичными вакцинами, защищающими людей от таких заболеваний, как коклюш, столбняк, дифтерия и менингококковый менингит.
Генетический подход (вакцина на основе нуклеиновых кислот)
В отличие от подходов к вакцинации, в которых используется ослабленный, убитый цельный микроорганизм или его части, вакцина на основе нуклеиновой кислоты использует участок генетического материала, который содержит инструкции для синтеза конкретных белков микроорганизма. ДНК и РНК являются «инструкциями», которые наши клетки используют для производства белков. В наших клетках ДНК сначала превращается в информационную РНК, которая затем используется в качестве основы для создания определенных белков.
Вакцина на основе нуклеиновых кислот доставляет нашим клеткам определенный набор инструкций в виде ДНК или матричной РНК, чтобы клетки вырабатывали определенный белок, на который должна отреагировать иммунная система. Подход с использованием нуклеиновых кислот является новым способом разработки вакцин. До пандемии COVID-19 ни одна из них еще не прошла полный процесс одобрения для использования на людях, хотя некоторые ДНК-вакцины, в том числе для конкретных видов рака, проходили испытания на людях. Из-за пандемии исследования в этой области продвигаются очень быстро, и некоторые вакцины против COVID-19 на основе матричной РНК получили разрешение на экстренное использование, что означает, что теперь их можно применять у людей вне клинических исследований.
Иммунитет после прививки от COVID-19: отвечаем на «острые» вопросы
Еще пару месяцев назад, коронавирусная «экспансия», казалось, пошла на убыль. Но с приходом нового индийского штамма, вопрос об иммунитете встал острее прежнего. Востребованность вакцинации возросла, а вместе с ней «выросло» и количество вопросов. Почему привитые болеют? Почему нет антител? Как долго держится иммунитет? И какой уровень антител «достаточный»?
Почему привитые болеют?
«Хайп» вокруг привитых заболевших многих заставил сомневаться в целесообразности прививки. А все потому, что вопреки ошибочному мнению, % эффективности вакцины – это количество привитых, избежавших полноценной, и особенно тяжелой, инфекции.
А не количество людей, защищенных от заражения как такового.
Таким образом, к примеру, эффективность «Спутника» в 91% говорит о том, что из 100 привитых, примерно 9 человек все же заболеют при контакте с вирусом, но в легкой форме. И есть данные исследований, что вакцинация и наличие антител существенно снижают риск тяжелого течения.
Остальные же привитые могут стать «временными» носителями, не имея при этом совершенно никаких симптомов. Поскольку иммунитет успевает «справиться» с вирусом еще до развития какого-либо воспаления.
Стратегия иммунизации (вакцинации) уже неоднократно доказала свою эффективность в «инфекционной истории» общества. Когда коллективный иммунитет помог «выдворить» вирус полиомиелита, кори и других опасных возбудителей.
Но достижение такого «уровня» в случае коронавируса, по мнению экспертов, требует вакцинации не менее 70% населения.
Почему по анализам нет антител?
Во-вторых, тест-система должна быть «настроена» на определение антител именно RBD-домена S-белка (или целиком к белку), отвечающего за прикрепление и внедрение вируса в клетку и входящего в состав всех имеющихся на сегодня вакцин. Ведь именно эти антитела отвечают за иммунитет от COVIDа.
В-третьих, некоторые вакцины, как «ЭпиВакКорона» центра «Вектор», требуют специализированных реагентов, разработанных экспертами того же центра. А анализ, проведенный на других тест-системах, ввиду некоторых особенностей вакцины, может не уловить антител.
Ну и, конечно же, стоит придерживаться рекомендуемых сроков «проверки». Когда первичный анализ можно сдать уже спустя 10-14 дней от первой прививки, с максимумом антител к 21 дню. Однако итоговую индивидуальную иммуногенность препарата рекомендуется оценивать не ранее 21 дня от второго введения вакцины.
Помимо прочего, не стоит забывать, что антительный механизм иммунитета – лишь один из путей защиты. При этом, уровень антител в норме со временем (примерно через 6 месяцев) снижается у каждого.
Выработанный же одномоментно с антительным, Т-клеточный иммунитет сохраняет «дееспособность» на месяцы и годы, потенциируя новый синтез антител при повторной встрече с возбудителем.
Так что, «антительный ноль» после прививки – еще не показатель полного отсутствия защиты. Однако ввиду отсутствия доступных тестов для массового определения Т-иммунитета. Точные причины ситуации рекомендуется выяснять с иммунологом.
Сколько антител «достаточно»?
На сегодняшний день таких данных не представил ни один из разработчиков вакцин.
Однако внутреннее исследование, проведенное компанией-разработчиком тест систем «Abbott», показало, что с вероятностью 95% для нейтрализации вируса достаточно уровня антител в 4000 AU/мл. А уровень в 2000 – обезвреживает вирус в 80% случаев.
Правда указанный эксперимент проводился в условиях In vitro (в «пробирке»). Так что каковы «достаточные цифры» в реальном организме – пока ответить сложно.
Как долго держатся антитела?
Точного ответа на этот вопрос также пока не существует, ввиду относительно короткого периода «поствакцинных» наблюдений, а также ряда индивидуальных особенностей иммунного реагирования.
По предварительным данным длительность защиты после «Спутника» должна составлять не менее 2-х лет, с высоким титром антител на протяжении не менее полугода.
А разработчики «ЭпиВакКороны» совместно с экспертами Роспотребнадзора заявляют о стойкости иммунитета не менее, чем на пол года после вакцинации.
При этом, не стоит забывать, что снижение антител через 6 месяцев после прививки – явление абсолютно естественное. И еще не говорит об отсутствии защиты.
Поэтому вопрос о ревакцинации, по мере снижения титра антител, должен решаться сугубо индивидуально. А общепринятых рекомендаций на этот счет на сегодняшний день не разработано.
Что такое вакцина
Знаете ли вы, что такое прививка?
Вакцинация (прививка) – это введение в организм человека медицинских иммунобиологических препаратов для создания специфической невосприимчивости к инфекционным болезням.
Предлагаем разобрать каждую часть этого определения, чтобы понять, что же такое вакцина и как она работает.
Часть 1. Медицинский иммунобиологический препарат
Все вакцины — это медицинские иммунобиологические препараты, т.к. они вводятся под контролем врача и содержат обработанные по специальной технологии возбудители заболеваний (биологические), против которых планируется создать иммунитет (иммуно-).
Кроме возбудителей или их частей-антигенов, вакцины иногда содержат специальные разрешенные консерванты для сохранения стерильности вакцины при хранении, а также минимальное допустимое количество тех средств, которые использовались для выращивания и инактивации микроорганизмов. Например, следовые количества дрожжевых клеток, используемых в производстве вакцин против гепатита В, или следовые количества белка куриных яиц, которые в основном используются для производства вакцин против гриппа.
Стерильность препаратов обеспечивают консерванты, рекомендованные Всемирной организацией здравоохранения и международными организациями по контролю безопасности лекарственных средств. Эти вещества разрешены для введения в организм человека.
Полный состав вакцин указан в инструкциях по их применению. Если у человека имеется установленная тяжелая аллергическая реакция на какой-то из компонентов конкретной вакцины, то обычно это является противопоказанием к её введению.
Часть 2. Введение в организм
Для введения вакцины в организм используются разные методы, их выбор определяется механизмом формирования защитного иммунитета, а способ введения указан в инструкции по применению.
Кликните на каждый из способов введения, чтобы больше о нем узнать.
Внутримышечный путь введения вакцин
Наиболее часто встречающийся путь для введения вакцин. Хорошее кровоснабжение мышц гарантирует и максимальную скорость выработки иммунитета, и максимальную его интенсивность, поскольку большее число иммунных клеток имеет возможность «познакомиться» с вакцинными антигенами. Удаленность мышц от кожного покрова обеспечивает меньшее число побочных реакций, которые в случае внутримышечного введения обычно сводятся лишь к некоторому дискомфорту при активных движениях в мышцах в течение 1-2 дней после вакцинации.
Место введения: Вводить вакцины в ягодичную область не рекомендуется. Во-первых, иглы шприц-доз многих вакцин недостаточно длинны для того, чтобы достичь ягодичной мышцы, в то время, как известно, и у детей, и у взрослых кожно-жировой слой может иметь значительную толщину. Если вакцина вводится в ягодичную область, то она, возможно, будет введена подкожно. Следует также помнить о том, что любая инъекция в ягодичную область сопровождается определенным риском повреждения седалищного нерва у людей с нетипичным его прохождением в мышцах.
Предпочтительным местом введения вакцин у детей первых лет является передне-боковая поверхность бедра в средней его трети. Это объясняется тем, что мышечная масса в этом месте значительна, при том, что подкожно-жировой слой развит слабее, чем в ягодичной области (особенно у детей, которые еще не ходят).
У детей старше двух лет и взрослых предпочтительным местом введения вакцин является дельтовидная мышца (мышечное утолщение в верхней части плеча, над головкой плечевой кости), в связи с небольшой толщиной кожного покрова и достаточной мышечной массой для введения 0,5-1,0 мл вакцинного препарата. У детей первого года жизни это место обычно не используется в связи с недостаточным развитием мышечной массы.
Техника вакцинации: Обычно внутримышечная инъекция проводится перпендикулярно, то есть под углом 90 градусов к поверхности кожи.
Преимущества: хорошее всасывание вакцины и, как следствие, высокая иммуногенность и скорость выработки иммунитета. Меньшее число местных побочных реакций.
Недостатки: Субъективное восприятие детьми младшего возраста внутримышечных инъекций несколько хуже, чем при других способах вакцинации.
Пероральный (т.е. через рот)
Классическим примером пероральной вакцины является ОПВ – живая полиомиелитная вакцина. Обычно таким образом вводятся живые вакцины, защищающие от кишечных инфекций (полиомиелит, брюшной тиф).
Техника пероральной вакцинации: несколько капель вакцины закапываются в рот. Если вакцина имеет неприятный вкус, ее могут закапывать либо на кусочек сахара, либо печенья.
Преимущества такого пути введения вакцины очевидны: нет укола, простота метода, его быстрота.
Недостатками Недостатками перорального введения вакцин можно считать разлив вакцины, неточность дозировки вакцины (часть препарата может выводиться с калом, не сработав).
Внутрикожный и накожный
Классическим примером вакцины, предназначенной для внутрикожного введения, является БЦЖ. Примерами вакцин с внутрикожным введением также являются живая туляремийная вакцина и вакцина против натуральной оспы. Как правило, внутрикожно вводятся живые бактериальные вакцины, распространение микробов из которых по всему организму крайне нежелательно.
Техника: Традиционным местом для накожного введения вакцин является либо плечо (над дельтовидной мышцей), либо предплечье – середина между запястьем и локтевым сгибом. Для внутрикожного введения должны использоваться специальные шприцы со специальными, тонкими иглами. Иголочку вводят вверх срезом, практически параллельно поверхности кожи, оттягивая кожу вверх. При этом необходимо убедиться, что игла не проникла под кожу. О правильности введения будет свидетельствовать образование специфической «лимонной корочки» в месте введения – белесый оттенок кожи с характерными углублениями на месте выхода протоков кожных желез. Если «лимонная корочка» не образуется во время введения, значит вакцина вводится неверно.
Преимущества: Низкая антигенная нагрузка, относительная безболезненность.
Недостатки: Довольно сложная техника вакцинации, требующая специальной подготовки. Возможность неправильно ввести вакцину, что может привести к поствакцинальным осложнениям.
Подкожный путь введения вакцин
Довольно традиционный путь введения вакцин и других иммунобиологических препаратов на территории бывшего СССР, хорошо известный всем уколами «под лопатку». В целом этот путь подходит для живых и инактивированных вакцин, хотя предпочтительно использовать его именно для живых (корь-паротит-краснуха, желтая лихорадка и др.).
В связи с тем, что при подкожном введении может несколько снижаться иммуногенность и скорость выработки иммунного ответа, этот путь введения крайне нежелателен для введения вакцин против бешенства и вирусного гепатита В.
Подкожный путь введения вакцин желателен для пациентов с нарушениями свертывания крови – риск кровотечений у таких пациентов после подкожной инъекции значительно ниже, чем при внутримышечном введении.
Техника: Местом вакцинации могут быть как плечо (боковая поверхность середины между плечевым и локтевым суставами), так и передне-боковая поверхность средней трети бедра. Указательным и большим пальцами кожа берется в складку и, под небольшим углом, игла вводится под кожу. Если подкожный слой у пациента выражен значительно, формирование складки не критично.
Преимущества: Сравнительная простота техники, незначительно меньшая болезненность (что несущественно у детей) по сравнению с внутримышечной инъекцией. В отличие от внутрикожного введения, можно ввести больший объем вакцины или другого иммунобиологического препарата. Точность введенной дозы (по сравнению с внутрикожным и пероральным способом введения).
Недостатки: «Депонирование» вакцины и как следствие — меньшая скорость выработки иммунитета и его интенсивность при введении инактивированных вакцин. Большее число местных реакций — покраснений и уплотнений в месте введения.
Аэрозольный, интраназальный (т.е. через нос)
Считается, что подобный путь введения вакцин улучшает иммунитет во входных воротах воздушно-капельных инфекций (например, при гриппе) за счет создания иммунологического барьера на слизистых оболочках. В то же время, созданный таким образом иммунитет не является стойким, и в то же время общий (т.н. системный) иммунитет может оказаться недостаточным для борьбы с бактериями и вирусами, уже проникшими в организм через барьер на слизистых оболочках.
Техника аэрозольной вакцинации: несколько капель вакцины закапывают в нос либо распыляют в носовых ходах с помощью специального устройства.
Преимущества такого пути введения вакцины очевидны: как и для пероральной вакцинации, для аэрозольного введения не требуется укола; такая вакцинация создает отличный иммунитет на слизистых оболочках верхних дыхательных путей.
Недостатками интраназального введения вакцин можно считать существенный разлив вакцины, потери вакцины (часть препарата попадает в желудок).
Часть 3. Специфическая невосприимчивость
Вакцины защищают только от тех заболеваний, против которых они предназначены, в этом заключается специфика иммунитета. Возбудителей же инфекционных заболеваний множество: они делятся на различные типы и подтипы, для защиты от многих из них уже созданы или создаются специфичные вакцины с разными возможными спектрами защиты.
Так, например, современные вакцины против пневмококка (одного из возбудителей менингита и пневмонии) могут содержать по 10, 13 или 23 штамма. И хотя ученым известно около 100 подтипов пневмококка, вакцины включают самые часто встречающиеся у детей и взрослых, например, самый широкий на сегодня спектр защиты — из 23 серотипов.
Однако нужно иметь в виду, что привитой человек имеет вероятность встретиться с каким-то редким подтипом микроорганизма, который не входит в вакцину и может вызвать заболевание, так как вакцина не формирует защиту против этого редко встречающегося микроорганизма, не входящего в её состав.
Означает ли это, что прививка не нужна, раз не может защитить от всех болезней? НЕТ! Вакцина дает хорошую защиту от наиболее распространенных и опасных из них.
Календарь прививок, подскажет вам, против каких инфекций необходима вакцинация. А мобильное приложение «Беби-Гид» поможет не забыть о сроках детских прививок.
Вакцина от коронавируса COVID-19: принцип работы, эффективность, противопоказания
Вакцина – единственный надежный способ избежать заражения или осложненного течения заболевания. Вакцинацию применяют против множества инфекций, а с недавних пор – и против коронавируса COVID-19. Даже если привитый человек заболеет, вероятность развития осложнений и тяжелого течения заболевания будет практически равна нулю.
Что нужно знать перед вакцинацией от коронавируса
Все существующие на данный момент вакцины от ковида – двухфазные, то есть для максимальной защиты требуется введение второй дозы. Такая тактика в медицине существует многие десятилетия. Введение повторной дозы, называемой «бустерной» (англ. booster, от boost — поднимать, повышать, усиливать), позволяет сформировать более выраженный иммунный ответ и сохранить защиту от инфекции на длительный период времени.
Однако некоторые страны решили отложить вакцинацию второй дозой, чтобы привить как можно больше людей. Что будет, если не пройти второй этап вакцинации? Насколько эффективна такая тактика?
Чтобы ответить на эти вопросы, мы расскажем, как именно работают вакцины от коронавируса, и что заставляет наш иммунитет сопротивляться вирусу.
Как работает вакцина от ковида?
Вторая – бустерная – доза вакцины запускает вторую часть иммунного ответа, в результате чего организм вырабатывает больше Т-клеток и формирует долгосрочную иммунную память. Этот процесс также «тренирует» В-клетки быстрее реагировать на вирусное вторжение, скорее делиться и вырабатывать более эффективные антитела.
Результаты крупных медицинских исследований всех имеющихся на сегодняшний день вакцин от COVID-19, показывают, что вторая доза увеличивает степень защиты в несколько раз. Израильские ученые пришли к выводу, что уровень антител у пациентов, получивших обе дозы вакцины от коронавируса, в 6-12 раз выше, чем у тех, кто привился разово. Как мы видим, второй этап вакцинации принципиально важен для надежной защиты.
Что будет, если получить только одну дозу?
На сегодняшний день нет обширных исследований, которые предоставили бы точные цифры об эффективности разовой вакцинации от COVID-19. Пока неизвестно, насколько долгим будет иммунитет от одной дозы вакцины. Также надо понимать, что любой вакцине требуется время, чтобы она начала действовать.
По данным исследования Pfizer, в течение двух недель после первой инъекции защита формировалась в 52% случаев. Для истинной оценки иммунитета после одной вакцины этих данных недостаточно. Также пока неизвестно, насколько долго эта защита остается эффективной.
Как себя вести после первой прививки от коронавируса?
На этот счет ученые дают четкую инструкцию: после первой дозы вакцины придется соблюдать все меры предосторожности – то есть вести себя так, как будто не прививались. Это необходимые меры, потому что, во-первых, нет надежных доказательств, что одна доза обладает достаточным воздействием на иммунную систему, а во-вторых, даже полная вакцинация не может на 100% предотвратить заражение и передачу вируса.
Эффективность вакцин главным образом оценивается по их способности предотвращать тяжелые симптомы. А как мы знаем, ковид может протекать бессимптомно, при этом человек заразен и опасен для окружающих.
Я привился – значит, защищен?
К сожалению, ни одна вакцина не может дать стопроцентной гарантии от заражения, хотя и существенно снижает риски. Грамотная вакцинация (с соблюдением нужного интервала между дозами) способна натренировать иммунную систему реагировать на вирус должным образом. Поэтому, даже если заражение все же произойдет, болезнь пройдет в значительно более легкой форме, а вероятнее всего – бессимптомно.
Однако нельзя забывать, что бессимптомные пациенты могут быть переносчиками инфекции. Поэтому, чтобы защитить непривитых окружающих вас людей, необходимо продолжать соблюдать социальное дистанцирование и носить маски даже после вакцинации.
Чтобы вакцина сработала, иммунитет должен правильным образом на нее среагировать – дать адекватный иммунный ответ.
Кому противопоказана прививка?
При любой вакцинации необходимо взвешивать потенциальные риски и пользу. Вакцина от ковида с осторожностью применяется при хронических заболеваниях печени, почек, сердечно-сосудистой системы, эндокринных нарушениях, эпилепсии и заболеваниях ЦНС. При наличии любого хронического заболевания решение о вакцинировании принимается индивидуально, после консультации с лечащим врачом.
Недавно список противопоказаний дополнили аутоиммунные и онкологические заболевания в анамнезе. Влияние вакцины на течение онкологического заболевания на данный момент до конца не изучено. Риски связаны с тем, что иммунная система онкологических больных ослаблена и разбалансирована, вторжение вакцины может в теории запустить нежелательные процессы. Если пациент находится на этапе устойчивой ремиссии, он может обсудить вакцинацию со своим ведущим онкологом.
Абсолютными противопоказаниями для вакцинации от коронавируса остаются возраст до 18 лет, беременность и период лактации, индивидуальная непереносимость компонентов вакцины, обострение хронических заболеваний, острые инфекционные заболевания.
Вакцина предназначена для людей, не перенесших заболевание, вызванное коронавирусом. В рекомендациях Минздрава отсутствует требование проводить предварительное исследование на наличие иммуноглобулинов IgG и IgM. Однако это единственный способ узнать, переболел ли человек.
Среди обязательных этапов подготовки к вакцинации – измерение температуры и общий осмотр у врача. Если в течение последних 14 дней был контакт с инфицированным коронавирусом, или если у пациента были симптомы COVID-19 или ОРВИ (кашель, температура, общее недомогание), необходимо перед прививкой сдать ПЦР-тест на ковид.