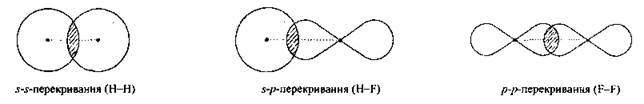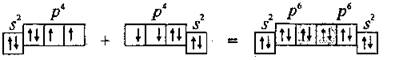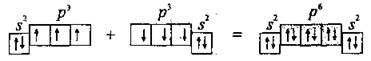что такое пи связь что такое сигма связь
Что такое пи связь что такое сигма связь
РАЗДЕЛ И. ОБЩАЯ ХИМИЯ
В образовании σ-связи могут принимать участие как обычные, так и гібридизовані орбитали.
Два неспаренные р-электроны в атоме Кислорода могут образовать две совместные ковалентные пары с электронами второго атома Кислорода:
Одна пара идет на образование σ-связи:
которые размещаются в плоскости, которая является перпендикулярной к оси соединения атомов Карбона:
В результате образования трех общих электронных пар N≡N каждый атом Азота приобретает устойчивую электронную конфигурацию инертного элемента 2 s 2 2 p 6 (октет электронов).
С помощью π-связи формируется молекула бензену и других аренов. Длина связи (ароматического, «полуторного», сказывается 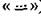
1 Под длиной связи понимают расстояние между центрами ядер атомов Углерода, участвующих в связи.
Метод валентных связей. Гибридизация атомных орбиталей
Метод валентных связей
Метод валентных связей (локализованных электронных пар) предполагает, что каждая пара атомов в молекуле удерживается вместе при помощи одной или нескольких общих электронных пар.
Поэтому химическая связь представляется двухэлектронной и двухцентровой, т.е. локализована между двумя атомами. В структурных формулах соединений обозначается черточкой:
Рассмотрим в свете Метода ВС, такие особенности связи, как насыщаемость, направленность и поляризуемость.
Образование сигма-, пи- и дельта-связей
Валентность атома — определяется числом неспаренных (валентных) электронов, способных принять участие в образовании химической связи.
Валентность выражается небольшими целыми числами и равна числу ковалентных связей. Валентность элементов, проявляющуюся в ковалентных соединениях, часто называют ковалентностью.
Некоторые атомы имеют переменную валентность, например углерод в основном состоянии имеет 2 неспаренных электрона и будет двух валентен. При возбуждении атома, возможно распарить другие два спаренных электрона и тогда атом углерода станет четырех валентен:
Возбуждение атома до нового валентного состояния требует затраты энергии, которая компенсируется выделяемой при образовании связей энергией.
Взаимное перекрывание облаков, т.е. образование связи может происходить разными способами, ввиду их различной формы. Различают σ-, π- и δ-связи.
Как различить сигма-, пи- и дельта-связи?
Сигма – связи образуются при перекрывании облаков вдоль линии, проходящей через ядра атомов.
Пи – связи возникают при перекрывании облаков по обе стороны от линии, соединяющей ядра атомов.
Дельта – связи осуществляются при перекрывании всех четырех лопастей d – электронных облаков, расположенных в параллельных плоскостях.
σ– связь может возникнуть при перекрывании вдоль линии, соединяющей ядра атомов в следующих орбиталей:
σ– связь обладает свойствами локализованной двухцентровой связи, каковой она и является.
π– связь может образовываться при перекрывании по обе стороны от линии, соединяющей ядра атомов следующих орбиталей:
Итак, s— элементы способны к образованию только σ– связи,
р— элементы — σ– и π– связи,
d— элементы — σ–, π– и δ‑ связи,
При совместном образовании π– и σ- связей получается двойная связь.
Если же одновременно возникают две π–и σ- связь, то образуется тройная связь.
Количество возникших связей между атомами, называется кратностью связи.
Между двумя атомами может возникнуть только одна сигма-связь.
Направленность ковалентной связи
Гибридизация атомных орбиталей
Рассмотрим пример. Представим, что четыре атома водорода соединились с атомом углерода и образовалась молекула метана CH4.
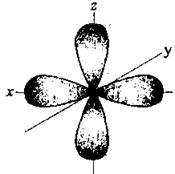
Рисунок показывает что происходит, но не объясняет, как ведут себя s- и р— орбитали, при образовании таких соединений.
Хотя р— орбиталь имеет две части, развернутые друг относительно друга, но она может образовывать только одну связь. В итоге, можно предположить, что в молекуле метана один атом водорода присоединяется к 2s- орбитали углерода, остальные – к 2р— орбитали.
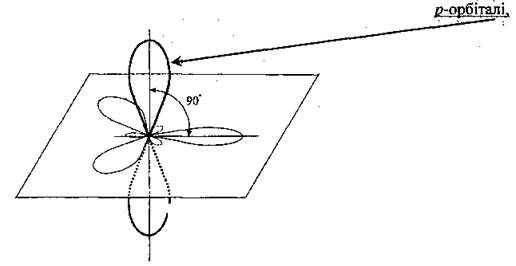
Тогда, каждый атом водорода будет находиться по отношению к другому под углом 90°, но это не так. Электроны отталкиваются друг от друга и расходятся на большее расстояние.
Что же на самом деле происходит?
Происходит гибридизация атомных орбиталей, в результате которой все орбитали объединяются, перестраиваются и образуют 4 эквивалентные гибридные орбитали, которые направлены к вершинам тетраэдра.
Типы гибридизации атомных орбиталей
В нашем примере, каждая из гибридных орбиталей содержит некий вклад 2s- орбитали и некоторые вклады 2р— орбиталей.
Как видно из рисунка, конфигурация гибридных орбиталей позволяет четырем атомам вдорода образовать ковалентные связи с атомом углерода, при этом орбитали будут располагаться относительно друг друга под углом 109,5°.
В молекуле H2O неподеленными электронными парами заняты две гибридные орбитали атома кислорода, а две другие используются для связывания с атомами водорода.
Число гибридных орбиталей определяется числом одинарных связей, а также количеством неподеленных электронных пар в молекуле. Эти электроны находятся на гибридных орбиталях. Когда же происходит перекрывание негибридных орбиталей двух атомов, то образуется кратная связь. Например, в молекуле этилена связь реализуется следующим образом:
Орбитали будут располагаться относительно друг друга под углом 120°.
sp-гибридизация
Таким же образом, в молекуле ацетилена образуется тройная связь. В данном случае происходит sp-гибридизация атомов, т.е. гибридные орбитали образованы одной 2s- и одной 2р— орбиталями, а другие две 2р— орбитали являются негибридными.
Орбитали располагаются относительно друг друга под углом 180°
Гибридные орбитали в пространстве располагаются различным образом:
Сигма (s) и пи (p)-связи



Метод валентных связей
Представления о механизме образования химической связи на примере молекулы водорода распространяются и на другие молекулы. Теория химической связи, созданная на этой основе, получила название метода валентных связей (МВС).
Основные положения:
1) ковалентная связь образуется в результате перекрывания двух электронных облаков с противоположно направленными спинами, причем образованное общее электронное облако принадлежит двум атомам;
2) ковалентная связь тем прочнее, чем в большей степени перекрываются взаимодействующие электронные облака. Степень перекрывания электронных облаков зависит от их размеров и плотности;
3) образование молекулы сопровождается сжатием электронных облаков и уменьшением размеров молекулы по сравнению с размерами атомов;
4) в образовании связи принимают участие s- и p-электроны внешнего энергетического уровня и d-электроны предвнешнего энергетического уровня.
Схема образования химической связи в молекулах хлора Cl2 (а) и хлороводорода HCl (б)
Химическая связь, для которой линия, соединяющая атомные ядра, является осью симметрии связывающего электронного облака, называется сигма (σ)-связью. Она возникает при «лобовом» перекрывании атомных орбиталей. Связи при перекрывании s-s-орбиталей в молекуле Н2; р-р-орбиталей в молекуле Cl2 и s-p-орбиталей в молекуле НСl являются сигма связями. Возможно «боковое» перекрывание атомных орбиталей. При перекрывании р-электронных облаков, ориентированных перпендикулярно оси связи, т.е. по оси у- и z-осям, образуются две области перекрывания, расположенные по обе стороны от этой оси.
Такая ковалентная связь называется пи (p)-связью. Перекрывание электронных облаков при образовании π-связи меньше. Кроме того, области перекрывания лежат дальше от ядер, чем при образовании σ-связи. Вследствие этих причин π-связь обладает меньшей прочностью по сравнению с σ-связью. Поэтому энергия двойной связи меньше удвоенной энергии одинарной связи, которая всегда является σ-связью. Кроме того, σ-связь имеет осевую, цилиндрическую симметрию и представляет собой тело вращения вокруг линии, соединяющей атомные ядра. π-Связь, наоборот, не обладает цилиндрической симметрией.
Одинарная связь всегда является чистой или гибридной σ-связью. Двойная же связь состоит из одной σ- и одной π-связей, расположенных перпендикулярно друг относительно друга. σ-Связь прочнее π-связи. В соединениях с кратными связями обязательно присутствует одна σ-связь и одна или две π-связи.
Одиночные и кратные связи. Сигма- и пи- связи.
Одиночная связь – ковалентная связь, при которой между двумя атомами образуется только одна общая электронная пара.
Сигма-связь – ковалентная связь, при образовании которой область перекрывания электронных облаков находится на линии, соединяющей ядра атомов. Одинарные связи всегда являются сигма-связями.
Пи-связь – ковалентная связь, при образовании которой область перекрывания электронных облаков находится по обе стороны от линии, соединяющей ядра. Образуются в тех случаях, когда между двумя атомами возникают две или три общие электронные пары. Число общих электронных пар между связанными атомами характеризует кратность связи.
Если связь между двумя атомами образована двумя общими электронными парами, то такая связь называется двойной связью. Любая двойная связь состоит из одной сигма-связи и одной пи-связи.
Если связь между двумя атомами образована тремя общими электронными парами, то такая связь называется тройной связью. Любая тройная связь состоит из одной сигма-связи и двух пи-связей.
Двойные и тройные связи имеют общее название: кратные связи.
Основные типы структур неорганических соединений. Вещества с молекулярной и
немолекулярной структурой. Атомные, молекулярные, ионные и металлические
кристаллические решетки.
| Тип | молекулярная | ионная | атомная | металлическая |
| В узлах | молекулы | Положительно и отрицательно заряженные ионы (катионы и анионы) | Атомы | Атомы и положительно заряженные ионы металлов |
| Хар-тер связи | Силы межмолекулярного взаимодействия ( в т.ч. водородные связи) | Электростатические ионные связи | Ковалентные связи | Металлическая связь между ионами металлов и свободными электронами. |
| Прочн | Слабая | Прочная | Очень прочная | Разной прочности |
| Отл. Физ. Св-ва | Легкоплавкие, небольшой твердости, многие растворимы в воде. | Тугоплавкие, твердые, многие растворимы в воде, растворы и расплавы проводят электрический ток (проводники 2 рода) | Очень тугоплавкие, очень твердые, практически нерасворимы в воде | Разнообразны по свойствам: имеют блеск, обладают электропроводностью (проводники 1 рода) и теплопроводностью. |
| прим | Йод, лёд, «сухой лед». | NaCl, KOH, Ba(NO3)2 | Алмаз, кремний | Медь, калий, цинк. |
Молекулярные и немолекулярные вещества — один из признаков химических веществ относительно их строения.
Молекулярные вещества — это вещества, мельчайшими структурными частицами которых являются молекулы
Молекулы — наименьшая частица молекулярного вещества, способная существовать самостоятельно и сохраняющая его химические свойства. Молекулярные вещества имеют низкие температуры плавления и кипения и находятся в стандартных условиях в твердом, жидком или газообразном состоянии.
Немолекулярные вещества — это вещества, мельчайшими структурными частицами которых являются атомы или ионы.
Ион — это атом или группа атомов, обладающих положительным или отрицательным зарядом.
Немолекулярные вещества находятся в стандартных условиях в твердом агрегатном состоянии и имеют высокие температуры плавления и кипения.
Существуют вещества с молекулярным и немолекулярным строением. Молекулярное строение имеют все газы, все жидкости. Твердые вещества могут иметь молекулярное и немолекулярное строение. Молекулярное строение имеют летущие твердые вещества (лед, иод, белый фосфор, органические вещества). В узлах кристаллической решетки легколетучих твердых веществ находятся молекулы. Большинство неорганических твердых веществ имеют немолекулярное строение, в узлах решеток находятся ионы (соли, основания) или атомы (металлы, алмаз, кремний). Вещества с молекулярным строением составляют более 95% от всех известных веществ, так как органические вещества имеют молекулярное строение, а органических веществ известно гораздо больше, чем неорганических.
Химические реакции. Классификация химических реакций. Основные задачи химической кинетики и химической термодинамики.
Химические реакции–это явления, при которых происходит превращение одних веществ в другие.
Признаки химических реакций:
Na2CO3+2HCl=2NaCl+H2O+CO2
ü Выпадение или растворение осадка
BaCl2+H2SO4=BaSO4 
ü Появление запаха.
ü Излучение света и тепла
Для протекания химических реакций необходимы условия: соприкосновения реагирующих веществ, нагревание, освещение.
Классификации химических реакций:
I. По числу и составу исходных реагентов:
a) Реакция соединения – реакция, при которой из нескольких веществ образуется одно вещество, более сложное, чем исходные: А+В=АВ
b) Реакция разложения – реакция, при которой из одного сложного вещества образуется несколько веществ. Конечными продуктами могут быть как простые, так и сложные вещества: АВ=А+В
c) Реакция замещения – реакция, при которых атомы адного элемента замещают атомы другого элемента в сложном веществе и при этом образуются два новых – простое и сложное: Х+АВ=АХ+В
d) Реакция обмена – реакция, при которой реагирующие вещества обмениваются своими составными частями, в результате чего из двух сложных веществ образуются два новых сложных вещества: АВ+СХ=АХ+СВ
II. По знаку теплового эффекта реакции делятся на:
a) эндотермические — реакции, протекающие с поглощением тепла
b) экзотермические— реакции, в результате которых тепло выделяется.
III. С учетом явления катализа:
a) каталитическими (протекающие с участием катализатора)
IV. По признаку обратимости реакции делят на:
a) обратимые – протекающие одновременно в пярмом и обратном направлении
b) необратимые – протекающие толкьов одном направлении
V. По признаку изменений степеней окисления элементов в молекулах реагирующих веществ:
a) ОВР – реакции с переносом электронов
b) Не ОВР – реакции без переноса электронов.
VI. По признаку однородности реакционной системы:
a) Гомогенные – протекающие в однородной системе
b) Гетерогенные – протекающие в неоднородной системе
Пи-связь
Пи-связь (π-связь) — ковалентная связь, образующаяся перекрыванием p-атомных орбиталей. В отличие от сигма-связи, осуществляемой перекрыванием s-атомных орбиталей вдоль линии соединения атомов, пи-связи, возникают при перекрывании p-атомных орбиталей по обе стороны от линии соединения атомов. Считается, что пи-связь реализуется в кратных связях — двойная связь состоит из одной сигма- и одной пи-связи, тройная — из одной сигма- и двух ортогональных пи-связей. [1]
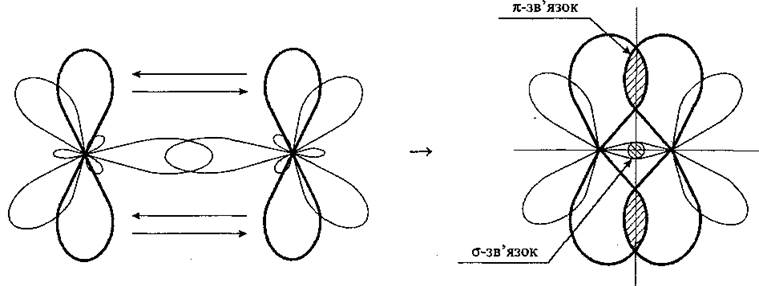
В случае образования двойной связи, сигма-связи образованы sp 2 гибридизированными орбиталями. Общее количество таких связей у атома углерода три и они расположены в одной плоскости. Угол между связями 120 °. Пи-связь располагается перпендикулярно указанной плоскости (рис.1).
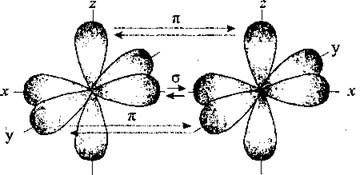
В случае образования тройной связи, сигма-связи образованы sp-гибридизрованными орбиталями. Общее количество таких связей у атома углерода две и они находятся под углом 180° друг к другу. Две пи-связи тройной связи взаимно перпендикулярны (рис.2).
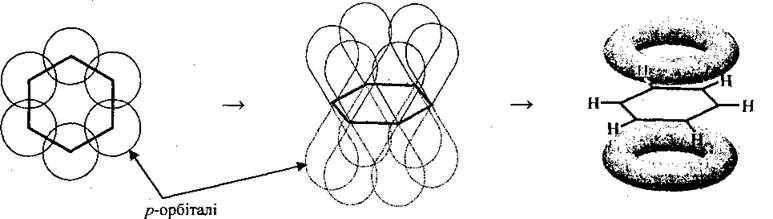
В случае образования ароматической системы, например, бензола C6H6, каждый из шести атомов углерода находится в состоянии sp 2 — гибридизации и образует три сигма-связи с валентными углами 120 °. Четвёртый p-электрон каждого атома углерода ориентируется перпендикулярно к плоскости бензольного кольца (рис.3.). В целом возникает единая связь, распространяющаяся на все атомы углерода бензольного кольц. Образуются две области пи-связей большой электронной плотности по обе стороны от плоскости сигма-связей. При такой связи все атомы углерода в молекуле бензола становятся равноценными и, следовательно, подобная система более устойчива, чем система с тремя локализованными двойными связями. Нелокализованная пи-связь в молекуле бензола обусловливает повышение порядка связи между атомами углерода и уменьшение межъядерного расстояния, то есть длина химической связи dcc в молекуле бензола составляет 1,39 Å, тогда как dC-C = 1,543 Å, а dC=C = 1,353 Å. [3]
Концепция Л.Полинга сигма- и пи-связей вошла составной частью в теорию валентных связей. В настоящее время разработаны анимированные изображения гибридизации атомных орбиталей.