Что такое холодовая проба в медицине
Холодовой тест Дункана
Холодовая аллергия (ХА) или крапивница – неиммунологическая форма аллергии, проявляется у 0,05% жителей европейских стран. Специалисты наблюдают как острые варианты развития (реже), так и хронические с рецидивами при каждом взаимодействии с холодом. Проявления могут возникнуть при внешних воздействиях (мороз, сильный ветер, холодная вода) и внутренних (холодная еда, питье, охлажденные инъекции, применение криопреципитатов).
Чаще всего холодовая аллергия проявляется у людей до 30 лет, в особенности женского пола. Она может развиваться на фоне хронических воспалительных процессов, связанных с инфекциями (кариес, гайморит, заболевания желчного пузыря, воспаление миндалин, холецистит и т.д.). У людей, зараженных сифилисом или гепатитом, на фоне заболевания возможно развитие холодовой аллергии.
Исследователи высказывают различные мнения о причине возникновения реакции на холод:
В общем смысле, причина заключается в том, что холод каким-либо образом влияет на клетки, в результате чего выделяется гистамин — именно из-за его наличия появляется классическая симптоматика крапивницы. Фактически холодовая аллергия является псевдоаллергией, поскольку процесс проходит без участия IgE.
Виды холодовой аллергии
Большинство специалистов классифицируют ХА на 2 группы — типичная приобретенная и атипичная холодовая. К первой категории относится первичная идиопатическая и вторичная аллергия, ко второй категории — наследственная и приобретенная.
Для типичной формы характерны зуд и волдыри на тех частях тела, которые были слабо защищены и замерзли — лицо, руки до запястья, икры, стопы. Если причины охлаждения еда и питье, проявляется отек языка и глотки, боль в области живота, понос. Иногда наблюдаются тошнота и последующая рвота, слабость, тахикардия, боль в голове и т.д. Наибольшие проявления чаще всего заметны в момент отогревания.
Наследственная атипичная форма проявляется по аутосомно-доминантному типу (относится к CAPS и связана с мутациями в гене) и проявляется в двух видах:
Системная приобретенная атипичная аллергия является одной из самых сложных, поскольку проявления в этом случае тяжелые и генерализованные.
Существует еще несколько классификаций. Например, при рефлекторной холодовой крапивнице покраснения и сыпь появляются вокруг охлажденной области, а не на ней, а при холодовой эритеме образуются не волдыри, а эритемы с болью без зуда. Проба Дункана в этом случае положительна.
Как правило, на наличие аллергии указывают следующие результаты обследований:
Как проходит тест
Холодовой тест Дункана используется для определения повышенной реактивности организма при воздействии холода. Для его применения необходимо при комнатной температуре под наблюдением врача приложить к запястью или предплечью с внутренней стороны кубик льда на 3-5 минут. Лед помещается в непроницаемый пакет, чтобы исключить аквагенную крапивницу. В течение всего исследования врач наблюдает за пациентом. По прошествии указанного времени кубик снимается и выжидается 10 минут.
Результаты могут быть следующими:
При аномальной непереносимости холода первые признаки возникнут через 30 секунд, поэтому важно держать пациента под наблюдением. У некоторых лиц проявления возникают только спустя 20-30 минут. Примерно у 20% больных тест не показывает положительного результата. Такое возможно у пациентов, у которых признаки проявляются только при полном замерзании тела, либо при атипичной патологии или наследственной форме аллергии. Если клиническая картина и собранный анамнез подтверждают наличие проблемы, а холодовой тест дает отрицательный результат, проводят другие виды исследований.
Если тест ничего не выявил?
Ранее для выявления аллергии при отрицательной пробе Дункана выбирали один из двух дополнительных тестов — пребывание в холодной комнате при температуре +4 градуса без одежды в течение нескольких минут и погружение руки в воду с низкой температурой. Эти тесты сопряжены с риском системной реакции и возникновением тяжелых симптомов. Помимо этого, тест с погружением руки в воду может дать ложноположительный результат у пациента с аллергией на воду.
Чтобы избежать негативной симптоматики, вышеуказанные исследования заменяются на исследования крови и забор кожного материала:
Зачем проводить тест?

Врач даст подробные рекомендации о профилактике, выпишет антигистаминные препараты (назальные спреи, глазные капли, таблетки). В зависимости от тяжести проявлений прописываются неседативные, седативные антигистамины, иногда глюкокортикостероиды. Возможно обсуждение проведения десенсибилизирующей терапии холодом.
Записаться на тест в клинике НИАРМЕДИК
В клинике НИАРМЕДИК принимают пациентов врачи высшей категории, обладатели научных степеней, участвующие в профильных семинарах, на конференциях, делающие публикации в научных зарубежных и российских изданиях. Аллерголог выявит любой тип холодовой аллергии и подберет эффективную поддерживающую терапию и профилактические меры.
Филиалы клиники НИАРМЕДИК располагаются как в центре, так и в спальных районах, вы можете подобрать удобное отделение ближе к дому или работе. Мы открыты без выходных до 21.00. Прием ведется по предварительной записи, поэтому вам не придется ждать очереди. Запись ведется на ближайшие несколько дней по телефону или через форму на сайте. При невозможности посещения клиники лаборант может провести пробу с выездом на дом.
Показания и противопоказания к тесту Дункана
Посетить аллерголога рекомендуется в случаях, когда после пребывания на холоде, купания в воде низкой температуры, приема охлажденных напитков и еды наблюдаются следующие симптомы:
Холодовая крапивница — самый распространенный симптом, однако у некоторых пациентов могут соблюдаться и другие симптомы, которые проходят при попадании в сухое помещение с нормальной комнатной температурой. Среди них реакции, похожие на конъюнктивит, гайморит, бронхиальную астму (псевдоаллергический ринит или конъюнктивит) — покраснение глаз, чихание, насморк, слезотечение, кашель, удушье.
Если вы узнали свои симптомы в этих описаниях, пройдите обследование, включающее проведение холодовых тестов, в том числе теста Дункана.
Что такое холодовая проба в медицине
Сердечно – сосудистые заболевания широко распространены и являются основной причиной смертности среди взрослого населения. Метаболический синдром, который представляет собой комплекс основных факторов риска сосудистых катастроф, достигает до 25-35% по частоте встречаемости в общей популяции. В основе метаболического синдрома (МС) лежит тканевая инсулинорезистентность (ИР), способствующая развитию гиперинсулинемии, активации симпатоадреналовой системы, повышению сосудистого тонуса и патологического сдвига в липидном спектре крови [4] На сегодняшний день имеются данные, позволяющие рассматривать нарушение структуры и функции эндотелия, в качестве важного компонента МС [7]. Выстилая сосудистое русло изнутри, эндотелиальные клетки представляют собой первичную мишень для воздействия гемодинамических, биохимических и иммунных факторов циркулирующей крови. Однако эндотелий выполняет не только барьерную функцию, но и является гормонально-активной тканью, вырабатывающей большое количество биологически активных веществ. Эндотелиальная дисфункция является системным патологическим нарушением, которое проявляется ослаблением эндотелий-зависимой вазодиляции и ремоделировании сосудов, что является ранним проявлением патологических процессов в сердечно-сосудистой системе [6]. Нарушение состояния эндотелия сосудов в клинических условиях можно диагностировать по биохимическим и функциональным маркерам. К биохимическим маркерам поврежденного эндотелия относятся изменение концентрации в крови большого количества биологически активных веществ, синтезируемых эндотелием и экспрессируемых на его поверхности, к ним относят: фактор фон Виллебранда, эндотелин-1, молекулы адгезии (Е-селектин, Р-селектин), тканевый активатор плазминогена, тромбомодулин, фибронектин [5].
Одним из признанных биомаркеров дисфункции эндотелия является васкулоэндотелиальный фактор роста (ВЭФ), который принимает участие в формировании атеросклероза, гипертонической болезни, сахарного диабета 2 типа. Экспрессия этого цитокина возрастает при гипоксии, обеспечивая регенерацию эпителия и образование новых сосудов [7].
К значимым и доказанным предиктором смертности от сердечно-сосудистых заболеваний относят микроальбуминурию (МАУ). Микроальбуминурия связана с нарушением капиллярной стенки клубочка с транскапиллярной потерей альбумина и это позволяет расценивать наличие МАУ как четкий маркер развития системной эндотелиальной дисфункции [3].
Однако большее значение для клинициста имеет значение не статические признаки дисфункции эндотелия, которые фиксируют биомаркеры, а возможность динамически оценить степень нарушения эндотелий-зависимую вазодилатацию сосудов. Микрососуды кожи являются удобным и доступным объектом для изучения, в том числе могут быть использованы для исследования функции эндотелия. Для регистрации кожного кровотока наиболее широко используются оптические методы, такие как фотоплетизмография и лазерная допплеровская флоуметрия (ЛДФ) а также термометрия высокого разрешения [6]. Спектральный анализ позволяет оценивать состояние сосудистого тонуса и реакцию его на внешние воздействия. В качестве простых, доступных функциональных проб для оценки состояния кожного кровотока традиционно используются холодовая и тепловая пробы.
На сегодняшний день отсутствует единый диагностический критерий дисфункции эндотелия, это позволило нам применить новый метод, основанный на измерении амплитуд кожной температуры с использованием вейвлет-анализа колебаний. Цель нашего исследования состояла в установлении взаимосвязи между доказанными биомаркерами дисфункции эндотелия и индексами вазоконстрикции и индексами востановления, полученными при проведении непрямой холодовой пробы у пациентов с МС.
Материалы и методы
За индекс вазоконстрикции (ИВК) принято значение k= (ST2-ST1)/ ST1, где ST1 – показатель исходного состояния, ST2- показатель во время холодового воздействия.
За индекс постхолодового восстановления (ИПВ) принято значение k= (ST4-ST1)/ ST1, где ST1 – показатель исходного состояния, ST4 – значение через 10 мин после холодового теста.
Результаты и обсуждение
Представительство различных проявлений МС было следующим. АГ была выявлена у всех пациентов, со средней длительностью 4,57±2,58 года. Отягощенная наследственность по сердечно-сосудистым заболеваниям (ССЗ) также была у всех пациентов. Дислипидемия с гипертриглицеридемией присутствовала у 90 %, гипо ХСЛПВП в 2%, а гипергликемия (без диагноза сахарного диабета) у 65 % пациентов.
У пациентов с МС по сравнению с группой практически здоровых лиц были выявлены повышенный уровень холестерина (ХС), триглицеридов (ТГ), липопротеидов низкой плотности (ЛПНП), глюкозы, мочевой кислоты (табл. 1). Также в группе МС ожидаемо присутствовала гиперинсулинемия и инсулинрезистентность. Кроме того, была установлена прямая достоверная корреляции между величиной окружности талии (ОТ) и уровнем мочевой кислоты (r=0,5; р=0,04), и уровнем ДАД (r=0,43; р=0,03). Инсулинрезистентность (HOMA-IR) сопровождалась повышением ХС (r=0,6; р=0,04), и мочевой кислоты (r=0,6; р=0,02).
Показатели больных с метаболическим синдромом в сравнении с группой практически здоровых лиц (М ± SD)
мочевая кислота (ммоль/л)
р – достоверность отличий в сравниваемых группах
Полученное изменения СКФ, в отсутствии заболеваний почек в анамнезе, и выявление четкой связи между показателями фильтрации, лабораторными проявлениями дисфункции эндотелия и уровня АД отражают начальные проявления нефропатии у больных МС. Полученная взаимосвязь МАУ с уровнем ВЭФ у данной категории больных свидетельствует о дисфункции эндотелия, а в сочетании со снижением СКФ можно рассматривать как раннее проявление почечного повреждения.
Концентрация биомаркеров эндотелиальной дисфункции в группах
Показатель, единица измерения
Значение медианы (25-75% перцентиль); [Min- и Max- величины показателя]
р – достоверность отличий в сравниваемых группах
Была установлена прямая высокой степени корреляция между уровнем ВЭФ и общим холестерином (r=0,74 ; р=0,02), креатинином (r=0,67 ; р=0,001), уровнем САД (r=0,6 ; р=0,02), МАУ (r=0,73 ; р=0,02) и отрицательная корреляция ВЭФ и СКФ (r=-0,7 ; р=0,02).
При проведении холодовой пробы у здоровых лиц амплитуда колебаний кожной температуры во время функциональной нагрузки в эндотелиальном, нейрогенном диапазонах частот достоверно снижалась более чем в 2 раза (табл. 3). После окончания холодового воздействия повышение температуры приводило к симметричному увеличению амплитуд колебаний и практически к их восстановлению до исходных значений в течение первых 3 минут
У пациентов с МС реакция на холодовую пробу значительно отличалась от здоровых лиц (табл. 3). В эндотелиальном диапазоне частот после достоверного снижения амплитуд колебаний кожной температуры их значения практически не нарастали, что свидетельствовало о длительной вазоконстрикции. В нейрогенном диапазоне амплитуды температур после холодового воздействия увеличивались, однако не достигали величины исходного уровня.
В таблице 4 представлены значения индексов реактивности микроциркуляции на холодовой прессорный тест.
Средние амплитуды колебаний кожной температуры (*103, 0С ) при проведении холодового теста
Значения индексов вазоконстрикции и постхолодового востановления в группах
Индекс вазоконстрикции (ИВК) со знаком «-» указывает на уменьшение амплитуды температурных осцилляций в сравнении с исходными значениями. Индексы раннего постхолодового восстановления (ИРВ) и постхолодового востановления (ИПВ) отражают увеличение амплитуды колебаний после окончания холодового воздействия, что соответствуют активности вазодиляторных механизмов.
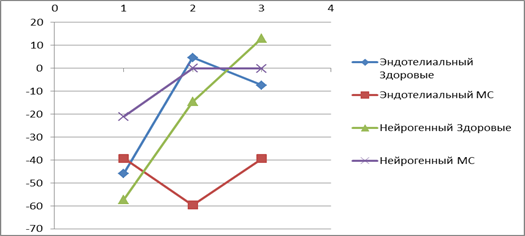
Несмотря на то, что ИВК группе больных МС значимо меньше, чем у здоровых лиц, значения индексов постхолодого восстановления (ИРВ и ИПВ) остаются большим, поскольку увеличения амплитуд колебаний кожной температуры не происходит в силу нарушения вазодилятации. На рисунке схематично представлены значения описанных индексов у здоровых и больных МС.
Рисунок. Индексы реактивности эндотелия у здоровых лиц и больных МС. Значения 1 – ИВК, 2- ИРВ, 3-ИПВ.
Холодовая проба приводит к мощной активации симпатической нервной системы, следствием чего является вазоконстрикция. У здоровых лиц вазоконстрикция на фоне холодовой пробы сопровождается уменьшением амплитуды колебаний кожной температуры и увеличением индекса вазоконстрикции. После окончания холодового воздействия начинается компенсаторная вазодиляции, которая сопровождается увеличением амплитуд колебаний кожной температуры до первоначальных значений в различных диапазонах частот, и следовательно снижается значение индекса постхолодовой восстановления. Таким образом, такую реакцию можно считать адекватной на прессорную пробу и расценивать как сохранение вазодилатационной функции эндотелиальных клеток.
У пациентов МС индекс постхолодовой вазодиляции в эндотелиальном диапазоне частот имеет высокие значения, а в нейрогенном значимо меньше, чем в группе сравнения, что отражает отсутствие восстановления амплитуд колебаний за счет нарушение вазодилаторных механизмов и может считаться признаком эндотелиальной дисфункции.
Наши данные подтверждают наличие взаимосвязи между показателями эндотелиальной дисфункции и метаболическими нарушениями при МС. Получена обратная корреляция между уровнем ХС ЛПВП и ИВК в эндотелиальном диапазоне частот (r=-0,73 ; р=0,001), т.е. чем ниже ХС ЛПВП, тем сильнее вазоконстрикция. Уровень инсулина коррелировал с ИВК в эндотелиальном (r=0,66 ; р=0,02), и нейрогенном диапазонах (r=0,64 ; р=0,01) частот.
На молекулярном уровне инсулин оказывает чрезвычайно сильное стимулирующее действие на экспрессию гена eNOS и на активность этого важного фермента для осуществления вазодилятации. При инсулинорезистентности действие инсулина через ФИ-3-киназу значительно угнетается, и в результате снижается влияние инсулина на активность eNOS и выработку NO. Было установлено, что в этих условиях инсулин утрачивает способность поддерживать стабильное состояние гладко-мышечных клеток (ГМК) и, наоборот, начинает стимулировать их миграцию и пролиферацию через неповрежденный МАП-киназный путь, т.е. действовать проатерогенно [9,5]. Таким образом, при МС подтверждается значимый вклад инсулинемии в развитии и поддержании эндотелиальной дисфункции, и в первую очередь, в усилении вазоконстрикторных влияний.
Связи между сывороточной концентрацией ВЭФ и изменениями амплитуд колебаний сосудистого тонуса не было получено. Однако, значимое увеличение уровня ВЭФ и МАУ у пациентов МС, а также полученные положительные корреляции уровней МАУ и ВЭФ с АД, могут косвенно свидетельствовать о связи увеличения значений биомаркеров вазоконстрикции с нарушением вазодилятирующей функции эндотелия, выявленным при термометрии.
Существует две точки зрения на причину эндотелиопатии при МС [5, 7]. С одной стороны утверждается, что дисфункция эндотелия вторична по отношению к имеющейся ИР, т.е. является следствием гипергликемии, артериальной гипертонии, дислипидемии. Влияние этих процессов на повреждение эндотелия достаточно изучено. При гипергликемии в эндотелиальных клетках активируется фермент протеинкиназа-С, который увеличивает проницаемость сосудистых клеток для белков и нарушает эндотелий-зависимую релаксацию сосудов. Кроме того, гипергликемия активирует процессы перекисного окисления, продукты которого угнетают сосудорасширяющую функцию эндотелия. При артериальной гипертонии повышенное механическое давление на стенки сосудов приводит к нарушению архитектоники эндотелиальных клеток, повышению их проницаемости для альбумина, усилению секреции сосудосуживающего эндотелина-1, ремоделированию стенок сосудов. Дислипидемия повышает экспрессию адгезивных молекул на поверхности эндотелиальных клеток, что дает начало формированию атеромы. Все перечисленные состояния, повышая проницаемость эндотелия, экспрессию адгезивных молекул, снижая эндотелий-зависимую релаксацию сосудов, способствуют прогрессированию атерогенеза и сосудистых катастроф.
С другой стороны можно считать, что дисфункция эндотелия является не следствием, а причиной развития ИР и, соответственно, связанных с ней состояний (гипергликемии, гипертонии, дислипидемии). Действительно, для того чтобы соединиться со своими рецепторами, инсулин должен пересечь эндотелий и попасть в межклеточное пространство. В случае первичного дефекта эндотелиальных клеток трансэндотелиальный транспорт инсулина нарушается и может развиться состояние ИР [5]. В таком случае ИР будет вторичной по отношению к эндотелиопатии. Нарушение секреторной (эндокринной) функции эндотелия, которое проявляется дисбалансом веществ, вырабатываемых им, ухудшает эндотелий-зависимое расслабление вследствие уменьшения синтеза NО при сохраненной или увеличенной продукции вазоконстрикторов, что ведет к изменению цитоархитектоники сосудов [1]
Пациенты с МС имели значимые отличия от здоровых лиц по всем метаболическим показателям. Полученные результаты дают основание полагать, что в данной категории пациентов повреждающими агентами в отношении эндотелия являются АГ, гипеурикемия, дислипидемия, гипергликемия, гиперинсулинемия. Кроме того, группа МС характеризовалась повышением ВЭФ, что определенно указывало на наличии дисфункции эндотелия. Нарушения вазодилации, выявленные при функциональной холодовой пробе у пациентов с МС, подтвердили взаимосвязь между аномальной сосудистой реактивностью и маркерами эндотелиальной дисфункции.
Таким образом, наши данные свидетельствуют о том, что при МС имеется дисбаланс между факторами, обеспечивающими в норме оптимальное течение всех эндотелийзависимых процессов, который может быть выявлен методом кожной термометрии с использованием вейвлет-анализа амплитуд колебаний.
1. Нормальный уровень ВЭФ и МАУ, биомаркеров эндотелиальной дисфункции, сопровождается адекватной реакцией эндотелия на холодовой стресс. У здоровых лиц амплитуда колебаний кожной температуры во время функциональной нагрузки в эндотелиальном, нейрогенном диапазонах частот достоверно снижается. После окончания холодового воздействия амплитуда колебаний увеличивается и в течение 3 минут восстанавливается до исходных значений.
3. У пациентов МС дисфункция эндотелия проявляется повышением уровня ВЭФ и МАУ, значения которых коррелируют с уровнем АД, мочевой кислоты и липидов крови. Снижение СКФ сопряжено с увеличением уровней МАУ и ВЭФ, что можно рассматривать как подтверждение раннего почечного повреждения при МС.
4. У пациентов с МС при холодовой пробе после достоверного снижения амплитуд колебаний отсутствует их увеличение в эндотелиальном диапазоне частот и отсутствует окончательное восстановление в нейрогенном диапазоне, что объясняется нарушением процессов вазодилатации. Индекс вазоконстрикции в эндотелиальном и нейрогенном диапазонах частот связан с уровнем инсулинемии.
5. Результаты, полученные методом кожной термометрии с использованием вейвлет-анализа амплитуд колебаний температур, коррелируют с основными факторами, характеризующими дисбаланс эндотелий-зависимой регуляции тонуса сосудов и может использоваться для диагностики эндотелиальной дисфункции
Работа выполнена при поддержке ГРАНТа РНФ № 14-15-00809.
Рецензенты:
Желобов В.Г., д.м.н., профессор кафедры госпитальной терапии ГБОУ ВПО Пермский государственный медицинский университет им. академика Е.А.Вагнера) Минздрава России, г. Пермь;
3aвражных Л.А., д.м.н., главный врач ЗАО «Курорт Усть-Качка», г. Пермь.
Оценка состояния автономной нервной системы у больных сахарным диабетом методом высокочастотной ультразвуковой допплерографии
Зеленина Т.А., Ворохобина Н.В., Мациевский Н.А., 2014
В методических рекомендациях рассматриваются проблемы ранней диагностики автономной сердечно-сосудистой нейропатии у больных сахарным диабетом.
Методические рекомендации предназначены для врачей общей практики, эндокринологов, для врачей кабинетов «диабетическая стопа», хирургов, сосудистых хирургов, врачей функциональной диагностики, а также могут быть рекомендовано преподавателям медицинских и фармацевтических образовательных учреждений, студентам медицинских вузов, преподавателям учреждений последипломного образования.
Условные сокращения:
АД – артериальное давление
ВЧУД – высокочастотная ультразвуковая допплерография
КАН – кардиальная автономная нейропатия
СД – сахарный диабет
ЧСС – частота сердечных сокращений
Сахарный диабет (СД) является одной из самых распространенных эндокринных патологий. Так, во всем мире насчитывается более 200 млн. больных СД, и, по самым оптимистичным прогнозам, это число должно удвоиться к 2025 году. Только в России в 2000 году было зарегистрировано более 2,07 млн. больных СД, а к 2025 году ожидается 4,51 млн. больных, т.е. в 2,18 раз больше, чем в 2000 году.
Наряду с этим растет и количество поздних осложнений СД. Наиболее распространенным осложнением СД, приводящим к ранней инвалидизации и смертности этих больных, является поражение нервной системы. Страдают как центральная, так и периферическая нервные системы, особенно у больных СД 2 типа, когда на момент постановки диагноза уже у 40-60% пациентов выявляются поздние осложнения диабета. Поражение периферической нервной системы вовлекает как соматическое, так и вегетативное (автономное) ее звенья. Периферическая сенсомоторная нейропатия является лидирующей причиной поражения стоп у больных СД. Так, язвы стоп встречаются у 5 – 10% пациентов, страдающих СД, а более чем 70 % всех нетравматических ампутаций нижних конечностей выполняются именно по причине синдрома диабетической стопы. Распространенность язвенных дефектов стоп в г. Санкт-Петербурге достигает 7% среди больных СД, по данным скрининга осложнений СД, проведенного в 20 регионах Российской Федерации в рамках федеральной целевой программы «Сахарный диабет». Возможно, только предположить, ввиду отсутствия статистических данных, но с достаточной достоверностью, что в нашем городе проживает около 20000 больных СД с язвенными дефектами стоп, и более 1000 из них ежегодно подвергаются ампутациям нижних конечностей.
Поражение вегетативной (автономной) нервной системы также играет немаловажную роль в патогенезе развития синдрома диабетической стопы. Это и открытие артериоло-венулярных шунтов, со сбросом крови минуя микроциркуляторное русло, лежащее в основе микроангиопатии у больных СД. И нарушение судомоторной функции потовых желез, приводящее к сухости кожи, гиперкератозу, формированию трещин с присоединением грибковой и бактериальной инфекции.
Распространенность кардиальной автономной нейропатии (КАН) среди больных СД составляет от 2,5 до 50%, что главным образом зависит от применяемых критериев и способов диагностики. Такие симптомы, как фиксированный сердечный ритм, ортостатическая гипотензия, диагностируемые при опросе и осмотре больного, свидетельствуют уже о тяжелых, далеко зашедших и необратимых стадиях заболевания. Более 2/3 случаев КАН протекает субклинически, бессимптомно и для их выявления традиционно используются кардиоваскулярные тесты Ewing DJ. Однако проведение этих тестов требует специального оборудования для постоянного мониторирования ЧСС и АД больного. Нарушения этих тестов свидетельствуют уже об органических изменениях и не позволяют оценить ранние, функциональные стадии заболевания. А именно ранние стадии КАН и обратимы, и поддаются терапевтическому воздействию. Для диагностики таких функциональных изменений существуют дополнительные методы: определение спонтанного и индуцированного артериального барорефлекса, спектральный анализ сердечного ритма. Однако эти методы доступны только в научных исследованиях.
Вместе с тем метод высокочастотной ультразвуковой диагностики в последнее время широко применяется для оценки состояния микроциркуляторного сосудистого русла при различных заболеваниях. Метод позволяет не только оценить параметры микроциркуляторного кровотока, который у больных СД зачастую снижен ввиду многих причин, но и проводить функциональные пробы для определения вазомоторной реактивности, которая уже напрямую будет зависеть от автономной адренергической иннервации сосудистой стенки. Приборы для проведения этого исследования имеются во многих кабинетах функциональной диагностики города, что позволяет широко применять метод в рутинной клинической практике.
Таким образом, существуют теоретические предпосылки (и материальная база) для применения метода высокочастотной ультразвуковой допплерографии (ВЧУД) при оценке состояния вегетативной (автономной) нервной системы у больных СД.
Показания к использованию метода высокочастотной ультразвуквой допплерографии при оценке состояния диабетической кардиальной автономной нейропатии
Противопоказания к использованию метода высокочастотной ультразвуквой допплерографии при оценке состояния диабетической кардиальной автономной нейропатии
Острые осложнения СД, любая сопутствующая патология в стадии декомпенсации.
Материально-техническое обеспечение для проведения исследования
Прибор для ультразвуковой высокочастотной допплерографии «Минимакс-Допплер-К» (ООО СП «Минимакс», Россия, Санкт-Петербург) (патент на изобретение № 2152173, зарегистрирован в Государственном реестре изобретений Российской Федерации 10 июля 2000 г.). В приборе имеются датчики частотой 20 и 25 МГц, позволяющие определять кровоток на глубине до 3,5 мм и скорость кровотока от 0,01 см/сек.
Прибор разрешен к применению в медицинской практике на территории Российской Федерации (регистрационное удостоверение № ФСР2007/00810 от 18 сентября 2007 г.).
Описание исследования
1. Определение исходных показателей микроциркуляции
При проведении исследования необходимо соблюдать стандартные условия для получения достоверных измерений. За сутки до исследования исключается прием вазоактивных препаратов, из рациона исключаются кофе, какао, спиртные напитки, шоколад.
Перед исследованием пациент находится в покое, в положении лежа 30 минут при температуре воздуха 24-25 °С. Установка датчика осуществляется без сдавления кожи, для получения качественного сигнала используется в качестве контактной среды акустический гель. При установке датчика в зоне локации необходимо менять угол наклона датчика до получения максимального по амплитуде и звуку сигнала. Звуковой сигнал, полученный с участка микроциркуляторного русла от артериол, характеризуется пульсирующим тихим шумом, синхронизированы с фазой сердечного цикла, визуально сигнал имеет в спектре систолический и диастолический пики.
Звуковой сигнал, полученный с участка микроциркуляторного русла от венул, характеризуется тихим, дующим шумом, напоминающим шум морского прибоя, синхронизированным с фазами дыхания. Визуально сигнал соответствует веретенообразной картине окрашенного спектра, без острых пиков.
Звуковой сигнал, полученный с участка микроциркуляторного русла от капилляров, характеризуется тихим монотонным сигналом, не синхронизированным с фазами сердечного цикла, визуально напоминающим монофазную кривую.
После записи допплерограммы исследуемой области проводится оценка как качественных показателей, полученных допплерограмм (формы, выраженности всех элементов, ширины спектрального окна, аудиохарактеристик кровотока), так и количественных линейных скоростных параметров, включающих среднюю взвешенную систолическую (Vas), среднюю взвешенную конечную диастолическую (Vad), а также усредненную среднюю за сердечный цикл скорости кровотока (Vam). Последний показатель рассчитывался по следующей формуле:
Vаm = (Vаs + 2Vаd) / 3, где Vаm – усредненная средняя за сердечный цикл скорость кровотока, Vаs – усредненная взвешенная систолическая скорость кровотока, Vаd – усредненная взвешенная диастолическая скорость кровотока (см. рисунок).
Рисунок. Кровоток дистального сосудистого русла в норме.
А – систолическая скорость кровотока,
В – диастолическая скорость кровотока,
С – максимальная плотность спектра.
Для оценки сосудистого сопротивления рассчитывают также резистивный индекс по формуле:
RI = (Vas – Vad) / Vas, где RI – резистивный индекс, Vas – средняя систолическая скорость кровотока, Vad – средняя диастолическая скорость кровотока.
По данным высокочастотной ультразвуковой допплерографии, скорость кровотока различных областей кожи в норме колеблется от 2,5 до 4,9 мм/с, поскольку при измерении учитывается не только капиллярный кровоток, но и кровоток в артериолах и венулах.
2. Исследование реактивности сосудов микроциркуляторного русла кожи.
Существует ряд функциональных проб для оценки сосудистой реактивности. Одни из них позволяют оценить реактивность, обусловленную иннервацией микроциркуляторного кровотока кожи (автономная сосудистая нейропатия), другие – состоянием самого эндотелия (эндотелиальная дисфункция). К первым функциональным тестам относятся постуральная (позиционная) проба, проба с гипервентиляцией, температурные пробы, ко второму типу –манжеточная (окклюзионная) проба.
2.1. Оценка рефлекторных изменений микроциркуляторного кровотока.
2.1.1. Постуральная (позиционная) проба.
Постуральная (позиционная) проба проводится для определения рефлекторного изменения кровотока (вено-ртериальный аксон-рефлекс) в ответ на увеличение давления в венах при опускании конечности ниже уровня сердца. В начале пробы определяют показатели перфузии в области ногтевого калика пальцев кисти, затем пациент опускает руку ниже уровня кушетки и остается в таком положении в течение 1 минуты, после чего укладывается в исходное положение. Уменьшение кровотока в опущенной руке начинается с прекапиллярных артериол и распространяется ретроградно на более крупные артерии мышечного типа. В норме уменьшение перфузии развивается в течение 20-25 секунд и достигает 30-45%. Запись допплерограммы производят исходно, во время пробы и через 20-25 секунд после пробы.
Типы реакции во время пробы:
1. Адекватный – повышение линейных скоростных показателей кровотока на 30-45% от исходного, снижение сосудистого сопротивления.
2. Неадекватный (недостаточный либо гиперреактивный)
3. Парадоксальный.
2.1.2. Проба с гипервентиляцией
Во время пробы пациент дышит глубоко (примерно 6 вдохов за 60 секунд) на протяжении 2-х минут. Запись допплерограммы производится исходно и непосредственно после прекращения форсированного дыхания. В норме во время пробы наблюдается сужение сосудов кожи в связи с усилением симпатических влияний, а также прямым действием кислорода на гладкомышечные клетки сосудов и опосредованным влиянием через уменьшение концентрации вазодилататоров и увеличение вазоконстрикторов.
1. Адекватный – снижение линейных показателей скорости кровотока на 20% от исходных, повышение RI – резистивного индекса сосудистого сопротивления.
2. Неадекватный – недостаточный либо гиперреактивный.
3. Парадоксальный.
2.1.3. Холодовая проба
Пробы с температурным воздействие проводятся для оценки симпатических адренергических механизмов регуляции тонуса сосудов кожи конечностей.
Холодовая проба проводится с полным погружением кисти на одну минуту в холодную воду с температурой 2-4°С (плавающий лед) и регистрацией кровотока в контралатеральной конечности. Кровоток контралатеральной кисти регистрируют исходно, во время охлаждения, а также поминутно в течение 3х минут после охлаждения. Измеряется максимальное отклонение усредненной средней скорости кровотока относительно исходного уровня. В норме кровоток во время охлаждения снижается на 30-50%, а после отмены холода возрастает на 20-30% выше исходного.
Вазоконстрикция в контралатеральной конечности имеет рефлекторную природу и связана с симпатической адренергической иннервацией. Вазодилатацию вслед за вазоконстрикцией нельзя объяснить только рефлекторными влияниями, поскольку в дистальных отделах конечностей присутствует только симпатическая иннервация.
1. Адекватный – прирост кровотока после отмены холодового стимула на 20-30% выше исходного, снижение резистивного индекса сосудистого сопротивления.
2. Неадекватный – недостаточный либо гиперреактивный.
3. Парадоксальный.
2.2. Оценка вазомоторной функции эндотелия.
Эндотелий выделяет вазоактивные вещества (оксид азота (NO), простациклин, гиперполяризующий фактор и проч.), а также вазоконстирикторные молекулы, оказывающие влияние на гладкомышечные клетки и вызывающие вазодилатацию или вазоконстрикцию соответственно.
2.2.1. Окклюзионная (манжеточная) проба.
Во время пробы на плечо накладывается манжета манометра, в которую нагнетается давление на 20 – 30 мм. рт. ст. выше систолического давления пациента. Компрессия проводится в течение 3 минут, затем быстрая декомпрессия плечевой артерии.
Определяют тканевую перфузию исходно, а затем на 30 сек., 1-ой, 2-ой, 3-ей, 4-ой и 5-ой минутах после декомпрессии вплоть до восстановления исходных параметров кровотока. Для расчета использовалось максимальное изменение усредненной средней скорости кровотока относительно исходного уровня. В норме после кратковременной окклюзии при сохраненной функции эндотелия регистрируется ускорение кровотока сосудистого русла ниже уровня компрессии в 1,5-3 раза относительно исходного значения.
1. Адекватный – прирост кровотока на 50% и выше от исходного, снижение сосудистого сопротивления.
2. Неадекватный – недостаточный либо гиперреактивный.
3. Парадоксальный.
Возможные осложнения и способы их устранения
Возможны ложноположительные и ложноотрицательные результаты, наличие которых устраняется соблюдением стандартных условий во время проведения проб.
Эффективность использования метода
Было обследовано 27 больных СД 2 типа (19 мужчин и 8 женщин) на базе кафедры эндокринологии им. акад. В.Г. Баранова ГБОУ ВПО СЗГМУ им. И. И. Мечникова Минздрава РФ. Средний возраст пациентов 57,2 ± 1,99 лет, длительность СД 8,6 ± 1,74 лет. При расспросе жалобы на чувство сердцебиения в покое, потемнение в глазах, головокружение при смене положения тела, указывающие на наличие вегетативной (автономной) нейропатии, выявлены только у 5 больных (18,5%). Контрольную группу составили 25 здоровых человек, сопоставимых по возрасту с исследуемой группой.
Для оценки наличия и выраженности кардиальной автономной нейропатии применялись функциональные кардиоваскулярные тесты: тест Вальсальвы, динамометрическая проба, проба с пассивным ортостазом, а также измерялась холодовая вазоконстрикция методом фотоплетизмографии.
Кроме того, оценивали спонтанный артериальный барорефлекс кросс-корреляционным методом.
Холодовая вазоконстрикция и динамометрическая пробы позволяют выявить автономную «вазомоторную» дисфункцию. Во время динамометрического теста пациент выполняет статическую нагрузку: сжимает динамометр в течение 3-х минут с усилием, составляющим треть от максимального. Проба оценивается как положительная (снижение вазоконстрикторного потенциала) при приросте АД, менее чем на 13 мм. рт. ст. Динамометрический тест имеет общие патофизиологические основы с одной из проводимых проб, а именно с окклюзионной (манжеточной) пробой.
КАН определяли, как функциональную, в случае снижения только спонтанного артериального барорефлекса и одного функционального теста, органическую (или начальную), при наличии двух патологических тестов, и выраженную (тяжелую) для всех больных с бессимптомной (или симптоматической) ортостатической гипотензией входе пробы с пассивным ортостазом.
Микроциркуляторный кровоток кожи у ногтевого валика пальцев рук оценивался в покое, а затем во время проб: холодовой и окклюзионной (манжеточной).
КАН диагностирована у 19 пациентов (из 27) (70,4%), выраженная тяжелая КАН у 14 больных СД (51,8%).
Исходно микроциркуляторный кровоток был снижен у всех больных СД, по сравнению с контрольной группой (таблица 1).
Таблица 1. Исходные параметры микроциркуляторного кровотока кожи у больных СД.