что такое hgs у девочек
Норма ХГЧ при беременности. Таблица значений ХГЧ по неделям. Повышенный ХГЧ. Низкий ХГЧ. ХГЧ при внематочной беременности. ХГЧ при ЭКО (ХГЧ после подсадки, ХГЧ на 14 дпп).
Что такое ХГЧ (= бета-ХГЧ)
ХГЧ частично проникает через плацентарный барьер. Уровень ХГЧ у новорожденных примерно 1/400 от уровня в материнской крови. И составляется примерно 10-50 мМЕ/мл при рождении. Период полувыведения – 2-3 дня. Таким образом, у 3 месяцам жизни уровень у новорожденных соответствует норме ХГЧ взрослого человека.
Когда сдавать кровь на ХГЧ
Повышение ХГЧ в крови может быть обнаружено за несколько дней до предполагаемой менструации. Оптимальное время сдачи анализа крови для определения ХГЧ – после задержки менструации.
Однократное определение ХГЧ не может использоваться для диагностики выкидыша или внематочной беременности.
Норма ХГЧ. Расшифровка анализа ХГЧ. Уровень ХГЧ при беременности
Уровень ХГЧ менее 5 мМЕ/мл говорит об отсутствии беременности или о том, что анализ сдан слишком рано. Уровень ХГЧ выше 25 мМЕ/мл – о наличии беременности.
В среднем удвоение уровня ХГЧ происходит каждые 36-72 часа. Уровень ХГЧ достигает своего пика на сроке 9-11 недель беременности (от даты последней менструации) и дальше снижается до 15 недели беременности, оставаясь неизменной в течение оставшегося срока беременности. В 85% случаев уровень ХГЧ на ранних сроках увеличивается вдвое каждые 48-72 часа. По мере развития беременности время удвоения уровня ХГЧ увеличивается до 96 часов.
Нормальное время удвоения ХГЧ
Уровень ХГЧ Время удвоения
1200 мМЕ/мл 48-72 часа
1200 – 6000 мМЕ/мл 72-96 часов
Больше 6000 мМЕ/мл Более 96 часов
При каком значении ХГЧ делать УЗИ?
После достижения уровня ХГЧ 1000 – 2000 мМЕ/мл при ультразвуковом исследовании может быть визуализировано плодное яйцо. Поскольку уровень ХГЧ имеет большую вариабельность, а дата зачатия может быть ошибочна, срок беременности определяется по УЗИ или по данным ЭКО, но не по ХГЧ.
Однократное определение ХГЧ недостаточно, так как важно оценивать динамику роста гормона каждые 48-72 часа.
Нормы ХГЧ по неделям. Таблица ХГЧ
Данные интервалы приведены в качестве справочной информации и не должны быть использованы для интерпретации конкретного анализа на ХГЧ.
Низкий ХГЧ. Что означает ХГЧ ниже нормы?
Отрицательный ХГЧ или ХГЧ, характерный для отсутствия беременности при задержке менструации
Необходимо повторить анализ на ХГЧ через 1-2 дня, возможно, беременность наступила позже ожидаемого срока. Если уровень ХГЧ не вырастет, необходимо искать иные причины задержки менструации.
ХГЧ и биохимическая беременность
ХГЧ и внематочная беременность
Внематочная беременность – беременность, при которой плодное яйцо находится за пределами полости матки. При внематочной беременности могут возникать боли внизу живота, кровянистые выделения. Уровень ХГЧ при внематочной (эктопической) беременности может увеличиваться не так быстро и не так значительно, как при нормально развивающейся маточной беременности. Однако, низкий уровень ХГЧ не позволяет сделать такое заключение однозначно. Начиная с уровня ХГЧ 1000 мМЕ/мл плодное яйцо может быть обнаружено в полости матки. При уровне ХГЧ 2000 мМЕ/мл и отсутствии плодного яйца в полости матки при УЗИ вероятность внематочной беременности значительна.
Повышенный ХГЧ. Что может означать уровень ХГЧ выше нормы?
ХГЧ и многоплодная беременность. ХГЧ и двойня.
Уровень ХГЧ при многоплодной беременности выше, чем при одноплодной, однако скорость нарастания ХГЧ и в том, и в другом случае одинакова.
Пузырный занос
Пузырный занос – редкое осложнение беременности при котором уровень ХГЧ будет значительно повышен, в среднем в 2 раза выше среднего значения для данного срока. К примеру, возможный уровень ХГЧ при пузырном заносе на 36 дней от первого дня последней менструации может достигать 200 000 мМЕ/мл, в то время как при нормально развивающейся беременности ХГЧ будет от 1 200 до 36 000 мМЕ/мл.
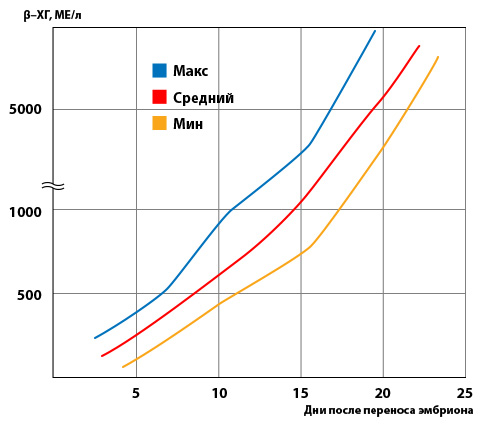
Анализ на ХГЧ после переноса эмбрионов. ХГЧ при ЭКО
Анализ на ХГЧ проводится примерно через 2 недели после переноса эмбриона (12-14 дней после подсадки (дпп)). Обычно уровень ХГЧ на 14 дпп более 100 мМЕ/мл.
Если уровень ХГЧ менее 25 мМЕ/мл, беременность не наступила. При уровне ХГЧ больше 25, тест повторяется через 2 дня, при развитии беременности его уровень должен возрастать. Уровень ХГЧ будет удваиваться примерно каждые 48 часов до 21 дня после подсадки.
Более высокие значения ХГЧ (300-400 мМЕ/мл) с большой вероятностью говорят о многоплодной беременности.
ХГЧ и синдром гиперстимуляции яичников
У пациенток с синдромом гиперстимуляции яичников уровень ХГЧ должен интерпретироваться с осторожностью. У этих пациенток могут развиваться отеки, что ведет к сгущению крови, что может приводить к ложному повышению уровня ХГЧ, а при нормализации состава крови к ложному отсутствию роста уровня ХГЧ.
ХГЧ в более поздние сроки беременности
Тест на ХГЧ входит также в пренатальный скрининг II триместра – анализ, который позволяет оценить риск развития пороков плода.
Повышенный уровень ХГЧ у небеременных женщин и мужчин
Вне беременности ХГЧ может продуцироваться клетками некоторых опухолей (семинома, тератома яичка, новообразования органов желудочно-кишечного тракта (в том числе, поджелудочной железы, печени, колоректального рака и рака желудка).
При успешном лечении ХГЧ-продуцирующей опухоли уровень ХГЧ должен снижаться до нормы.
Как меняется ХГЧ после выкидыша, аборта, родов?
В большинстве случаев уровень ХГЧ снижается. Период полувыведения ХГЧ – 24-36 часов. Скорость достижения нулевых значений ХГЧ зависит от того, что именно произошло: спонтанный выкидыш, аборт, роды, выскабливания) и насколько высоким был уровень ХГЧ в момент потери беременности. Врачи рекомендуют продолжать оценку уровня ХГЧ до достижения его уровня менее 5 мМЕ/мл. Если уровень ХГЧ остается высоким, следует обратиться к врачу.
Какие лекарства влияют на уровень ХГЧ?
На уровень ХГЧ влияют препараты, которые содержат ХГЧ (Прегнил, Хорагон).
Что такое hgs у девочек
Дегидроэпиандростерон-сульфат (ДЭА-SO4) – это андроген, мужской половой гормон, который присутствует в крови как у мужчин, так и у женщин. Он играет важную роль в развитии вторичных мужских половых признаков при половом созревании и может преобразовываться в тестостерон и эстрадиол. ДЭА-SO4 вырабатывается корой надпочечников, его производство контролируется адренокортикотропным гормоном (АКТГ).
Женщинам рекомендуется сдавать анализ на 8-10-й день цикла.
Дегидроэпиандростерон (DHEA, ДГЭА).
Dehydroepiandrosterone Sulfate, 5-Dehydroepiandrosterone (5-DHEA).
Конкурентный твердофазный хемилюминесцентный иммуноферментный анализ.
Мкг/дл (микрограмм на децилитр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Дегидроэпиандростерон-сульфат – это мужской половой гормон (андроген), который содержится в крови как мужчин, так и женщин. Он участвует в формировании мужских вторичных половых признаков во время полового созревания и может быть преобразован организмом в более действенные андрогены (тестостерон и андростендион), а также конвертирован в женский гормон эстроген. Выработка ДЭА-SO4 контролируется питуитарным адренокортикотропным гормоном (АКТГ), а также другими питуитарными факторами.
Дегидроэпиандростерон-сульфат является информативным маркером функции надпочечников. Опухоли и рак надопочечников, а также их гиперплазия могут привести к избыточному производству ДЭА-SO4. У мужчин повышение уровня этого андрогена иногда остается незамеченным, в то время как для женщин оно опасно аменореей и маскулинизацией.
Избыточное производство ДЭА-SO4 у детей способствует преждевременному половому созреванию у мальчиков и неоднозначным наружным половым органам, повышенному оволосению тела и аномальным менструальным циклам у девочек.
Для чего используется исследование?
Когда назначается исследование?
ГЕПАТИТ C у детей и подростков
Почему вирусный гепатит С чаще принимает хроническое течение? Почему в острой стадии вирусный гепатит С диагностируется редко? Какие препараты используются при лечении вирусного гепатита С? Сегодня гепатит C во всем мире представляет собой одну из наи
Почему вирусный гепатит С чаще принимает хроническое течение?
Почему в острой стадии вирусный гепатит С диагностируется редко?
Какие препараты используются при лечении вирусного гепатита С?
Сегодня гепатит C во всем мире представляет собой одну из наиболее значимых медико-социальных проблем. Вирусом гепатита С на данный момент инфицированы 150—200 млн. человек на земном шаре. В США и странах Европы вирус гепатита С (ВГС) является этиологическим агентом в 20% случаев острого гепатита, 70% — хронического гепатита, 40% — цирроза печени, 65% — первичной гепатоцеллюлярной карциномы. Более 30% производимых в мире трансплантаций печени причинно связаны с ВГС.
Из наиболее значимых вирусных поражений печени гепатит С — самый «молодой»: ВГС открыт в 1989 году. Несколько ранее его обозначали как вирус гепатита «ни А, ни В». Он относится к семейству флавивирусов. Основной его особенностью является чрезвычайная изменчивость, способность образовывать так называемые «квазивиды», вследствие чего вирус легко уходит из-под иммунного пресса, а возникающие антитела не обладают защитным действием, а лишь являются «свидетелями», маркерами инфицированности. Существует минимум 6 генотипов ВГС и множество субтипов, имеющих различную чувствительность к интерферонотерапии (наименьшей чувствительностью отличается 1-й генотип, к сожалению наиболее распространенный в нашей стране).
Эти особенности вируса в большой степени предопределяют тот факт, что гепатит С часто принимает хроническое течение (в 75—80% случаев) и, кроме того, возможно, пожизненное носительство, в связи с чем именно хронический гепатит С (ХГС) в последние годы становится все более актуальной проблемой, в том числе и для педиатров.
ХГС, представляющий собой инфекцию с парентеральными путями передачи, все чаще выявляется среди детей и подростков. Как правило, за этим стоят гемоплазмотрансфузии, проведенные до 1997 года, когда вводимые гемопрепараты в нашей стране не тестировались на ВГС, а в последнее время распространение инфекции связано с волной наркомании, захлестнувшей наших подростков, а также с вошедшими в моду татуировкой и пирсингом, не всегда проводимыми в надлежащих условиях. Сегодня, в эпоху разового инструментария, среди медицинских манипуляций в распространении ВГС сохраняют свое значение стоматологические и эндоскопические вмешательства.
Клинические проявления гепатита С чаще всего минимальны. Именно поэтому в острой стадии ВГС обычно не выявляется и, как правило, определяется случайно, при обследовании, например перед операцией, проведением эндоскопии и т. д. Заболевание у детей протекает первично-хронически, долгие годы не сопровождаясь манифестными симптомами, такими как желтушность покровов, увеличение селезенки, подчеркнутая венозная сеть на животе и т. д., которые появляются поздно, знаменуя собой уже переход в цирротическую фазу.
Однако существует ряд симптомов, которые должны насторожить врача и послужить поводом к обследованию на ХГС. Это длительное немотивированное недомогание, утомляемость, необъяснимый субфебрилитет, сосудистые, так называемые «печеночные звездочки», нерезко выраженные, но упорные диспепсические и абдоминальные жалобы, особенно увеличение и уплотнение печени, которое педиатры часто и необоснованно считают допустимым у здоровых детей. Дети и подростки годами наблюдаются с различными диагнозами (дискинезия желчевыводящих путей, гастродуоденит, вегетососудистая дистония и т. д.), обращаются к косметологам по поводу «звездочек». Между тем своевременный диагноз ХГС и начало противовирусного лечения могут существенно и благоприятно повлиять на исход заболевания.
Проведенные в настоящее время серьезные мультицентровые международные исследования показали, что ХГС у детей представляет собой фибротическое прогрессирующее заболевание: более чем у половины детей при повторных пункционных биопсиях печени выявляется нарастание фиброза, причем основным фактором, определяющим темпы этого нарастания (в отсутствие кo-факторов гапатотоксичности, таких как алкоголь, наркотики, сопутствующие тяжелые заболевания и нарушения обмена, медикаментозная нагрузка, стрессы и т. д.), является продолжительность инфицирования, особенно при наличии вирусной репликсации. Согласно результатам исследования, проведенного в клинике акад. РАМН, проф. В. Ф. Учайкина, из 204 детей с ХГС через 10—13 лет у 97% было обнаружено фиброзирование ткани печени, а в 10% случаев уже в первые 5—8 лет сформировался цирроз печени. Длительная спонтанная ремиссия наблюдается лишь у 8% детей. У 82% больных ХГС протекает малосимптомно, но с длительно сохраняющейся активностью процесса (повышение активности АЛТ) и вирусной репликацией (обнаружение РНК ВГС в ПЦР), что и должно служить основанием для постановки диагноза ХГС и вопроса о противовирусном лечении.
Главной целью лечения ХГС, согласно современным представлениям, является прекращение вирусной репликации, ведущее к снижению активности процесса, уменьшению темпов фиброзирования и замедляющее переход в цирроз печени и гепатокарциному. По сравнению со взрослыми пациентами, педиатры ограничены в выборе противовирусных препаратов, далеко не все из которых разрешены к применению у детей.
В настоящее время в лечении ХГС у детей безальтернативным является использование препаратов α-интерферонов, обладающих прямым и сложно-иммунопосредственным противовирусным, иммуномодулирующим и антифибротическим действием.
Показания и противопоказания к интерферонотерапии (ИФН-терапия) приведены ниже. Вопрос о применении ИФН при остром ГС (в редких случаях, когда его удается диагностировать) по-прежнему дискутируется, однако в последние годы мировое сообщество гепатологов склоняется к необходимости ИФН-терапии острого ГС в расчете на уменьшение риска хронизации.
Показания к интерферонотерапии гепатита С у детей
Противопоказания к интерферонотерапии у детей
Принимать решение о целесообразности проведения ИФН-терапии врач должен, не только исходя из наличия показаний и отсутствия противопоказаний, но и с учетом так называемых предикторов эффективности, то есть факторов, которые повышают эффективность лечения, а также шансы достичь ремиссии: полной первичной (если РНК ВГС не определяется, а АЛТ нормализовалась в конце лечения) или полной стабильности (те же показатели сохраняются через 6—12 месяцев после окончания лечения).
Перечень предикторов эффективности ИФН-терапии при ХГС следующий.
Исходя из набора предикторов, уже на старте врач может составить некоторое представление о том, каковы шансы на успех ИФН-терапии, и соответственно, подкорректировать режим лечения (дозы, схемы, комбинированная терапия и т. д.).
Стандартное лечение, рекомендуемое Международным консенсусом гепатологов (Париж, 1999): 3 млн МЕ три раза в неделю в течение 12 месяцев. Этот режим может использоваться у детей всех возрастов начиная с 2 лет с любым генотипом вируса, кроме первого.
При неблагоприятном наборе предикторов терапия ужесточается за счет повышения дозы ИФН, увеличения частоты введения (например, ежедневно в течение первых 2–3 месяцев) или назначения комбинированной противовирусной терапии (см. далее).
Важно отметить, что это лишь схемы, коррекция которых необходима на всех этапах лечения, но для каждого ребенка индивидуально, в зависимости от соотношения показателей эффективности лечения и его переносимости.
Успех лечения напрямую зависит от адекватности применяемых режимов терапии. По данным нашей клиники, полная клиническая ремиссия ХГС достигается у 56–64% детей, при том что спонтанная ремиссия (без противовирусного лечения) регистрируется лишь у 0–4% детей.
Показатель достижения клинической ремиссии у детей значительно выше, чем у взрослых пациентов (до 20–30% успеха), что говорит о перспективности и целесообразности ИФН-терапии ХГС у детей. Полная стойкая ремиссия при ХГС отмечается в среднем у 32–40% детей, получающих препараты ИФН, и у 0–3% не получающих противовирусного лечения, при этом следует подчеркнуть, что показатели эффективности лечения ХГС у детей сильно различаются. Так, при 1 b-генотипе ВГС она не превышает (при монотерапии препаратами ИФН) 20–35%, а при других генотипах (2а, 3а и др.) достигает 70–80%.
Достижение ПСР прямо зависит от исходной активности трансаминаз (57% успеха при высокой АЛТ против 32% при низкой) и в обратной пропорции — от исходной вирусной нагрузки (55% — при низкой и 16% — при высокой).
Но наиболее значимым фактором (после генотипа вируса), влияющим на эффективность ИФН-терапии, является давность заболевания: 64% успеха у детей с давностью заболевания до 3 лет и 11% — при сроке заболевания более 5—10 лет.
Эти факторы говорят о необходимости как можно более раннего выявления и лечения ХГС у детей.
У 16–28% детей в течение первого полугодия после окончания ИФН-терапии может развиться рецидив. В этих случаях терапия возобновляется на 6 месяцев и чаще в виде комбинированного противовирусного лечения.
Таким образом, комбинированная противовирусная терапия является методом выбора:
В качестве второго противовирусного препарата у детей в возрасте от 7 лет может применяться препарат ремантадин (амантадин, римантадин, альгирем), который оказывает противовирусное действие в отношении РНК-содержащих вирусов, прерывая транскрипцию генома вируса и выход вирусных частиц из клетки.
Препарат усиливает противовирусное действие ИФН и при ХГС применяется только в сочетании с ним.
Дозы ремантадина при ХГС у детей:
Длительность лечения — 6 месяцев.
Перед началом ИФН-терапии родителям ребенка следует подробно рассказать о возможных побочных эффектах назначаемого лечения. Последние тем чаще и выраженнее, чем выше доза ИФН и моложе ребенок. Почти у всех детей после первых 3–5 инъекций появляется гриппоподобная реакция: подъем температуры до 38–39°, головная боль, ломота в суставах и мышцах и т. д. В связи с этим мы рекомендуем начинать ИФН-терапию в стационаре, а перед первыми инъекциями назначать антипиретики (парацетамол). В дальнейшем в качестве побочных эффектов может развиться миелосупрессия, в частности наблюдается падение гемоглобина и эритроцитов, особенно тромбоцитов (анализ крови следует проверять ежемесячно), снижение аппетита, похудение, усиление выпадения волос, нервозность. Все эти явления обратимы. В случае их значительной выраженности требуется снижение дозы ИФН или его временная отмена.
Комбинация ИФН с ремантадином не увеличивает опасности возникновения побочных эффектов противовирусной терапии ни качественно, ни количественно.
Эффективность комбинированной терапии существенно выше, чем ИФН-монотерапии: ППР — до 66%, а ПСР — до 58% против 26%, главным образом за счет значимого снижения частоты рецидивов (с 26 до 8%).
Помимо собственно противовирусной терапии, важное значение в лечении ХГС придается применению современных гепатопрепаратов, среди которых препаратом выбора при ХГС является урсодезоксихолевая кислота (УДХК).
Препараты УДХК широко применяются в лечении заболеваний, протекающих с манифестным холестазом (синдром Алажиля, болезнь Байлера и другие врожденные дуктопении, первичный склерозирующий холанит, муковисцидоз, желчнокаменная болезнь и т. д.).
Однако в последние годы стало известно, что благоприятное воздействие УДКХ проявляется не только при лечении вышеперечисленных заболеваний. Наряду с уменьшением холестаза (в том числе субклинического, играющего большую роль в патогенезе хронических гепатитов, и особенно ХГС), УДХК обладает мембраностабилизирующим, гепатопротективным действием (уменьшение токсического повреждения гепатоцитов и эпителия желчных протоков, выражающееся в снижении активности АЛТ и ЩФ). Кроме того, УДХК на разных уровнях блокирует патологический каскад медиаторов, запускающих апоптоз, устраняя или частично нейтрализуя этот важнейший механизм прогрессирования ХГС, а также способствует уменьшению фиброза, что является одной из главных целей лечения ХГС, в том числе противовирусного.
Известное гипохолестеринемическое действие УДХК также весьма благоприятно при ХГС, так как ожирение и стеатоз (см. предикторы) вдвое снижают эффективность противовирусной, в том числе ИФН-терапии.
Поэтому наряду с ИФН-терапией или комбинированным противовирусным лечением назначение УДХК целесообразно при ХГС у детей. Доза УДХК при ХГС 10–12 мг/кг/сутки. Длительность курса от 3–6 до 12 месяцев.
По последним данным, присоединение УДХК, не обладающей собственной противовирусной активностью, к противовирусной терапии ХГС у детей потенцирует противовирусный эффект препаратов ИФН, повышая его с 33,0 до 56,5%.
Кроме того, УДХК в 3,5 раза уменьшает частоту и выраженность побочных эффектов ИФН в отношении ЖКТ (боли в животе, анорексия, похудение): с 29 до 7,8%.
УДХК отличается хорошей переносимостью. Применение ее целесообразно при всех формах ХГС.
Несмотря на открывающиеся сегодня возможности, связанные с успехами противовирусного лечения ХГС, нельзя не признать, что оно не обеспечивает стопроцентного эффекта, сопряжено с необходимостью длительных инъекций, выраженными побочными эффектами и большими материальными затратами.
Весь мир работает над совершенствованием методов терапии ХГС, но, естественно, оптимальным способом могла бы стать профилактика ГС. Однако вакцинопрофилактика этой инфекции значительно затруднена из-за гетерогенности и изменчивости вируса, в связи с чем вакцина против ГС до сих пор не создана.
Таким образом, на сегодняшний день наиболее доступный способ профилактики ХГС — это пусть не очень эффективная, но необходимая работа с детьми, подростками и их родителями с целью предотвращения парентеральных путей передачи этой весьма серьезной инфекции.
А.Р. Рейзис, доктор медицинских наук, профессор ЦМИИ эпидемиологии, Москва
Что такое половое созревание преждевременное? Причины возникновения, диагностику и методы лечения разберем в статье доктора Барковской А. Ю., гинеколога со стажем в 5 лет.
Определение болезни. Причины заболевания
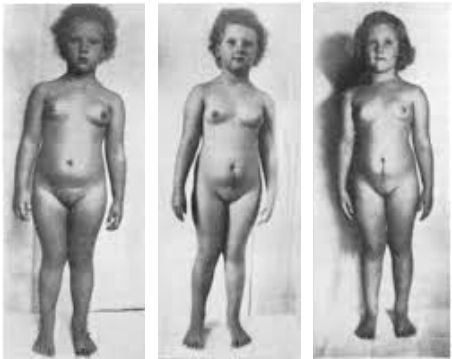
Преждевременное половое созревание — это появление одного или нескольких вторичных половых признаков у девочек в возрасте до 8 лет. К таким признакам относятся рост молочных желёз, первая менструация, появление волос в подмышечных впадинах и на лобке.
Распространённость заболевания коррелирует с возрастом:
Причины появления заболевания:
Факторы риска:
Симптомы преждевременного полового созревания
Преждевременное половое развитие можно заподозрить при появлении у девочки до 8 лет одного или нескольких из следующих признаков:
Дополнительными симптомами, которые позволяют заподозрить патологию, являются:
Патогенез преждевременного полового созревания
Для понимания механизмов заболевания рассмотрим процесс полового созревания при нормальном развитии. Ключевую роль в половом созревании играет гонадотропин-рилизинг гормон. С 2-3 лет и до начала пубертатного периода гипоталамо-гипофизарная система находится в «ювенильной паузе». Далее по мере взросления кора надпочечников становится более чувствительной к воздействию АКТГ (гормону гипофиза), за счёт этого увеличивается выработка тестостерона.
Тестостерон в жировой ткани под действием ферментов трансформируется в эстроген. Растущий уровень эстрогена способствует развитию органов малого таза, наружных половых органов и молочных желёз (телархе).
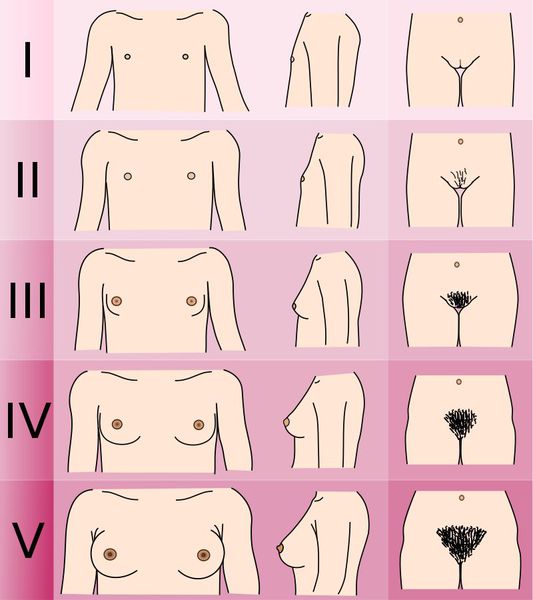
Под воздействием андрогенов и эстрогенов появляются волосы в подмышечных впадинах, на половых губах, а затем на лобковом треугольнике. Происходит резкий скачок роста. Как правило, первыми развиваются молочные железы в среднем в 10,5 лет — появляются одно- или двусторонние образования в субареолярной зоне, чувствительные при пальпации. Далее эти уплотнения растут, выходят за пределы ареолы, ареолы пигментируются и формируются соски.
Далее рассмотрим патологические механизмы преждевременного полового созревания. Выделяют две формы патологии — гонадотропин-зависимую и гонадотропин-независимую.
Гонадотропин-зависимая форма. Она обусловлена преждевременной активацией гипоталамуса под воздействием неблагоприятных факторов. В следствие этого выработка гонадотропин-рилизинг гормона происходит раньше. Также с опережением гипофиз и яичники начинают продуцировать половые гормоны. Неблагоприятными факторами могут быть:
Синдром может также возникать в результате механического сдавления и нарушения работы гипофиза и гипоталамуса. К патологии приводят следующие факторы:
Гонадотропин-независимая форма. При этой форме половые гормоны вырабатываются без влияния гормонов гипоталамуса в периферических тканях. Причинами могут быть:
Также выделяют неполные формы. Для них не характерен скачок роста, изменения фигуры, увеличение костного возраста (степени зрелости костей). Патогенез неполных форм изучен недостаточно.
Классификация и стадии развития преждевременного полового созревания
Классификация полового созревания основывается на патофизиологическом механизме формирования заболевания.
Выделяют полные и неполные формы преждевременного полового созревания.
К полным формам относят:
Неполные формы:
Осложнения преждевременного полового созревания
Известно, что эстроген участвует в костном обмене кальция. При большой его концентрации закрываются зоны роста трубчатых костей. Соответственно, при синдроме преждевременного полового созревания из-за высокого содержания половых гормонов костный возраст начинает опережать биологический, вследствие чего осложнением заболевания часто становится низкорослость.
Диагностика преждевременного полового созревания
Подозрение на синдром преждевременного полового созревания возникает при появлении одного или нескольких из клинических признаков: андренархе и пубархе (появление лобковых и подмышечных волос), телархе (увеличение молочных желёз), менархе (начало менструаций) в возрасте до 8 лет.
Для диагностики синдрома используют следующие методы:
Антропометрия. Оценивается рост и вес ребенка, скорость их увеличения за последние 3-6 месяцев. Далее эти параметры сравниваются со средними значениями для данного возраста по центильным номограммам.
Сущность центильного метода оценки роста заключается в следующем — результаты измерений у большой группы детей одного пола и возраста располагают в восходящем порядке в виде упорядоченного ряда, который делят на интервалы. Средняя линия (50-я перцентиль) — это средний показатель роста для данного возраста. Нижняя линия графика (3-я перцентиль) — такой рост имеют 3 % детей данного возраста. Верхняя линия графика (97-я перцентиль) — такой рост также имеют 3 % детей данного возраста. Низкорослость как осложнение синдрома диагностируется при показателях роста ниже 3-й перцентили [1]
Оценка вторичных половых признаков по шкале Таннера. Шкала предназначена для объективной оценки степени полового развития.
Оценка менструальной функции. Регулярные менструальные кровотечения чаще всего характеризуют центральную форму преждевременного полового созревания. Ациклические кровянистые выделения свойственны периферической форме патологии.
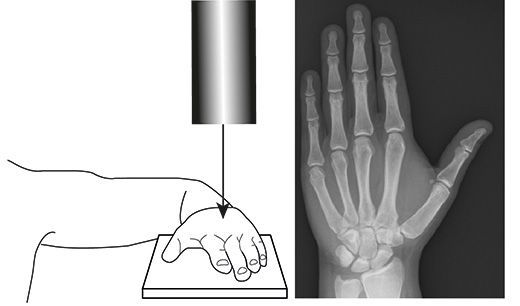
Проведение рентгенографии кистей рук для определения костного возраста. Опережение костного возраста более чем на два года — признак синдрома преждевременного полового созревания.
МРТ головного мозга проводят при подозрении на гонадотропин-зависимую форму и/или при наличии неврологической симптоматики.
УЗИ органов малого таза. Признаками преждевременного полового созревания являются:
Лечение преждевременного полового созревания
Цель лечения — замедлить половое созревание, затормозить прогрессирование костного возраста и помочь ребёнку в психологической и социальной адаптации.
При проведении терапии проводится мониторинг следующих показателей:
Критериями эффективного лечения являются:
При недостаточном клиническом эффекте врач повышает дозировку препарата или сокращает межинъекционные интервалы.
Критериями отмены терапии могут служить:
Показанием для хирургического вмешательства является присутствие неврологической симптоматики или подозрение на злокачественное образование. Решение об операции принимается нейрохирургом. Гонадотропин-зависимая форма преждевременного полового созревания не является показанием к хирургическому лечению.
Прогноз. Профилактика
Прогноз для жизни и здоровья благоприятный. Первичная профилактика синдрома преждевременного полового развития сводится к антропометрии один раз в полгода и оценке стадии полового развития по шкале Таннера в соответствии с возрастом педиатром или родителями.