Что такое фрп в медицине расшифровка
Функциональные расстройства желудочно-кишечного тракта
Функциональные расстройства желудочно-кишечного тракта составляют группу гетерогенных (различных по природе и происхождению) клинических состояний, проявляющихся различными симптомами со стороны ЖКТ и не сопровождающихся структурными, метаболическими или системными изменениями. При отсутствии органической основы заболевания, такие расстройства существенно снижают качество жизни больного.
Для постановки диагноза необходимо существование симптомов на протяжении не менее полугода с активными их проявлениями в течение 3-х месяцев. Следует помнить также, что симптомы ФРЖКТ могут наслаиваться и перекрывать друг друга при наличии иных заболеваний, не связанных с ЖКТ.
Причины функциональных расстройств желудочно-кишечного тракта
Выделяют 2 основные причины:
Симптомы функциональных расстройств желудочно-кишечного тракта
Зависят от вида функционального расстройства:
Диагностика функциональных расстройств желудочно-кишечного тракта
Полное, всестороннее клиническое и инструментальное обследование органов ЖКТ. При отсутствии обнаружения органических и структурных изменений и наличии симптомов дисфункции ставится диагноз функционального расстройства желудочно-кишечного тракта.
Лечение функциональных расстройств желудочно-кишечного тракта
Комплексное лечение включает диетологические рекомендации, психотерапевтические мероприятия, лекарственную терапию, физиотерапевтические процедуры.
Общие рекомендации при запорах: отмена закрепляющих препаратов, продуктов, способствующих запорам, прием большого количества жидкости, пищи, богатой балластными веществами (отруби), физическая активность и устранение стресса.
При преобладании диареи ограничивают поступление в организм грубой клетчатки и назначают медикаментозную терапию (имодиум).
При преобладании болевых ощущений назначают спазмолитики, физиотерапевтические процедуры.
Профилактика функциональных расстройств желудочно-кишечного тракта
Повышение стрессоустойчивости, позитивный взгляд на жизнь, уменьшение вредных влияний на ЖКТ (алкоголь, жирная, острая пища, переедания, несистематичность питания и т.д.). Специфической профилактики не существует, поскольку прямых причинных факторов не обнаружено.
Функциональные расстройства желудочно-кишечного тракта у детей: диагностика и возможности спазмолитической терапии
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Статья посвящена проблеме функциональных расстройств желудочно-кишечного тракта у детей и вопросам их диагностики и лечения
Введение
Функциональные нарушения (ФН) желудочно-кишечного тракта (ЖКТ) – одна из самых распространенных проблем в детской гастроэнтерологии. По данным различных авторов, ФН ЖКТ встречаются у 55–75% детей первых месяцев жизни [1]. По мере взросления ребенка частота функциональных расстройств нарастает, формы их становятся более разнообразными. У многих детей c возрастом наблюдается эволюция симптомов ФН, к примеру: срыгивания у детей до 1 года, циклическая рвота у детей 3–8 лет и абдоминальные боли, диспепсия у детей старше 8 лет [2]. Этому способствуют анатомо-физиологические возрастные особенности развития ЖКТ у детей, нарушения режима и техники вскармливания у младенцев, режима и характера питания – у старших детей, а также нарастающие физические и психоэмоциональные нагрузки, частая сочетанная патология ЦНС. Особенностями детского возраста являются неспецифичность жалоб, которые может предъявить маленький пациент, невозможность локализации боли у детей младшего возраста. Многочисленные жалобы ребенка вызывают значительную тревогу у родителей. На их простые вопросы «Что не так с моим ребенком? Почему такое происходит? Как долго это будет продолжаться? Можно ли это вылечить?» должен ответить педиатр.
Терминология и классификация
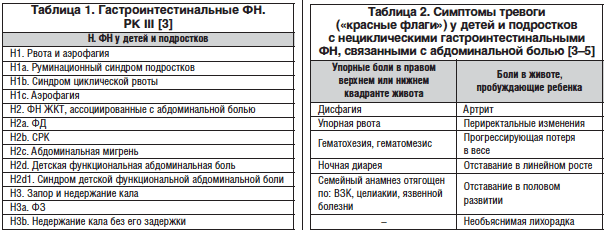
Согласно Римским критериям III пересмотра (РК III, 2006) [3] (табл. 1), гастроинтестинальные ФН у детей и подростков включают разнообразную комбинацию хронических или рецидивирующих симптомов без структурных или биохимических нарушений.
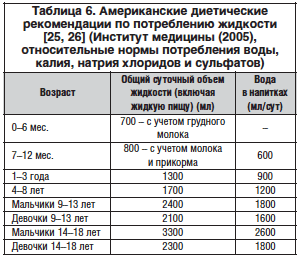
Задача педиатра на первичном приеме при сборе анамнеза болезни и осмотре ребенка обратить внимание на возможные «симптомы тревоги» («красные флаги») (табл. 2) для исключения органической патологии ЖКТ [4–5]. Такие изменения требуют углубленного, нередко инвазивного обследования.
Преимущественный симптом ФН позволяет установить диагноз и определить подходы к терапии. РК III являются важным диагностическим инструментом в ежедневной работе педиатра.
Наиболее часто среди детей и подростков выявляются следующие ФН ЖКТ: абдоминальная боль (25–40% случаев), функциональная диспепсия (ФД) (до 27% случаев), синдром раздраженного кишечника (СРК) (до 45% детей) и функциональный запор (ФЗ) (до 25% случаев). Остальные расстройства (рвота и аэрофагия, абдоминальная мигрень, детская функциональная абдоминальная боль, недержание стула) наблюдаются значительно реже [2, 3, 5, 14, 21].
H2. Функциональные расстройства ЖКТ, связанные с абдоминальной болью
Абдоминальная боль – самая частая, пугающая, но неспецифичная из жалоб у детей при ФН ЖКТ. Она заставляет пациентов и их родителей обращаться за врачебной помощью. 10–15% детей и подростков, не имеющих каких-либо органических заболеваний, предъявляют жалобы на боли в животе [6], т. е. имеют ФН. С другой стороны, боли в животе у ребенка в 90% случаев являются функциональными.
Диагностические РК III [3] позволяют установить преимущественную форму ФН.
H2a. Функциональная диспепсия (табл. 3)
Диспепсия беспокоит от 3,5 до 27% детей и подростков в различных странах [2, 5]. Разграничение диспепсии на варианты – язвенноподобный и дискинетический – у младших детей не оправданно вследствие неспецифичности жалоб, невозможности разграничить чувства боли и дискомфорта в животе [3].
Обязательная необходимость эндоскопического обследования при постановке такого диагноза ставится под сомнение. Частота изменений слизистой оболочки верхних отделов ЖКТ, объясняющих диспепсические жалобы, у детей значительно меньше, чем у взрослых [7]. При «симптомах тревоги» (табл. 2) проведение эзофагогастродуоденоскопии, подтверждение ассоциации с Helicobacter pylori (H. pylori) обязательно, особенно при наличии дисфагии и сохранении или рецидиве упорной симптоматики на фоне антисекреторной терапии [8]. Диспепсия может длительно сохраняться после перенесенных кишечных и респираторных вирусных инфекций [9]. Поэтому наличие умеренных воспалительных изменений в биоптатах слизистой оболочки пищевода, желудка, двенадцатиперстной кишки при морфологическом исследовании не противоречит диагнозу ФН [9]. У детей с ФД наблюдаются: расстройства миоэлектрической активности желудка, замедленная эвакуация пищи из желудка, изменение антродуоденальной моторики, снижение ответа стенки желудка на нагрузку объемом пищи [10–12].
Принципы и подходы к терапии ФД у детей: отказ от применения нестероидных противовоспалительных препаратов, диета с исключением/ограничением провоцирующих продуктов (таких как кофеин, специи, жирная пища). При преимущественно болевом синдроме применяются антисекреторные препараты (ингибиторы протонной помпы), прокинетики – при дискомфорте в верхней половине живота [3]. При подтверждении H. pylori-этиологии функциональных расстройств показана эрадикационная терапия [13].
H2b. Синдром раздраженного кишечника (табл. 4)
Согласно данным западных исследователей, СРК встречается у 22–45% детей 4–18 лет [14].
Подтверждают диагноз СРК сочетание дискомфорта или боли в животе с изменениями стула: частоты (4 и более раз в день или 2 и менее раз в неделю), формы (от «овечьего»/твердого стула до неоформленного/водянистого), нарушение пассажа стула (натуживание, внезапные позывы к дефекации или ощущение неполного опорожнения прямой кишки), пассаж слизи, метеоризм [3].
Основным патогенетическим компонентом СРК является висцеральная гиперчувствительность [15], возникающая из-за ряда патологических процессов: инфекций, воспаления, травмы кишечника, аллергии, нарушающих моторику кишечника [16]. Также имеют значение генетическая предрасположенность, стрессовые ситуации, наличие схожих нарушений у родителей. Часто симптомам СРК сопутствуют тревожность, депрессия и спектр различных соматических жалоб.
В зависимости от ведущего клинического синдрома выделяют 3 варианта течения СРК: с преобладанием болей и метеоризма, с запорами, с диареей. Хотя нередки комбинации и чередование основных симптомов СРК.
Внимательное изучение анамнеза заболевания, возможных триггерных факторов возникновения СРК у пациента, отсутствие «симптомов тревоги», нормальные данные физикального обследования, неизмененные ростовые кривые ребенка позволяют избежать инвазивных процедур в большинстве случаев [17].
Принципы и подходы к терапии разнообразны: беседа с родителями и самим пациентом (снижение тревожности, объяснение причин и механизмов развития данных нарушений), психологическая коррекция, диетотерапия, фармакотерапия (в зависимости от варианта течения СРК – спазмолитики, слабительные или антидиарейные, седативные препараты, пре- и пробиотики), лечебная физкультура и физиотерапия, в т. ч. иглорефлексотерапия.
Лечение
Лечение СРК начинается с изменения стиля жизни, выработки определенного стереотипного поведения в отношении туалета: регулярное посещение туалета и ведение дневника стула, поощрение продуктивного посещения туалета.
Диетотерапия при преобладающих запорах обогащена пищевыми волокнами, включает достаточный объем жидкости, продукты, стимулирующие моторику толстой кишки (фрукты и овощи, молочнокислые продукты). При преобладании диареи включаются продукты с закрепляющим действием. При преобладании метеоризма исключают газообразующие продукты.
Фармакотерапия СРК зависит от варианта его течения [18–20, 30], общим является обязательное подключение седативных средств, адаптогенов, которые может назначить педиатр или невролог. Предпочтительны в педиатрии растительные седативные средства с доказанной эффективностью на основе мяты перечной, мяты лимонной, валерианы. Полезен их дополнительный спазмолитический эффект. Также дополнительный терапевтический эффект при любом варианте СРК дает присоединение к терапии ферментов (при запорах – желчесодержащих), пре- и пробиотиков.

При преимущественно болевом синдроме применяются спазмолитики различных групп и средства, уменьшающие метеоризм (симетикон).
При запорах показаны слабительные, увеличивающие объем каловых масс (лактулоза, макрогол и др.), короткие курсы стимулирующих слабительных, спазмолитики. При диарее применяются антидиарейные средства (лоперамид), сорбенты, спазмолитики. Интересно применение комплексного препарата, содержащего релиз-активные антитела к гистамину, фактору некроза опухоли-a, белку S-100, применяемого при различных вариантах СРК [20]. Терапия направлена не только на купирование основных симптомов СРК, но и на нормализацию моторных нарушений кишки, снижение висцеральной гиперчувствительности, коррекцию механизмов восприятия болей.
H3. Функциональный запор (табл. 5)
Каждый четвертый ребенок страдает запорами [21], более чем у 1/3 детей с этой проблемой заболевание принимает хроническое течение. Истинная частота запоров неизвестна, т. к. не все родители понимают серьезность проблемы и не обращаются за медицинской помощью, занимаясь самолечением. Кроме того, имеется множество возрастных и индивидуальных детских особенностей строения и развития толстой кишки, что обусловливает значительную вариабельность частоты стула у ребенка.
Запор (от лат. constipatio) (по W.G. Thommpson, 1999 [22]) – нарушение функции кишечника, выражающееся увеличением интервалов между актами дефекации по сравнению с индивидуальной физиологической нормой, затруднением акта дефекации, чувством неполного опорожнения кишечника, отхождением малого количества кала повышенной плотности (табл. 6).
Запоры принято подразделять на первичные (функциональные, идиопатические) либо вторичные, связанные с множеством патогенетических механизмов. Вторичные запоры чаще связаны с органическими и неврологическими причинами и очень редко – с эндокринными [23]. Хронические запоры вследствие органических причин, как правило, развиваются постепенно, утяжеляются с ростом ребенка и отражают декомпенсацию функции кишки. Большая часть детей (до 95%) страдают ФЗ [24].
При сборе анамнеза болезни и осмотре следует обратить внимание на возможные «симптомы тревоги» [25, 26], подозрительные в отношении врожденной органической патологии толстой кишки, аномалии развития спинного мозга и метаболических расстройств: возникновение запора с рождения, позднее (более 48 ч) отхождение мекония; отставание в развитии ребенка; выраженный метеоризм и рвота; нарушения раннего моторного развития.
Оценка комплекса данных анамнеза и специализированного физикального обследования ребенка с запором, включающего осмотр перианальной области, ягодиц, спины, оценку мышечного тонуса, силы и рефлексов в нижних конечностях, в некоторых случаях – пальцевое ректальное исследование, позволяет решить вопрос о необходимости дальнейших диагностических мероприятий. Если запор носит функциональный характер, назначается стартовая терапия. В большинстве случаев не требуется дальнейших инструментальных исследований. Обнаружение «симптомов тревоги» является показанием к дообследованию ребенка [26].
Для успешного лечения запора необходим индивидуальный подход к каждому ребенку. Нужно учитывать все возможные факторы: возраст ребенка, этиологию и длительность запора, наличие сочетанной патологии, эффективность ранее проведенного лечения. Комплексное лечение запоров включает изменение образа жизни, коррекцию питания, медикаментозные и немедикаментозные методы лечения (лечебная физкультура, физиотерапевтические процедуры, санаторно-курортное лечение, методика биологической обратной связи).
Для ребенка старшего возраста крайне важна «информационная поддержка»: в беседе с ребенком и родителями обсуждаются вопросы о частоте и качестве стула, запорах, на руки даются материал о содержании диеты, лечебной физкультуре, памятка о приеме лекарств, информация о наблюдении для участкового педиатра. В рационе ребенка старше 1 года, страдающего запором, должна быть пища с высоким содержанием пищевых волокон (отруби, овощи, фрукты), лакто- и ацидофильными бактериями.
Для профилактики запоров у детей старшего возраста необходимым условием является постоянная физическая нагрузка. Лечебная физкультура должна быть направлена на повышение давления в брюшной полости, стимуляцию кишечной моторики, укрепление мышц тазового дна. Необходимы соблюдение режима дня, профилактика острых инфекционных заболеваний.
Согласно данным большинства исследователей, даже стартовая терапия запоров не должна ограничиваться рекомендациями относительно режима и диеты (достаточный прием жидкости и пищевых волокон) [26]. Имеющиеся в арсенале педиатра слабительные средства разделяются на группы по механизму действия (табл. 7) [23].
Лекарственная терапия запоров для детей до 1 года: в качестве смягчителей показаны лактулоза, сорбит, кукурузный сироп, изредка стимулирующие слабительные, не показаны минеральные масла. Дети старше 1 года: возможна диетическая коррекция (фрукты, овощи, зерна), из лекарственных средств применяются минеральные масла, магния сульфат, лактулоза, сорбитол, короткие курсы стимулирующих слабительных(возможно использование пикосульфата натрия (Гуттулакс®) у детей младше 4-х лет в дозировке 1 капля на 2 кг массы тела), длительный прием полиэтиленгликоля (макрогол) в низких дозах у детей с упорным запором [3, 23–28].
Дополнительное назначение препаратов определяется преимущественным механизмом развития запора и спектром сочетанной патологии, применяются спазмолитики, прокинетики, желчегонные препараты, ферменты с желчными кислотами, пре- и пробиотики.
Правильное формирование туалетных навыков, метод биологической обратной связи высокоэффективны при аноректальной дисфункции [27, 28].
Гладкомышечный спазм часто является патогенетически последним звеном и основной причиной многих ФН ЖКТ у детей, прежде всего синдрома абдоминальной боли, СРК, большинства случаев ФЗ.
В арсенале педиатра имеется большой спектр спазмолитических препаратов, список их постоянно пополняется [29].
Регуляция активности гладкомышечных клеток осуществляется центральной и вегетативной нервными системами, а также воздействием на опиоидные и серотониновые рецепторы с помощью нейропептидов. Спазмолитические препараты можно разделить на 2 группы: нейротропные и миотропные.
Нейротропные препараты влияют на проведение импульса в вегетативной нервной системе путем действия на холино- и адренорецепторы. Наиболее известен и активно применяется в педиатрии препарат тримебутин, действующий на энкефалиновые рецепторы нервных сплетений Мейсснера и Ауэрбаха, обладающий прокинетическим и спазмолитическим действием. Показания к применению анксиолитиков и антидепрессантов, также обладающих нейротропным спазмолитическим действием, в педиатрии ограничены.
В практической педиатрии наиболее широко применяются миоспазмолитики. Возбуждение М-холинорецепторов вызывает открытие натриевых каналов, поступление ионов натрия в клетку приводит к деполяризации мембраны, открытию потенциал-зависимых кальциевых каналов и поступлению ионов кальция в клетку. Далее следует каскад биохимических реакций, приводящий к образованию актин-миозинового комплекса, сокращению миоцита. Расслабление миоцита происходит за счет накопления в клетке циклического аденозинмонофосфата (цАМФ) и циклического гуанозинмонофосфата.
В настоящее время известно несколько групп миотропных спазмолитиков, отличающихся по механизму действия.
Дротаверин и папаверин давно используются в педиатрии и доказали свою эффективность. Препараты ингибируют фосфодиэстеразу 4-го типа, что ведет к накоплению цАМФ и расслаблению миоцита. Однако системность их действия на гладкомышечные органы, наличие постспазмовой гипотонии ограничивают курсовое применение, препараты чаще применяются по требованию.
Необходимость селективного действия спазмолитиков привела к созданию новых препаратов.
Мебеверин – миотропный спазмолитик, блокирующий натриевые каналы. Эффективность препарата выше, чем у традиционных спазмолитиков, он хорошо переносится, действует длительно (до 12 ч), включен в схемы лечения заболеваний кишечника, билиарных путей, поджелудочной железы, но имеет возрастные ограничения – применяется только с 18 лет.
Сочетанное действие пинаверия бромида связано с блокадой кальциевых каналов, подавлением спазма, вызванного холецистокинином и субстанцией Р, умеренным М-холиноблокирующим эффектом. Препарат широко используется в гастроэнтерологии при многих ФН ЖКТ у взрослых больных. Опыт применения его в педиатрии ограничен, препарат не рекомендован до 18 лет.
К спазмолитикам первой ступени применяется ряд требований: высокий уровень безопасности, высокая спазмолитическая активность, длительный спазмолитический эффект, большой международный опыт применения, доступность (невысокая стоимость), возможность самолечения (безрецептурный отпуск), наличие пероральных форм.
Гиосцина бутилбромид (Бускопан®, «Берингер Ингельхайм Фарма», Германия) как медицинский препарат известен с 1950-х гг., впервые получен и применен в Германии и неоднократно доказал свою эффективность и безопасность во многих странах при различных заболеваниях, сопровождающихся болевым синдромом [30]. Гиосцина бутибромид – М-холиноблокатор на натуральной основе (получен из листа растения Datura stramonium) и является уникальным спазмолитиком направленного действия, тропным к гладкомышечным клеткам стенок внутренних органов: ЖКТ, желчевыводящих и мочевыводящих путей [31]. Бускопан® обладает также антисекреторным эффектом, снижая секрецию пищеварительных желез. Быстрый клинический эффект (через 15 мин) объясняется прямым М-холиноблокирующим действием. Действие холинолитических препаратов тем сильнее, чем выше начальный тонус блуждающего нерва, что важно при вегетативной дисфункции, являющейся фоном ФН ЖКТ.
Гиосцина бутилбромид является четвертичным аммониевым производным и не проникает через гематоэнцефалический барьер [31], поэтому не оказывает антихолинэргического влияния на ЦНС, что важно для более свободного и безопасного применения препарата Бускопан® в педиатрии. Большим преимуществом данного лекарственного средства является избирательность его спазмолитического действия – только в месте возникновения спазмов. Сохранение перистальтической активности ЖКТ при ФН способствует нормализации моторной функции толстой кишки.
Бускопан® имеет широкий спектр показаний к применению: различные спастические состояния – желчные, кишечные и почечные колики, спастическая дискинезия желчевыводящих путей, пилороспазм, комплексная терапия обострений язвенной болезни желудка и двенадцатиперстной кишки, холецистита. Однозначным преимуществом для применения в педиатрии является наличие различных форм препарата: Бускопан® выпускается в виде таблеток, покрытых сахарной оболочкой, и ректальных суппозиториев по 10 мг; назначается детям старше 6 лет по 1–2 таблетке (10 мг) 3 р./сут или по 1 суппозиторию (10 мг) 3 р./сут per rectum [31].
Множество исследований [33–36] показало безопасность и эффективность применения препарата Бускопан® в педиатрии для купирования абдоминального болевого сидрома, различных диспепсических расстройств, симптомов СРК, улучшения качества жизни таких пациентов. Интересно применение различных форм препарата в комплексной терапии хронических ФЗ у детей в зависимости от преимущественного механизма их возникновения [36]. Подчеркивается дополнительное преимущество ректальной формы препарата (прямое спазмолитическое на сфинктеры прямой кишки и местнораздражающее действие) при дисфункции анального сфинктера.
Таким образом, ФН ЖКТ – распространенная проблема среди детей различного возраста. Проявления ФН ЖКТ разнообразны, имеются определенная динамика и эволюция симптомов с возрастом. ФН любой локализации свойственны рецидивирующее течение, повышенная тревожность пациента, сочетанные нарушения со стороны других систем органов, что значительно снижает качество жизни ребенка.
Учитывая необходимость уменьшения инвазивности процедур в детском возрасте диагностика функциональных состояний ЖКТ педиатром возможна на основе РК III, но следует осуществлять обязательный динамический контроль «симптомов тревоги».
Патогенетическая терапия ФН ЖКТ может быть только комплексной с обязательной коррекцией сопутствующих нейрогенных расстройств, сочетанным применением медикаментозной и различных методов немедикаментозной терапии.
Гиосцина бутилбромид (Бускопан®) является высокоэффективным безопасным спазмолитиком для купирования спастических состояний при различных ФН ЖКТ у детей, особенно при ФН с диспепсией, абдоминальной болью, СРК, ФЗ. Наличие оральных и ректальных форм препарата удобно в педиатрии, в т. ч. при запорах с аноректальной дисфункцией.
Последние годы ознаменовались прогрессом в детской гастроэнтерологии, что привело к значительным достижениям в диагностике, лечении и профилактике заболеваний желудочно-кишечного тракта (ЖКТ) у детей.
Последние годы ознаменовались прогрессом в детской гастроэнтерологии, что привело к значительным достижениям в диагностике, лечении и профилактике заболеваний желудочно-кишечного тракта (ЖКТ) у детей. Данные литературы свидетельствуют о большой частоте заболеваний органов пищеварения с 8000 до 12000 на 100000 детского населения. Характерен возраст от 5 до 12 лет, в котором происходят наиболее интенсивные морфофункциональные изменения органов и систем и возникает дезинтеграция роста. Этим обусловлены функциональные нарушения ЖКТ, которые занимают ведущее место среди заболеваний органов пищеварения у детей (удельный вес 60-80%) и способные к прогрессированию и формированию органической патологии. Чаще обнаруживаются у детей раннего возраста (первый возрастной пик заболеваемости), особенно у преждевременно родившихся младенцев. Диагностика функциональных нарушений ЖКТ часто вызывает значительные трудности у практических врачей, приводя к большому числу ненужных обследований, а главное, к нерациональной терапии. Клинические и инструментальные, новые функциональные и морфологические методы исследования расширили представление об этиологии и патогенезе хронических заболеваний ЖКТ. Своевременно поставить диагноз, провести оптимальное лечение и реабилитационные мероприятия являются задачей детской гастроэнтерологии. Для этого прежде всего следует знать анатомо-физиологические особенности органов пищеварения в детском возрасте и методы исследования.
Анатомо-физиологические особенности органов пищеварения у детей
Полость рта новорожденного сравнительно мала, она покрыта нежной, легко ранимой слизистой. Язык относительно велик. Жевательная мускулатура хорошо развита. Имеются комочки Биша (жировые комочки в толще щек). Характерна дуплекатура слизистой оболочки десен и складчатость губ. Здоровый доношенный новорожденный рождается с выраженной способностью сосания. Это сложный рефлекс, возникающий без участия коры головного мозга. Центр его расположен в продолговатом мозгу. Активность сосательных движений является показателем зрелости и здоровья ребенка.
Слюнные железы в первые недели жизни ребенка развиты слабодо 3-4 месяцев. Слюна содержит птиалин, мальтазу, лизоцим, бактериолизин и IgA.
Пищевод – мышечная трубка длиной 8-10 см у новорожденных и 25 см у подростков. Физиологические сужения у детей раннего возраста слабо выражены, недостаточно развита слизистая оболочка и мышцы.
Желудок. Горизонтальное расположение желудка, недостаточное развитие кардиального отдела и хорошее развитие пилорического сфинктера приводят к срыгиваниям, которые часто наблюдаются в грудном возрасте. Моторика желудка у этих детей замедлена и перистальтика вялая. Емкость составляет у новорожденных 30-35мл, в 1 год – 250-300мл и в 8 лет – 1000мл. Общая кислотность и ферментативная активность более низкая, чем у взрослых, что определяет низкую барьерную функцию желудка и рН желудочного сока. Это позволяет сохранить иммунные факторы защиты, имеющиеся в женском молоке.
Желудочный сок содержит соляную кислоту и ферменты, такие как пепсиноген, катепсин, гастриксин, химозин, липазу, гастрин. Соляная кислота стимулирует верхние отделы ЖКТ и преобразует пепсиноген в пепсин. Главные клетки желудка синтезируют и внутренний фактор Кастла, необходимый для всасывания витамина В12 в кишечнике. Бикарбонаты и слизь обеспечивают защиту ЖКТ от отрицательного воздействия кислоты и пепсина.
Двенадцатиперстная кишка (ДПК) вырабатывает более 30 гормонов, такие как энтерогастрон, секретин, холецистокинин, панкреозимин и др. они заставляют кишечные железы активно выделять сок, возбуждают моторику кишечника, регулируют деятельность желчного пузыря и поджелудочной железы. Некоторые гормоны обладают общим действием и оказывают влияние на обмен веществ в организме, нервную, эндокринную и сердечно-сосудистую системы. ДПК у детей до 12 лет отмечается высокой подвижностью.
Тонкая кишка обеспечивает полостное пищеварение благодаря синтезу ферментов энтерокиназы, щелочной фосфатазы, липазы, амилазы, мальтазы, сахаразы, лактазы идр. Здесь происходит основной процесс мембранного или пристеночного пищеварения, который обеспечивает всасывание конечных продуктов расщепления пищевых веществ, воды, электролитов и витаминов. Тонкая кишка обеспечивает защиту организма от поступивших извне токсинов.
В толстой кишке продолжает всасываться вода и электролиты. Она выполняет накопительную функцию и обладает сократительной активностью благодаря 4 видам моторики. Соотношение между ростом и длиной всего кишечника у новорожденного составляет 1:8, к году 1:6, у подростков 1:5. Относительно длинная кишка, ее изгибы обуславливают привычные запоры, а недостаточная координация с сокращениями мышц анального сфинктера приводят к затруднениям акта дефекации.
Между тощей и подвздошной кишкой нет четкой границы. Длинная и легко растяжимая брыжейка может привести к перекрутам и инвагинациям. Слабая фиксация слизистого и подслизистого слоев прямой кишки способствует к их выпадению при тенезмах и упорном запоре. У старших детей причиной затруднения опорожнения являются ослабление перистальтических движений. Эпителиальные клетки кишечника участвуют в синтезе Ig, обеспечивая защиту, толерантность или аллергию.
Кишечник самый большой орган иммунной системы, содержащий 80% всех иммунокомпетентных клеток. Число микроорганизмов составляет порядка 10 14, что в 10 раз превышает количество клеток в организме человека. Большое значение имеет микрофлора кишечника и общая масса микробных тел составляют 5-8 % массы тела ребенка.
Поджелудочная железа состоит из головки, тела и хвоста и выполняет две функции:
Печень у детей имеет относительно большие размеры и у новорожденных составляет около 4% массы тела, у подростков 2-3%. После рождения печень растет не интенсивно, ферментативной функции у нее практически нет. Воротная вена делит печень на правую и левую долю, которые состоят из 8 сегментов. Каждый сегмент имеет свою артерию, систему желчных протоков и образован из множества печеночных долек. Желчь образуется в печени и депонируется в желчном пузыре. В кишечник поступает при приеме пищи.
Желчный пузырь грушевидной формы с относительно большим объемом. У детей раннего возраста характерно внутрипеченочное его расположение и неинтенсивное желчеобразование. Желчь бедна желчными кислотами, холестерином, лецитином, солями и щелочью, но богата водой, муцином, пигментами и мочевиной. Она усиливает активность всех панкреатических ферментов, особенно липазы в 20 раз.
Обладает способностью эмульгировать жиры, оказывать бактерицидное действие на бактериальную флору кишечника и стимулировать его моторную функцию.
В пищеварительной системе, начиная с ротовой полости, расщепляются углеводы под действием амилолитических ферментов, активность которых у детей до 1 года невысока и постепенно увеличивается к 4-9 годам.
Белки расщепляются в желудке и в ДПК до аминокислот.
Расщепление пищевых жиров происходит под действием липазы, желудочного и поджелудочного соков до жирных кислот, которые всасываются в лимфу и через лимфатические сосуды попадают в системный кровоток.
Аминокислоты, моносахариды, витамины, минеральные вещества и вода всасываются непосредственно в кровь.
Для диагностики заболеваний ЖКТ у детей применяют различные методы исследования:
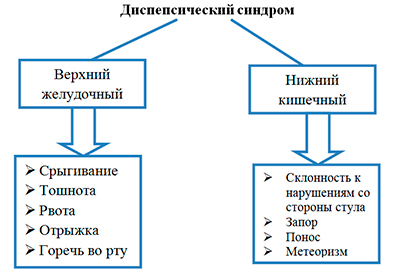
1)Клиническое обследование больного ребенка начинают с хорошо и подробно собранного анамнеза, начиная с рождения. Выясняют длительность заболевания, частоту обострений, проводимое лечение и характер жалоб. При жалобах на диспепсический синдром необходимо определить его характер.
Таблица №1
Затем проводят осмотр живота. Поверхностную и глубокую пальпацию желудка, кишечника, печени, селезенки. Обязательно обследуют болевые зоны, точки и пузырные симптомы, Проводят перкуссию и аускультацию живота.
2) Исследование испражнений и обследование ануса.
Оценку стула проводят на конечном этапе обследования ребенка методами опроса и осмотра. Выявляют частоту, характер каловых масс, а именно: цвет, консистенцию, примеси.
Нормальный стул у младенцев на естественном вскармливании 2-4 раза в день, желтый, неоформленный с ароматическим запахом.
На искусственном и после введения прикорма, стул 1-3 раза в день, бледно-желтый, сухой, крошкообразный.
У детей дошкольного и школьного возраста стул 1 раз в день, светло или темно-коричневый с запахом сероводорода, оформленный.
Состав кала при сбалансированном питании:
Твердые составляющие 20-25%.
Соли кальция и железа 10%.
Не переваренная клетчатка 45-70%.
Таблица №2
Характеристика стула здоровых детей
Группа детей
Частота
Цвет и запах
Консистенция
От рождения до 5го дня жизни (меконий и переходный стул)
Темно-зелёный; без запаха
Густой, вязкий, клейкий, неоформленный
На первом году жизни при естественном вскармливании
Золотисто-жёлтый, ароматический запах
После введения прикорма, при искусственном вскармливании
Бледно-коричневый, щелочной неприятный запах
Дети дошкольного и школьного возраста
Светло-,тёмно-коричневый, запах сероводорода
Для диагностики заболеваний ЖКТ оценка анализа кала дает основную информацию.
Таблица №3
Показатели копрограммы у здоровых детей
Показатель
Характеристика
Отсутствуют или встречаются отдельные переваренные волокна без исчерченности, у детей до 1 года могут быть непереваренные мышечные волокна
Отсутствует, у детей до 1 года- в незначительном количестве
Отсутствуют, у детей до 1 года- в незначительном количестве
Единичные клетки или клеточные группы. Содержится в разных количествах
Отсутствует, у детей до 1 года- в незначительном количестве
Патологическая копрограмма позволяет поставить предварительный диагноз заболевания у ребенка.
Таблица№4
Микроскопические исследования кала
Показатель
Характеристика
Креаторея: ахилия, хронический панкреатит, энтерит, запор, гнилостная и бродильная диспепсия
Жиры (нейтральный жир, жирные кислоты и мыла-соли жирных кислот)
Стеаторея I типа (увеличение нейтрального жира): панкреатическая недостаточность при хроническом панкреатите, панкреатолитаза
Стеаторея II типа (увеличение жирных кислот и мыл): моторные нарушения, дискинезия желчного пузыря, энтерит
Стеаторея III типа (увеличение всех жиров): муковисцидоз, целиакия, экссудативная энтеропатия, болезнь Аддисона, лимфогранулематоз
Амилорея: функциональная недостаточность поджелудочной железы, желудка, реже недостаточность слюноотделения, нарушения моторики тонкой кишки
Лиенторея: функциональная недостаточность поджелудочной железы, желудка, ускоренная перистальтика
Острые энтероколиты, колиты (кишечные инфекции)
Эритроциты, проба на скрытую кровь
Эрозивно-язвенные процессы, кишечные инфекции (дизентерия, сальмонеллёз), кровь скрытая: язвенная болезнь желудка и ДПК, новообразования
Прозрачная желатиновая слизь на поверхности оформленного кала: спастический запор, мукозный колит; кровянистая слизь: язвенный колит, дизентерия, злокачественные новообразования прямой кишки
Таблица№5
Копрологические синдромы
Синдром
Причины
Осмотр и микроскопия
Недостаточное пережёвывание пищи и ускоренное прохождение по ЖКТ
Непереваренные остатки пищи
Секреторная недостаточность желудка и поджелудочной железы
Реакция резко-щелочная, креаторея, лиенторея, кристаллы оксалатов, микроорганизмы
Выраженная функциональная недостаточность желудка и ДПК
Реакция слабощелочная, креаторея, лиенторея
Панкреатит, дуоденит, глистная инвазия
Испражнения жидкие, мазевидные, полифекалия желто-серого цвета, стеаторея I типа, креаторея
Холецистохолангит, аномалии развития желчных путей
Испражнения серого цвета, стеаторея I типа, отсутствие реакции на стеркобилин
Вирусный гепатит, атрезия желчных путей, иногда при дискинезии желчного пузыря
Ахоличный стул: стеаторея I типа, отсутствие реакции на стеркобилин
Энтерит при острых кишечных инфекциях
Стул жидкий, гомогенный, желтого цвета, эпителиальные клетки, стеаторея II типа, растворимые белки
Энтероколит при острых кишечных инфекциях
Испражнения со слизью, пенистые, с кислым запахом, лиенторея, амилорея, йодофильная микрофлора, лейкоциты, эритроциты
Колит при дизентерии, сальмонеллеза и других кишечных инфекциях
Испражнения со слизью, неоформленные (нередко “ректальный плевок”), пищевых остатков нет или незначительное количество, могут быть кровь, лейкоциты, эритроциты
При бактериологическом посеве кала в норме отсутствуют патогенные микроорганизмы. Полное представление о количественных и качественных изменениях флоры кишечника дает анализ кала на дисбактериоз.
Таблица №6
Качественный и количественный состав микрофлоры толстого кишечника у здоровых людей (КОЕ/г фекалий) Стандарт 2003г.
Микроорганизмы
Дети до 1 года
Дети после 1 года и взрослые
Пожилые люди
Грибы рода Candida
Стафилококки: сапрофитный, эпидермальный
Методы исследования органов пищеварения у детей.
Эзафагогастродуоденоскопия (ЭГДС): Она может быть плановая и экстренная.
Плановое обследование проводится натощак. Анестезия выполняется непосредственно перед исследованием орошением слизистой оболочки ротовой полости соответствующими лекарственными средствами. У детей старше 10 лет проводят психологическую подготовку.
Выявленные изменения при ЭГДС описываются в виде стандартизированного протокола. В течение одной процедуры последовательно осматривается пищевод, желудок, двенацатиперстная кишка и тонкая кишка. При необходимости можно получить биоптаты для дальнейшего исследования.
Лечебная эндоскопия проводится для санации слизистой оболочки, орошения ее лекарственными препаратами гемостатического, противоотечного, регенерирующего действия. С помощью эндоскопии удаляют инородные тела, проводят лучевую терапию, криотерапию. Существуют новые методы хирургической эндоскопии.
Ректороманоскопия – позволяет произвести осмотр слизистой оболочки прямой кишки и дистальных отделов сигмовидной кишки (20см). Используется на первом этапе исследования толстой кишки.
Колоноскопия проводится для исследования всех отделов тонкой и толстой кишки гибкими фиброколоноскопами.
Рентгенография органов пищеварения.
Обзорная рентгенография органов брюшной полости без контрастирования используется для диагностики врожденных аномалий, пороков развития ЖКТ, органических поражений органов пищеварения, осложнений язвенной болезни. Помогает уточнить локализацию инородного тела.
Ведущим методом исследования толстой кишки является ирригография с ретроградным введением бариевой взвеси после предварительной подготовки. С помощью ирригографии диагностируются опухоли, полипы, дивертикулы, пороки развития (долихосигма, мегаколон, болезнь Гиршпрунга идр) Можно выявить неспецифический язвенный колит, хронический колит, функциональные нарушения моторики толстой кишки.
Компъютерная томография — это усовершенствованный метод с высокой диагностической способностью всех органов ЖКТ без предварительной подготовки у детей старшего возраста.
Эхографическое исследование ЖКТ и печени (УЗИ) используется с первых дней жизни в связи с его безопасностью, высокой информированностью, широкой доступностью. Метод не имеет противопоказаний, безболезненный и занимает немного времени. Дает представление о размерах внутренних органов и их отделов, опухолевидных образованиях и аномалиях развития. Исследование кровотока в сосудах с помощью УЗИ называется допплерографией.
Функциональные исследования.
Начинают с 24-часовой рН метрии пищевода для диагностики функциональных срыгиваний при рН равным 4,0 и продолжительность менее 4 % общего времени мониторирования.
При гастроэзофагеальном рефлюксе (ГЭР) при рН менее 4.0 и продолжительность более 4,2 % общего времени мониторирования.
Внутриполостная рН-метрия желудка используется для определения кислотности внутрижелудочной среды. Для этого применяют зонды с 5 датчиками и замеры проводят непрерывно в течение 30 минут до стимуляции и в течении 1 часа после стимуляции (гистамини пентагастрин). В норме рН желудка составляет 1,5- 2,5.
Анализ рН- метрии желудка следующие:
— рН 1.5 и менее – гиперацидный гастрит;
— рН 6,0 – анацидный гастрит
Если в желудочном соке присутствует желчь, это свидетельствует о дуоденогастральном рефлюксе.
Дуоденальное зондирование — проводят для исследования желчи, отсасывания её и введения в ДПК лекарственных препаратов. Этот метод позволяет определить и тип дискенезии желчного пузыря, наличие холестаза и лямблиоза при микроскопическом исследовании желчи.
Таблица №7
Характеристика фракционного дуоденального зондирования
Фаза
Характеристика
Примечание
I-фаза общего желчного протока (холедохусфаза)
Период с момента появления первых порций желчи до введения раздражителя. Скорость выведения желчи- 1-1,5 мл/мин, время 15-20 мин, количество 20-30мл
При отсутствии желчи предполагают спазм сфинктера Одди или наличие механического препятствия оттоку желчи в дистальном отделе холедоха. Если получена пузырная желчь, верифицируют гиперкинетическую дискинезию желчного пузыря
По окончании выделения желчи через зонд медленно вводят 25% раствор магния сульфата, затем зонд перекрывают на 3 мин
II-фаза закрытого сфинктера Одди
Время от введения желчегонного раздражителя до появления новой порции желчи. Время 3-5 минут
При поступлении желчи до 3 мин после введения раздражителя-гипотония сфинктера Одди. Увеличение продолжительности фазы-спазм сфинктера Одди.
От момента открытия сфинктера Одди до появления темной пузырной желчи. Время – 3-5 мин, количество до 5 мл
Удлинение продолжительности этой фазы более 8 мин- сниженный тонус желчного пузыря или гипертонус сфинктера Люткенса
IV-пузырная фаза. Порция В
Время выделения густой темно- оливковой желчи. Скорость выделения – 2-3 мл/мин, время-20-30 мин, количество-30-50мл
V-печеночная, порция С
Скорость выделения желчи золотисто-желтого цвета из печеночных ходов – 1-1,5 мл/мин
Функциональную диагностику экзокринной функции поджелудочной железы проводят по определению в крови:
1) α-амилазы крахмала по Каравею (норма 12-32 мг /мл);
2) Липазы (менее 160 БД/мл);
3) Трипсина (10-60 мкг/л) радиоиммунологическим методом;
В моче определяют α-амилазу по Каравею (норма 28-160 мг/мл), по Велгемуту (норма 16-64 БД)
В кале определяют эластазу-1 (норма 200 мкг/час)
Переваривающую функцию тонкой кишки определяют по исследованию:
1) Активности ферментов в кишечном соке и кале энтерокиназы и щелочной фосфатазы
2) Нагрузочных проб дисахаридами (лактозой или сахарозой) из расчёта 2гр/кг массы тела проводят с первых недель жизни для диагностики лактазной недостаточности у младенцев. Содержание глюкозы в крови натощак, на 15й, 30й и 60й минутах. Восходящая часть гликемической кривой говорит о всасывательной функции тонкой кишки, нисходящая – утилизация и депонирование поступивших углеводов. Уровень глюкозы в крови в норме увеличивается не менее чем на 20 % от исходного (-1,1 ммоль/л) в течение 60 минут после нагрузки
3)Наличие в кале или в моче дисахаридов говорит за дисахаридазную недостаточность у детей.
Для диагностики муковисцидоза используется потовая проба, которая дает точные результаты. Собирается пот с помощью ионофореза, пилокарпина и слабого электрического тока, который стимулирует потовые железы. Определяют концентрацию ионов натрия и хлора. Для достоверности, пробу повторяют 2-3 раза. У здоровых детей концентрация натрия и хлора не превышает 40 ммоль/л, но повышение до 60-80 ммоль/л подтверждает диагноз муковисцидоза. В последнее время внедрены в практику аппараты «Макродакт» и «МВ-индуктор» для скрининг диагностики муковисцидоза в условиях амбулаторной практики.
Диагностическое значение имеет определение эластазы-1 в каловых массах и сыворотки крови при подозрении на муковисцидоз. Норма более 500 мкг/г стула, а снижение показателей свидетельствует о панкреатической недостаточности, что имеет место при муковисцидозе. Значение уровня эластазы-1 помогает подобрать дозу заместительных панкреатических ферментов и чем ниже показатели, тем выше их суточная доза. Если уровень эластазы-1 выше 200 мкг/г стула, необходимость в панкреатических ферментах отпадает.
Причиной срыгиваний может быть аэрофагия. В этом случае необходимо внести поправку в технику кормления и прежде всего, чтобы ребенок правильно захватывал сосок при грудном вскармливании. При искусственном – контролировать диаметр отверстия в бутылочке. При частых и обильных срыгиваниях целесообразно увеличить число кормлений на 1-2 в сутки, одновременно уменьшив разовый объем пищи.
Важная роль в лечении регургитации отводится диетотерапии, которая зависит от вида вскармливания.
При естественном вскармливании прежде всего необходимо создать дома спокойную обстановку для кормящей матери, что сохраняет хорошую лактацию. Необходимо нормализовать режим кормления, исключить перекорм и аэрофагию. Известно, что срыгиванияу ребенка могут быть проявлением пищевой непереносимости у матери, и в этом случае ей назначается гипоаллергенная диета.
При синдроме нервно-рефлекторной возбудимости вследствие перенесенного перинатального поражения ЦНС диетическая коррекция должна сочетаться с медикаментозным лечением, которое назначает детский невропатолог.
При отсутствии эффекта при упорных срыгиваниях используются смеси- загустители (антирефлюксные смеси АРС). Для повышения вязкости в этих смесях используются специальные загустители: клейковина бобов рожкового дерева-камедь и модифицированные крахмалы (рисовый, кукурузный или картофельный). Это 2 полисахарида, клиническая эффективность и безопасность которых проверена десятилетиями.
Наиболее эффективной является камедь из рожкового дерева, которая относится к пищевым волокнам. Она устойчива к воздействию панкреатической амилазы и дисахаридаз тонкой кишки, но активно ферментируется полезной микрофлорой толстой кишки и прежде всего бифидобактериями.
В результате этого камедь приобретает пребиотические свойства. В частности возрастает содержание бифидобактерий, pH кишечника сдвигается в кислую сторону и улучшается трофика клеток кишечного эпителия. Всё это создаёт условия для подавления условно-патогенной кишечной микрофлоры и улучшает её состав.
При грудном вскармливании АРС назначаются в небольшом объеме (20-40 мл) перед кормлением грудным молоком.
При искусственном вскармливании и упорных срыгиваниях базисная адаптированная смесь сочетается с АРС, частично в количестве 1/3-1/2 от необходимого объема в каждое кормление, с которой начинают кормить ребенка, а заканчивают базисной смесью. Редко АРС дается в полном суточном объёме кормления. Продолжительность применения смесей определяется индивидуально, но чаще всего около 2-3 месяцев. Только после достижения стойкого терапевтического эффекта ребенок переводится на свою адаптированную смесь. Несмотря на то, что АРС являются полноценными по составу и обеспечивают физиологические потребности ребенка в пищевых веществах и энергии, они относятся к лечебным смесям. Поэтому используются строго при наличие клинических показаний по рекомендации педиатра.
После введения прикормов необходимость в АРС отпадает.
При синдроме срыгивания медикаментозная терапия применяется редко и в основном это препараты группы Домперидона. Оригинальным препаратом является «Мотилиум». Для детей грудного возраста может использоваться суспензия 1 мгв /мл.рекомендуемые дозы составляют 0,025-0,5мл на 1 кг массы тела 3-4 раза в день до еды. Курс лечения зависит от эффекта.
Младенческие колики
К числу функциональных расстройств в ЖКТ у детей грудного возраста относятся кишечные колики, которые занимают лидирующее положение в структуре заболеваний органов пищеварения этого возраста (по разным данным 90-95%). Это эпизоды болезненного плача, которые получили название «правило трёх». Продолжительность не менее 3 часов, не реже 3 дней в неделю и не менее 3 недель. Коликами называются приступообразные боли в животе с выраженным беспокойством ребенка, покраснением лица, прижатыми ножками к животу и недостаточным отхождением газов и стула. Младенческие колики рассматриваются как «условно» физиологическое состояние периода адаптации и созревания ЖКТ у ребенка грудного возраста. Как правило кишечные колики возникают у младенцев к началу 3й недели жизни, достигают кульминации в возрасте 3х месяцев и постепенно уменьшаются, обычно исчезает в 4 или 5 месяцев. Наиболее типичное время для колик это вечерние часы. Длительность от 10 мин до 3 ч. В зависимости от степени тяжести они делятся на 3 формы:
Состояние улучшается после отхождения газов или стула. Несмотря на то,что приступы колик повторяются часто и довольно длительное время, общее состояние ребенка не страдает и остается хорошим. Между приступами, младенец ведет себя спокойно. Сохранен хороший сосательный рефлекс и нормальная прибавка в весе и росте.
Механизмы развития кишечных колик предполагают участие нескольких факторов:
Предрасполагающими факторами со стороны матери – являются: нарушение питания кормящей матери, вредные привычки, стрессы, депрессии и прием некоторых лекарственных препаратов.
Курение матери во время беременности и после родов увеличивает риск возникновения колик у ребенка в 2 раза. Распространенность колик не связана с социально-экономическим статусом семьи и уровнем материального обеспечения.
Предрасполагающими факторами со стороны ребенка являются недоношенность, незрелость к сроку гестации, внутриутробные инфекции.
К пищевым факторам возникновения младенческих колик относятся нерациональное вскармливание, перекорм, насильственное кормление, аэрофагия. Имеет значение и быстрый переход на искусственное вскармливаниеи неправильное разведение смесей. Кроме того нарушение питания со стороны кормящей матери могут явиться причиной колик у младенца.
Нарушение моторики кишечника связано с незрелостью нервно-мышечного аппарата кишечника и нарушением центральной регуляции. Кишечник имеет собственную нервную систему и при растяжении гладких мускулатур происходит стимуляция афферентных нейтронов и передается возбуждение вегетативную нервную систему, которая принимает участие в регуляции моторики кишечника и секреции. Дисбаланс в работе вегетативной нервной системы сопровождается нарушением регуляции в магистральных артериях головы, что усугубляет церебральную гипоксию. На фоне этого запускается механизм «вегето-висцерального порочного криза», составной частью которого являются функциональные моторные нарушения, а именно колики.
Ферментативная недостаточность. Известно, что к моменту рождения у большинства детей имеет место относительная незрелость ферментативных систем ЖКТ. Впервые недели жизни переваривание происходит за счет ферментов грудного молока в присутствии аутолитического компонента. Этим частично компенсируется недостаточность полостного пищеварения у младенцев. Экзокринная функция поджелудочной железы относительно незрелая, но все-таки обеспечивает гидролиз пищевых веществ, содержащихся в молоке. Процессы мембранного пещеварения осуществляются ферментами энтероцитов и панкреатического сока. Однако довольно часто возникает незрелость дисахаридаз и в частности лактозы, что и является причиной парентерального синдрома с кишечной коликой у детей первых недель жизни независимо от вида вскармливания. Лактоза- это молочный сахар, которая содержится в любом животном молоке, в том числе и в адаптированных молочных смесях. Хочется отметить, что в кисломолочных продуктах лактозы содержится значительно меньше.
В целом созревание ферментативных процессов переваривания происходит к 3месяцам. Однако у недоношенных и незрелых детей этот процесс затягивается.
Пищевая непереносимость- одна из частых причин кишечных колик у грудных детей. Это прежде всего непереносимость белков коровьего молока, которая может быть обусловлена как иммунными, так не иммунными механизмами.
Другой алиментарной причиной младенческих колик может быть лактазная недостаточность. Часто она имеет транзиторный характер в результате незрелости или повреждения кишечного эпителия. Колики возникают в результате повышенного образования водорода в кишечнике из-за бактериального брожения нерасщепленной лактозы. Газы растягивают кишку, возникает боль, а незрелость регуляции моторики способствует нарушению его выявления наружу. Диагностическим тестом является определение водорода в выдыхаемом воздухе у детей первых месяцев, концентрация которого будет повышена при лактазной недостаточности. К 3-4 месячному возрасту улучшается усвоение лактазы и колики проходят.
Обзор современных литературных данных свидетельствует о том, что младенческие колики характеризуются обратным самостоятельным развитием и лечение предусматривает работу с родителями, а при необходимости назначаются лекарственные препараты с учетом их безопасности и эффективности для уменьшения беспокойства ребенка.
Нарушение микробиоценоза кишечника. Нормальный микробиоценоз кишечника является основой здоровья ребенка. Полноценная кишечная флора выполняет много эссенциальных функций в организме:
1) Подавляет рост и размножение патогенной и условно-патогенной флоры;
2) Оказывает иммуномодулирующее действие;
3) Определяет моторную функцию кишечника;
4) Формирует пищевую толерантность;
5) Принимает участие в пищеварении;
6) Участвует в регуляции обмена минералов;
7) Синтезирует витамины группы В и К;
8) Оказывает метаболическое действие.
В результате бактериального расщепления пищевых веществ образуются газы и короткоцепочечные жирные кислоты. Избыточное газообразование приводит к младенческим коликам. Выраженность последних связана еще и с увеличением общего количества условно-патогенных микроорганизмов семейства Enterobacteriaceae. Это свидетельствует о дисбактериозе, что способствует развитию воспалительных изменений в слизистой оболочке кишечника. Нарушается моторика и повышается проницаемость слизистой оболочки. Важным фактором нормального развития местных и системных иммунных реакций является остаточная колонизация кишечника лактобациллами Acidophilea. Этот факт используется для внесения их в молочные смеси и другие продукты питания для младенцев. В тоже время увеличение отдельных видов лактобактерий (brereis и lactis) в кишечнике может вызвать метеоризм и брожение, что способствует возникновению колик. Значимость кишечной микрофлоры подтверждается и тем фактом, что колики возникают в период интенсивного становления кишечного биоценоза, когда флора наиболее уязвима, неустойчива и подвержена различным влияниям.
Лечение.
Основным принципом лечения детей с коликами является пошаговая терапия.
При смешанном и искусственном вскармливании ребенку необходимо подобрать адаптированные молочные смеси, имеющие лечебно-профилактическую направленность, содержащие пробиотики, пребиотики, нуклеотиды. Эффективным может быть использование гипоаллергенных, низколактозных или безлактозных смесей.
Прежде всего это укропная вода и фитосборы на основе ромашки, фенхеля, мелиссы, вербены, мяты перечной, которые обладают ветрогенным действием. Эти препараты стимулируют пищеварительные процессы, секрецию желудочного сока, усиливают перистальтику кишечника, способствуя отхождению газов и оказывают мягкий спазмолитический эффект. Особое место занимают препараты на основе симетикона – это высокомолекулярный полимер диметикон, активированный двуокисью кремния.
Это вещество оказывает ветрогенное действие, ослабляет поверхностное напряжение пузырьков газа в кишечнике, разрывает их на мельчайшие пузырьки с последующим выведением их из организма. Симетикон не всасывается, не влияет на процесс пищеварения и выводится из организма в неизмененном виде, не вызывая к нему привыкания. Давление газов в просвете кишечника снижается и купируется болевой синдром колик. Симетикон образует защитную пленку на слизистой оболочке ЖКТ, которая нейтрализует действие агрессивных факторов. К препаратам, содержащих симетикон относятся боботик, эспумизан, коликвел, которые могут использоваться с первых недель жизни и длительно, не оказывая побочных проявлений.
При избыточном газообразовании целесообразно назначение энтеросорбентов.
Препараты ферментов поджелудочной железы, а чаще всего рекомендуется в детском возрасте микрогранулированные препараты с активностью липазы 10000 ед в капсуле. Назначается только при копрологических признаках, свидетельствующих о нарушении экзокринной функции поджелудочной железы. Курс лечения от 10 дней до 1 месяца.
Из отвлекающих средств купирования младенческих колик у младенцев используют тепло на животик и масляные компрессы.
Функциональные запоры.
Это состояние относится к числу распространенных нарушений функции кишечника и выявляются у 20-35% детей первого года по данным литературы. Под запорами понимают нарушение дефекации, что проявляется увеличением интервалов между актами дефекации по сравнению с индивидуальной физиологической нормой более 36 часов или систематически неполным опорожнением кишечника. Частота стула у детей считается нормальной, если в возрасте от 0 до 4 месяцев происходит от 7 до 1 актов дефекации в сутки, от 4 месяцев до 2 лет- от 3 до 1 и старше 2 лет от 2 до 1 раза в 2 дня.
К диагностическим критериям запоров относятся следующие:
1)удлинение интервалов между актами дефекации более чем на 32-36 часов;
2) длительный период натуживания (менее 25% от общего времени дефекации);
3) консистенция кала плотная, или в виде комочков;
4) чувство неполного опорожнения кишечника у детей, начиная с раннего возраста.
Возникновение запоров чаще обусловлено дискинезией толстой кишки (гипо- и гипермоторными нарушениями), болезненным спазмом сфинктера прямой кишки, ослаблением тонуса гладкой мускулатуры или сочетанием этих факторов. В некоторых случаях возникновение запоров у детей раннего возраста может быть связано с аномалиями развития толстой кишки. К факторам риска развития запоров у детей первого года жизни относятся раннее искусственное вскармливание, перинатальное поражение ЦНС, недоношенность, морфофункциональная незрелость новорожденного, дисбиоз кишечника и отягощенная наследственность по желудочно-кишечным заболеваниям. У детей первого года жизни запоры являются результатом алиментарных нарушений. Но по этиологии еще выделяются такие виды запоров, как неврогенный, психогенный, эндокринный, воспалительный, инфекционный (после перенесенной инфекции). Употребление противосудорожных, мочегонных средств, препаратов железа и кальция могут сопровождаться запорами. Лечение функциональных запоров у детей первого года жизни включает в себя диетотерапию и при необходимости медикаментозное лечение.
Основные принципы диетотерапии функциональных запоров у детей первого года жизни:
1) Удовлетворение физиологических потребностей ребенка в пищевых веществах и калориях;
2) Исключение избыточного потребления белков и жиров, которые тормозят моторику кишечника;
3) Обогащение рациона пищевыми волокнами;
4) Нормализация кишечной микрофлоры.
Назначение диетотерапии зависит от вида вскармливания. У детей на грудном вскармливании необходимо исключить недокорм. Провести коррекцию пищевого рациона кормящей женщины ограничением продуктов с высоким содержанием животных жиров, но включая в рацион растительные масла. В рацион кормящей женщины вводить продукты, стимулирующие моторику кишечника, так как имеет место прямая корреляция между возникновением запоров у детей и их матерей. Для этого используются кисломолочные продукты, продукты с высоким содержанием пищевых волокон (овощи, фрукты, сухофрукты, гречневая, овсяная, кукурузная крупы, хлеб из муки грубого помола). Имеет значение соблюдение питьевого режима как у матери, так и ребенка.
Медикаментозное лечение.
Включает в себя применение слабительных средств, регуляторов моторики ЖКТ, препаратов размягчающих каловые массы. Из слабительных средств чаще назначаются препараты лактулозы. Ферменты тонкой кишки не разлагают лактулозу и препарат поступает в толстый кишечник, где расщепляется под действием микрофлоры. Оказывает бифидогенный эффект, увеличивая объем каловых масс и способствует их размягчению. Дозы выбираютя индивидуально в зависимостиот от веса и возраста. Назначают по 0,5-1,0мл на кг веса у детей до 1 года 1 раз в день натощак. Эту дозу можно разделить на 2 приема. Отменяют препарат постепенно, уменьшая объем разовой дозы, а затем- кратность приема по 5 мл 2-3 раза в неделю. Курс лечения 1-2 месяца.
Средства размягчающие каловые массы:
1)вазелиновое масло до 1 года ½-1ч.л. 1 раз в день, с 1г до 3 лет- 10мл 1 раз в день
2)желчегонные препараты (хофитол) на 2-4 недели
У детей с проктогенными функциональными запорами используют средства для ректального применения:
1) у детей грудного возраста свечи облепиховые 1 раз в день, курс лечения 10 дней;
2) глицериновые свечи у детей раннего возраста по 6 ной 1 раз в день, курс 10 дней;
3) микроклизмы с 2 летнего возраста.
Детям не показаны слабительные раздражающего действия (препараты сены, крушины, ревеня) и комбинированные слабительные.
В комплексную терапию запоров включаются пробиотики, пребиотики нормализующие микрофлору кишечника.
Функциональные диареи.
Это состояние не связано с каким-либо органическим поражением ЖКТ и не сопровождаетя болевым синдромом. Детям до 1 года такой диагноз не ставится. В более старшем возрасте функциональный характер диареи подтверждается не увеличением объема стула, а изменением его характера. Стул может быть жидким или кашецеобразным более 2 раз в день, сопровождающийся усиленным газообразованием и императивными позывами на дефекацию. Если диарея продолжается более 3 недель, она считается хронической и требует лечения для предупреждения развития энтероколита с поражением энтероцитов и формированием дисбактериоза.
В настоящее время в лечении всех видов диарей новым является использование прупаратов цинка, что связано с его уникальными свойствами:
3) репаративное (восстанавливает щеточную кайму в тонком кишечнике и ускоряет регенерацию энтероцитов);
4) укрепляет и стимулирует иммунитет;
5) антиоксидантное действие за счет утилизации свободных радикалов;
6) цитопротективное действие- защищает мемраны клеток от вредных веществ или реакций;
7) снижает риск проникновения аллергена из кишечника далее в организм, расщепляет аллергены в кишечнике, укорачивает и ослабляет течение аллергии;
8) выводит из организма аллергены, токсины и другие вредные вещества;
9) восстанавливает пищеварение в кишечнике и стул; является важным питательным микроэлементом для синтеза белков, роста клеток, транспорта воды и электролитов в кишечнике.

Ценность этого прапарата заключается сочетанием цинка с пробиотиками (бифидобактерии и лактобактерии), которые обеспечивают здоровое функционирование энтероцитов и нормализуют микрофлору кишечника. 1 грамм препарата содержит цинка сульфата 15,54мг и полезных бактерий 3х10 9 КОЕ+ целлюлоза и крахмал кукурузный или картофельный.
У нас накоплен довольно большой опыт применения “Bifolak ® -Цинкум” при целиакии, дисбактериозе и гастроинтестинальной форме пищевой аллергии и был выраженный клинический эффект практически у всех детей. Эффективность выражалась уменьшением частоты стула, улучшением консистенции и ликвидации болевого синдрома в кишечнике. Достоверно отмечалось улучшение процессов пищеварения и общего состояния детей.
Использовался способ применения:
— До 1 года- по ½ или 1 пакетику 1 раз в день
-От 1 года до 5 лет по 1 пакетику 2 раза в день
-От 5 до 12 лет- по 1 пакетику 2 раза в день
Курс лечения составлял 10 дней.
1) У детей с синдромом срыгивания в определенном проценте случаев в старшем возрасте может развиться гастроэзофагальный рефлюкс или гастроэзофагальная рефлюксная болезнь;
2) Младенческие колики могут явиться причиной развития синдрома раздраженной кишки по типу диареи или запоров;
3) Среди детей, перенесших младенческие колики в возрасте 2-3 лет наблюдаются негативные варианты поведения.
Таким образом, частота функциональных нарушений ЖКТ у детей грудного и раннего возраста по литературным данным колебнется от 30 до 70%, что свидетельствует о важности этой проблемы. В данных методических рекомендациях мы изложили все многообразие клинических проявлений, лечебные мероприятия, включая работу с родителями, диетотерапию и медикаментозные средства. Очень важно оценить прогностическое значение каждого функционального расстройства для дальнейшего развития патологии пищеварительного тракта. Выбор правильного решения в построении лечебной программы должен быть творческим, индивидуальным и всегда начинаться с вопроса- почему, как и зачем.
Собственные наблюдения:
Под нашим наблюдением в течение 10 лет находилось достаточное количество детей с функциональными нарушениями желудочно-кишечного тракта. Обобщая наши данные, наиболее частыми проявлениями были младенческие колики и синдром срыгивания. Реже встречались функциональная диарея и запоры. Возраст детей был от 1 мес до 1,5 лет. Диагноз ставился на основании анамнеза матери, ребенка, клинических проявлений, лабораторных исследований.
Лечение проводилось поэтапно и прежде всего это диетотерапия со стороны матери при младенческих коликах и запорах. При искусственном вскармливании индивидуально детям подбирались адаптированные смеси, такие как безлактозные, кисломолочные или гипоаллергенные. Часто параллельно диетотерапии при младенческих коликах назначались препараты симетикона.
При синдроме срыгивания прежде всего были рекомендованы рекомендации по правильной технике грудного кормления и постурального положения ребенка. При отсутствии эффекта патологического синдрома срыгивания 10% детей были переведены на антирефлюксные смеси в количестве 1:1 с грудным молоком или базисной смесью. В единичных случаях использовалась суспензия мотилиума на 8-10 дней.
Особое значение имела диетотерапия матери при запорах у детей. Назначалась диета №3 с использованием продуктов, стимулирующих перистальтику кишечника. Детям с 5-6 месяцев назначались прикормы в виде соответствующих соков, фруктовых и овощных пюре, а из каш использовалась кукурузная. Из медикаментозных средств применялся прежде всего дюфалак в соответствующих дозах до 1-1,5месяцев. Нередко диетотерапия оказывалась эффективнее медикаментозного лечения. Рекомендовались теплые компрессы на живот или теплая грелка. Рекомендовались облепиховые свечи детям до 1 года, а старше- глицериновые курсом от 8 до 10 процедур. При функциональной диареи у детей старше года было нарушение диеты у матери, если ребенок еще кормился грудью, соответственно давались рекомендации. При наличии стеатореи у детей проводилась заместительная терапия ферментами, пробиотиками и пребиотиками. Учитывая значение цинка при функциональной диарее мы использовали отечественный препарат “Bifolak ® -Цинкум”, содержащий и пробиотики (бифидо- и лактобактерии). В 1 гр. цинка 15,54мг и пробиотиков более 3 х10 9 КОЕ. Курс лечения составил 10 дней по 1 саше 1 раз в день. Эффективность характеризовалась уменьшением частоты стула и улучшением его качества, хорошим состоянием, аппетитом и исчезновением дискомфорта в животе.
Таким образом, только количественный подход к лечению функциональных расстройств ЖКТ включая диетотерапию матери и ребенка, обучение правильной технике грудного вскармливания и часто в сочетании с медикаментозными средствами приводит к положительным результатам и коррекции их состояний.
Литература.
1) Авдеева Т.Г. с соавт. «Детская гастроэнтерология» ГЭОТАР-медиа Москва 2011г.
3) Бельмер С.В. с соавт «Функциональные нарушения органов пищеварения у детей: Библиотека врача специалиста» М.-2018г. 244 с.
4) Грибакин С.Г., Давыдовская А.А. Минимальные пищеварительные дисфункции у детей грудного возраста и их диетологическая коррекция. «Педиатрия» 2011г. Т90. №4 с.73-76.
5) Таран Н.Н. Функциональная диспепсия у детей раннего возраста. «Вопросы практической педиатрии 2012г. Т 7. №1. с 76-80».
6) Приворотов В.Ф., Лупова Н.Е. Кишечные колики у детей раннего возраста: Проблемы и пути решения. Педиатрия 2012г. Т91. № 4. с 98-104.
7) Кильдиярова Р.Р., Лобанов Ю.Ф. Наглядная детская гастроэнтерология и гепатология. Москва 2013г.
8) Лебедева У.М., Кириллина С.А. Клиническая оценка эффективности диетотерапии при функциональных нарушениях пищеварения у детей. «Вопросы практической педиатрии 2014г. Т9. №6. с66-74».
9) Мельникова И.Ю. «Детская гастроэнтерология» ГЭОТАР-медиа Москва 2018г.
10) Эрдес С.И., Мухаметова Е.М. Функциональные расстройства верхних отделов пищеварительного тракта у детей раннего возраста: возможности практической педиатрии 2012г. Т7. №5. с19-24.