Что такое фкд 2 типа
Фокальная корковая дисплазия

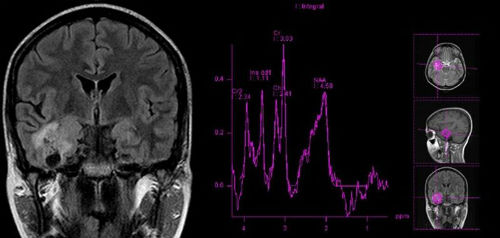
Диагностика заболевания проводится врачом неврологом на основании результатов ЭЭГ, МРТ и ПЭТ исследования. Консервативное лечение данной патологии проблематично, ввиду ее высокой устойчивости к противоэпилептической терапии. В тяжелых случаях может быть показано полное удаление пораженного участка мозга.
Фокальная корковая дисплазия – развивается во внутриутробном периоде и проявляется в виде патологий, локализующихся в отдельных участках мозговой оболочки. ФКД является самым распространённым фактором, провоцирующим появление эпилепсии у детей (по некоторым данным ФКД наблюдается у тридцати процентов детей больных эпилепсией).
Особенности, позволяющие отличить ФКД от обычной эпилепсии, является:
Большинство патологий при ФКД локализуется в височной и лобной долях. Патологические поражения очень плохо визуализируются, что значительно усложняет проведение МРТ диагностики.
Причины возникновения заболевания
Возникновение ФКД обуславливается внутриутробными нарушениями в развитии церебральной коры, что обуславливает нарушения миграции клеток мозговой оболочки, образуя участок с аномально развитыми нейронами. Формируется ФКД на конечной стадии беременности, приблизительно за шесть недель до родов.
Из-за того, что у некоторых групп пациентов при обследовании были найдены рецессивные дефекты в структуре гена TSC1, нельзя полностью исключить генетическую причину развития заболевания. Большинство современных научных исследований ведется именно в этом направлении.
Усилия ученых сконцентрированы на разработке методик:

Согласно данному классификатору ФКД бывает:
Симптомы заболевания
Главным симптомом, опираясь на который можно диагностировать наличие у пациента корковой дисплазии является – краткосрочные эпилептические приступы. Манифестирует заболевания рано, часто еще до достижения пациентом 5 лет.
Приступы заболевания сложные (сопровождающиеся расстройством поведенческих реакций), интенсивные (осложняются потерей равновесия и возникновением спонтанных двигательных реакций) и кратковременные (редко длятся дольше одной минуты). В раннем возрасте при отсутствии должного лечения провоцируют развитие аутизма.
Симптоматика ФКД напрямую зависит от ее типа, локализации, выраженности симптомов, наличии осложнений и заболеваний, провоцирующих ее появление. Ранняя манифестация в большинстве случаев отягчается задержкой психического и умственного развития.
Симптомы дисплазии первого типа менее выражены, однако, в некоторых случаях данный тип ФКД может провоцировать ухудшение когнитивных способностей у пациента.
Симптомы дисплазии второго типа намного более выражены, чем первого. ФКД данного типа сопровождается возникновением тяжелейших эпилептических припадков.
Симптомы дисплазии третьего типа напрямую зависят от характера основного заболевания.
Диагностика заболевания
Главным диагностическим методом, позволяющим определить наличие ФКД, является – МРТ диагностика, которая, однако, должна производиться согласно специальному диагностическому протоколу. Толщина среза, согласно которому не должна превышать полутора миллиметров. Только столь тщательное сканирование позволяет выявить даже самые минимальные изменения в коре.
В процессе диагностики значение имеет квалификация и опыт врача рентгенолога, из-за чего интерпретация результатов должна вменяться в обязанность исключительно специалисту.
Проведение МРТ исследования позволяет выявить следующие признаки наличия ФКД:
Каждый вид ФКД имеет спектр характерных именно для него симптомов. Уточнить данные полученные при прохождении МРТ позволяет проведение электроэнцефалографии, позволяющей выявить наличие локальной эпилептической активности, не только в момент эпилептического припадка, но и в период после него. Во время приступа отмечается активация участков мозга, расположенных в зонах локализации дисплазии. Данная закономерность объясняется наличием за пределами основной локализации дисплазии аномальных мозговых клеток.
Также обозначить зоны локализации дисплазии можно при помощи ПЭТ диагностики, дополненной МРТ исследованием. Однако у данного диагностического метода существует один значительный нюанс, ПЭТ исследование позволяет локализовать дисплазию только в период эпилептического припадка (контрастное вещество должно быть введено в организм пациента исключительно после первого пароксизмального заряда). Данный вид диагностики особенно ценен, в случае если МРТ диагностика не дала четких и однозначных результатов. Для получения более точного результата может применяться электрокортикография.
Терапия
Лечение больного курируется врачом неврологом, совместно с врачом эпилептологом. Лечение начинается с выбора и определения эффективной дозировки противосудорожного препарата. С данными целями может использоваться карбамазепин, диазепам, леветирацетам, топирамат и препарат вальпроевой кислоты. В большинстве случаев эпилепсия, отягощенная ФКД, оказывается крайне устойчивой к какому-либо противосудорожному лечению.
В указанном выше случае должен быть поставлен вопрос о хирургической резекции пораженного участка. Оперативное лечение проводится исключительно врачом нейрохирургом, совместно с неврологом. В связи с тем, что дисплазия носит фокальный характер, оперативное лечение является эффективным.
Многие специалисты настаивают на целесообразности как можно более полного и радикального удаления пораженного мозгового участка. Данное утверждение спорно, потому что локализация клеток, расположенных вокруг основного очага поражения достаточно обширна, а их полное удаление без нанесения значительного вреда пациенту невозможно.
В зависимости от тяжести симптомов, их локализации и размера пораженного участка может быть использован один из трех вариантов хирургического лечения:
При ФКД третьего типа целесообразно удаление, как самого участка дисплазии, так и главного очага поражения.
Прогноз развития заболевания

Возникновение заболевания в детском возрасте может спровоцировать проявление отклонений в развитии, с постепенным развитием олигофрении.
Оперативное лечение является результативным, при одиночном очаге поражения. Практически у половины пациентов возобновления заболевания не наблюдается. Однако через десять лет после оперативного вмешательства стойкая ремиссия наблюдается только у трети пациентов. Скорее всего, рецидив заболевания в данном случае связывается с неполным удалением поврежденного сегмента.
Возникновение рецидива заболевания непосредственно после проведенного оперативного вмешательства наблюдается приблизительно у двух пациентов их ста, а в случае распространенного поражения, рецидив наступает у шести пациентов из ста прооперированных.
Риск рецидива увеличивается, в случае если оперативное вмешательство проводилось вблизи функционально важных участков головного мозга.
Что такое фкд 2 типа
Пороки развития коры (ПРК), также известные, как нарушения нейрональной миграции или кортикальная дисплазия, включают гетерогенную группу заболеваний в результате изменения трех эмбриологических периодов, происходящих между 8-й и 16-й неделями внутриутробной жизни: клеточная пролиферация зародышевых листков, миграция нейронов и организация клеток в коре головного мозга.
Такой измененный кортикогенез может быть генетически детерминированным или возникнуть в результате экзогенной травмы (внутриутробные и/или даже перинатальные причины), хотя его этиопатогенез часто неясен. Сложный и многофакторный этиопатогенез пороков развития коры (ПРК) объясняется их возможную связь с некоторыми неврологическими синдромами.
Пороки развития коры (ПРК) являются одними из ведущих причин детской ФРЭ (до 40% детей с ФРЭ и половина из тех, кто подвергается хирургическому лечению эпилепсии при воздействии ПРК). Даже если электрокортикография демонстрирует эпилептизацию диспластической коры, внутренние механизмы начала припадков по-прежнему остаются практически неизвестными. Последние молекулярные исследования на животных и человеческих клетках указывают на роль NMDA и АМРА-рецепторы глутамата.
Различные формы порока развития коры (ПРК) отличаются макроскопически, но имеют ряд общих микроскопических особенностей, как серого, так и белого вещества. Они включают:
1. Кортикальную деламинацию (корковая ламинарная и столбчатая дезорганизация).
2. Плохую дифференциацию серого/белого вещества.
3. Отсутствие миелинизации.
4. Глиоз.
5. Микроскопическая нейрональная гетеротопия (островки неправильно расположенных нейронов).
6. Волокона Розенталя (периваскулярные эозинофильные тельца и волокна в результате дегенерации астроглии).
7. Баллонные клетки (аномальные и сильно увеличенные в размере клетки, со стекловидной и эозинофильной цитоплазмой и эксцентричным ядром, имеющие иногда положительный ответ на глиальные маркеры, а иногда и на нейронные).
8. Гигантские нейроны (увеличение размеров нейронов с центральными ядрами и нормальной морфологией).
9. Незрелые нейроны (нормального размера, круглой формы и однородными нейронами, с большим и незрелым ядром, небольшой цитоплазмой и нормальной морфологией).
10. Дисморфоз нейронов (нервные клетки с аномальным размером, формой, ядром, цитоплазмой и дендритами, имеющие тигроид и цитоплазматические нейрофиламенты).
Порок развития коры (ПРК) может включать в себя только некоторые области коры (фокальная корковая дисплазия) или несколько долей (квадрантная дисплазия) до целого полушария (гемимегалэнцефалия).
а) Очаговые пороки развития. Фокальная кортикальная дисплазия (ФКД). ФКД является локализованным ПРК, наиболее часто связанным с ФРЭ в детском возрасте. Она включает в себя целый спектр изменений, начиная от легкой корковой деструкции до более тяжелых форм. По данным Palmini et al., она может быть разделена на два типа. Тип IA/B нелегко обнаружить при МРТ, его клиническая картина варьирует от отсутствия эпилепсии до ФРЭ и когнитивных нарушений. Тип ПА/В, как правило, хорошо распознается при МРТ (см. ниже), часто связан с плохо поддающейся лечению и катастрофической эпилепсией, и имеет, соотвественно, худший прогноз.
Приступы и неврологические симптомы варьируют в зависимости от расположения ФКТ, которая, как правило, имеет вневисочную локализацию (и часто располагается около роландовой борозды). Фокальные двигательные припадки и генерализованный эпилептический статус, о которых сообщается в 30% случаев в детстве и подростковом возрасте, с течением времени становятся более отягощенными. Раннее начало припадков связано с худшими результатами и более высокой частотой неврологических нарушений и умственной отсталости. Сенсорно-моторный дефицит описывается у 50-75% пациентов, у половины из которых уровень IQ ниже 80.
Паттерны ЭЭГ обычно состоят из изолированных эпилептиформных разрядов и фокальных замедлений, часто вовлекая более протяженные участки мозга, чем анатомические границы патологического очага, и /или серий повторяющихся эпилептиформных разрядов (4-10 Гц ритмические спайк-волны или 2-7 Гц ритмические острые волны), как правило, более ограниченных, чем размер поражения по данным нейровизуализации.
ФКД, выявляемая при МРТ, характеризуется очаговым утолщением коры головного мозга, затенением на границе серого и белого вещества, повышением сигнала на Т2-взвешенных и протонной плотности последовательностях (от поверхности коры до желудочка в случае фокальной трансмантийной дисплазии), иногда повышением после введения контрастного вещества. Примерно в одной трети случаев данные МРТ в норме.
Тотальное хирургическое иссечение очагов дисплазии является одним из наиболее важных прогностических факторов. Результат зависит от правильного предоперационного планирования на основе нейровизуализации и по интраоперационным находкам, выявляемым хирургом. Достижение контроля над припадками ожидается в 60-75% случаев. Такой уровень имеет тенденцию к снижению со временем, так что требуется длительное наблюдение.
1. Шизэнцефалия. Шизэнцефалия является заболеванием, характеризующимся односторонним или двусторонним расщеплением, обычно от мягкой мозговой оболочки лобной или теменной доли до бокового желудочка, с выстилкой дизламинированной и полимикроглиальной корой головного мозга. При варианте с «закрытыми (или сомкнутыми) краями» стенки расщепления накладываются друг на друга, а при форме с «открытыми краями» они разделены, соединяя полость желудочков и субарахноидальное пространство. Могут присутствовать другие аномалии, такие как гетеротопия серого вещества, склероз гиппокампа, мозолистого тела и/или агенезия прозрачной перегородки.
Эпилепсия поражает 35-85% пациентов с шизэнцефалией, как правило, начиная с первых двух десятилетий жизни и, обычно, проявляется более ранним началом и худшими результатами при двусторонних и/или открытых формах. Часто присутствуют задержка психического развития и двигательный дефицит. Хирургическое лечение малоэффективно.
2. Склероз гиппокампа (СГ). Атрофии гиппокампа (50-85%) и миндалевидного тела (30-60%), которые часто встречаются у детей с пороком развития коры (ПРК) височной доли, а также у лиц с вневисочными мальформациями (до 35%), но они могут возникнуть также изолированно (чистый СГ). Нет особых различий между чистым СГ и СГ с сопутствующим пороком развития коры (ПРК) относительно анамнеза, приступов и прогноза, а приступы исчезают после операции у 90% пациентов.
3. Гетеротопия серого вещества. Это неправильное положение массы серого вещества, локализованной перивентрикулярно или в подкорковом белом веществе, часто двустороннее, в результате нарушения процесса миграции. Картина эпилептических припадков разнообразна; лучший результат наблюдается при изолированных формах (как правило, при вовлечении области желудочкового треугольника).
б) Диффузная полушарная мальформация:
Гемимегалэнцефалия (ГМЭ). ГМЭ является прототипом врожденного полушарного порока развития коры (ПРК) с диспластической гипертрофией одного полушария, в то время как второе полушарие не поражается вообще или только в легкой степени. Действительно, последние гистологические, нейрофизиологические исследования и нейровизуализации предполагают постоянное, хотя незначительное вовлечение «здорового» полушария. Несмотря на многочисленные теории, этиопатогенез ГМЭ остается неизвестным. Ее можно рассматривать как сложную аномалию развития в результате нарушения нейронной пролиферации (первичное событие, с 3 по 4 неделю беременности), возможно последующее нарушение миграции (вторичное событие, между 12 и 20 неделями). Специфические гены не идентифицированы.
Гемимегалэнцефалия (ГМЭ) возникает с частотой 1-3/1000 у детей, страдающих эпилептическими припадками и составляет 1-14% всех пороков развития коры (ПРК) и 30-50% аномалий, требующих выполнения гемисферэктомии. Заболевание может проявляться как изолированная аномалия (спорадическая и наиболее распространенная) или может быть связано с частичным или полным гемигигантизмом тела и/или нейрокожным синдромом (например, синдром невуса Ядассона, синдром Протея, гипомеланоз Ито, синдром Клиппеля-Треноне-Вебера). При «тотальной ГМЭ» вовлекаются также гомолатеральные структуры задней черепной ямки.
Микроскопические особенности ГМЭ отчасти или полностью совпадают с описанными для других пороков развития коры (ПРК). Макроскопически определяются увеличенные полушария, гиперваскуляризация и широкий спектр аномалий развития коры (например, агирия, пахигирия, полимикрогирия, лиссэнцефалия). Такие изменения могут включать в себя все полушарие или его часть (как правило, задние отделы), в височной доле часто отмечается атрофия.
Асимметричная макрокрания, как правило, не проявляющаяся повышенным внутричерепным давлением, является типичным внешним проявлением.
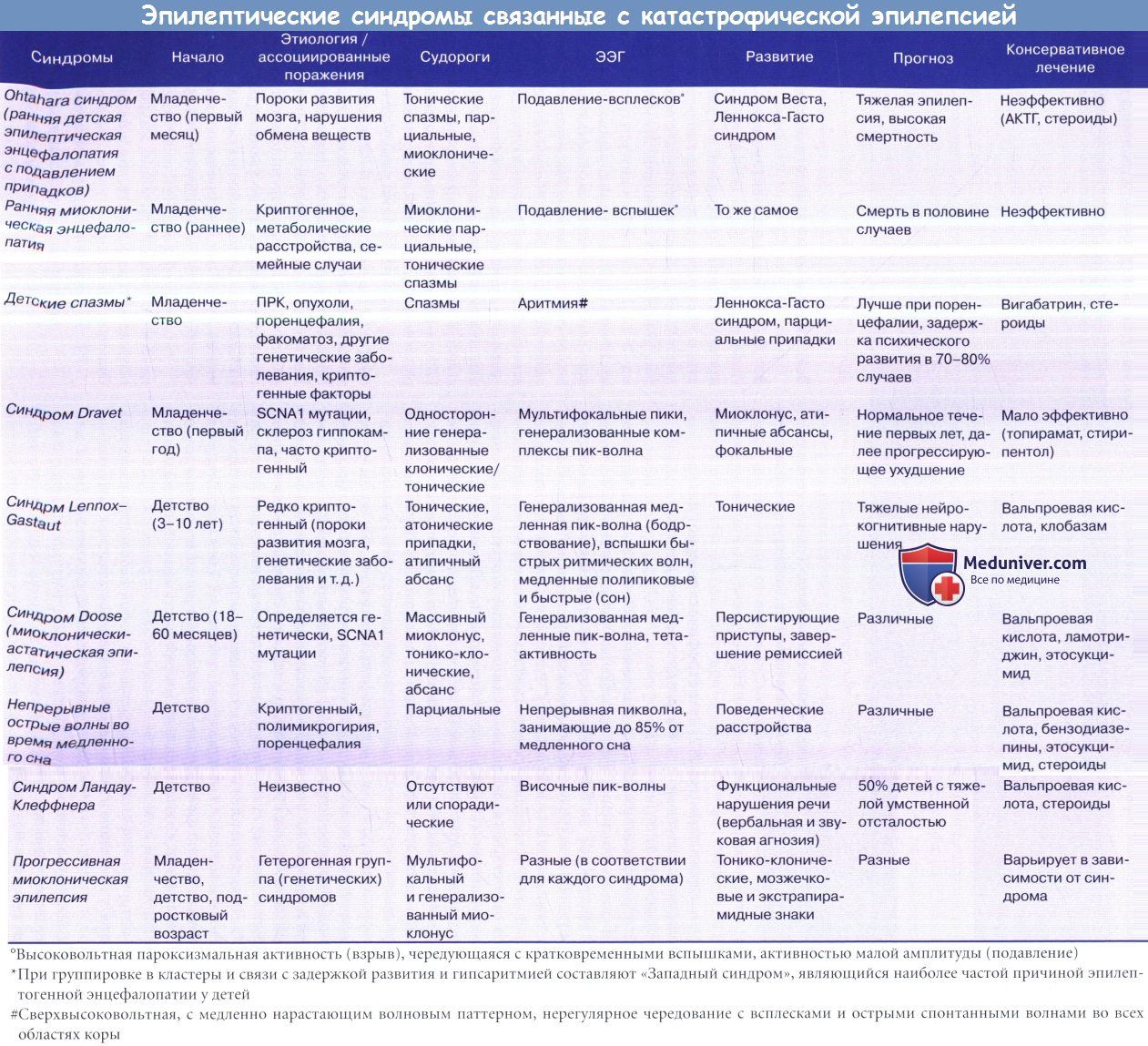
Гемимегалэнцефалия (ГМЭ) является наиболее тяжелой формой ПРК, а у большинства пациентов в течение нескольких недель или месяцев с момента рождения развивается КЭ. Типичная клиническая триада состоит из ФРЭ, контралатерального медленно прогрессирующего гемипареза и гемианопсии, с (тяжелой) задержкой психомоторного развития. Припадки возникают почти у 90% пациентов, могут наблюдаться большинство из синдромов, представленных в таблице ниже. Эпилепсия обычно начинается в раннем послеродовом периоде, как мягкие парциальные припадки и/или асимметричные спазмы и/или латерализованные миоклонические подергивания, часто превращаясь в синдром Ота-хара или синдром Веста. Впоследствии могут появляться синдром Леннокса-Гасто или тяжелые моторные парциальные припадки/кортикальная эпилепсия. Ранняя резистентность к противосудорожной терапии является практически правилом.
Ранняя межприступная ЭЭГ обычно показывает односторонний паттерн «вспышка-подавление», способный измениться или смениться гемигипсаритмией. Поздний ЭЭГ-паттерн состоит из еще более дезорганизованой и непрерывной активности над пораженным полушарием, возможно распространение на противоположную сторону. Указанные макроскопические диспластические состояния, такие как увеличение полушария, аномалии развития извилин, дисплазия коры, плохая дифференцировка серого/белого вещества и гетеротопии, могут быть выявлены при МРТ.
Гомолатеральная желудочковая система, как правило, расширена, с прямым фронтальным рогом и расширенным затылочным, но она также может быть нормальной или уменьшенной. На поздних стадиях болезни пораженное полушарие может атрофироваться.
Даже сопряженная с высокой смертностью и инвалидизацией гемисферэктомия является выбором при лечении ГМЭ. На самом деле, практически у 80-90% пациентов, подвергнутых гемисферэктомии, отмечается длительный период без судорог, с таким же уровнем показателей, как при менее тяжелой форме ФРЭ, требующей гемисферэктомии. Тем не менее, двигательные и когнитивные результаты могут оставаться плохими у значительной доли оперированных пациентов.
Мультилобарная кортикальная дисплазия включает полушарную ПРК, которая не может быть классифицирована как ГМЭ из-за менее распространенных диспластических областей и довольно больших неизмененных регионов. Заднеквадрантная дисплазия, в соответствии с определением, данным D’Agostino et al., является своеобразным ПРК, вовлекающим височную, затылочную и теменную доли (постцентральная извилина исключена). Этиопатогенетическая гипотеза будет такой же, как при ГМЭ, с частичным вовлечением полушария чем можно объяснить мозаичность. Гистологические, клинические характеристики и нейровизуализации похожи на ГМЭ, за исключением вовлечения структур передних отделов полушария и более легкого клинического течения. Можно выполнять мультилобарные резекции вместо гемисферэктомии, получая такие же хорошие результаты с небольшим хирургическим риском, если только нет предоперационного моторного дефицита и/или ЭЭГ аномалии не являются гологемисферическими.



Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое фкд 2 типа
Хотя отдельные фокальные дисплазии включают участки полимикрогирии (ПМГ), большинство из них обычно не являются полимикрогирии с гистологической точки зрения, поэтому предпочтительнее неоднозначное определение фокальная корковая дисплазия, включающее аномалии как миграции, так и организации, а в отдельных случаях нарушения пролиферации и дифференцировки нейробластов. Значительное число сообщений в литературе об эпилепсии появилось за последние 20 лет (см. Janota и Polkey, 1992, Guerrini и Filippi, 2005). Очаговые дисплазии могут быть обнаружены в любой области коры. Нередко встречается оперкулярная дисплазия (Ambrosetto, 1992, Sebire et al., 1996).
Действительно, многие случаи локализованной кортикальной дисплазии избирательно поражают эту область. В области корковой дисплазии кора уплотнена, а извилины увеличены. Гистологическая картина варьирует от простой дезорганизации пластинок или колонок с субкортикальными гетеротопическими нейронами до более сложных аномалий с гигантскими нейронами и клетками, подвергшимися баллонной дистрофии, а также гигантскими многоядерными астроцитами (Taylor et al; 1971, Tassi et al., 2002; Alonso-Nanclares et al., 2005).
Классификация этих мальформаций с патологической точки зрения остатеся предметом дискуссий (Palmini et al., 2004). Выделено по меньшей мере два типа, известные как тейлоровская и не-тейлоровская кортикальная дисплазия. В недавней классификации (Tassi et al., 2002) выделено три типа: архитектоническая дисплазия, при которой нарушается корковая структура, но гигантские нейроны или аномальные клетки отсутствуют; цитоархитектоническая дисплазия, где в дополнение к патологически организованной коре имеются гигантские и/или дисморфические нейроны; и тейлоровский тип дисплазии, при котором также присутствуют «баллонные клетки», напоминающие повреждения при туберозном склерозе.
Эти клетки окрашиваются как нейрональными, так и глиальными маркерами и являются следствием раннего нарушения клеточной дифференцировки. Кортикальные дисплазии могут поражать любую часть коры и рассматриваются в качестве основной причины очаговой эпилепсии, часто трудно поддающейся лечению. Тейлоровский тип обычно преобладает в лобных и теменных долях, тогда как другие типы чаще встречаются в височных долях (Kuzniecky et al., 1994). Основным клиническим проявлением являются очаговые судороги (Hamiwka et al; 2005, Fauser et al., 2006) часто, но не всегда устойчивые к медикаментозному лечению (см. главу 15). У четырех детей сообщалось о небольших участках корковой дисплазии, которые могли отвечать за очаговый корковый миоклонус и фокальные двигательные судороги (Kuzniecky et al., 1986). Подобные повреждения были обнаружены в случае с эпилептическим статусом (Desbiens et al., 1993).

Большие нейроны неправильно расположены в пределах коры.
Отдельные нейроны с характерной периферической конденсацией хроматина.
В недавних исследованиях микроанатомии, молекулярного патогенеза и патофизиологии этих повреждений описана подробная структура с демонстрацией присущего им эпилептогенного потенциала (Bentivoglio et al., 2003; Alonso-Nanclares et al., 2005; Crino, 2005).
Визуализация данной патологии основывается на MPT исследовании, но выявление может оказаться непростым и потребовать новейших методов МР. Тем не менее, значительная часть случаев может остаться нераспознанной. Тейлоровский тип дисплазии может иметь отличительные МР признаки в виде особенно высокого сигнала в белом веществе под повреждением, иногда распространяющегося до желудочка (так называемая трансмантийная корковая дисплазия) (Barkovich et al., 1997). Архитектонические и цитоархитектонические дисплазии чаще проявляются истонченной корой на MPT (Tassi et al., 2002).
Фокальная кортикальная дисплазия может сопровождаться опухолями дисэмбриогенеза (ганглиоглиомами и нейроэпителиальными опухолями) в этой же области мозга.
Хирургическое лечение эпилепсии в результате очаговой дисплазии возможно в значительной доле случаев и способно купировать судороги (Tassi et al., 2002; Cascino et al., 2004; Fauser et al., 2004, 2006; Hamiwka et al., 2005).
Большинство случаев кортикальной дисплазии относятся к спорадическим, но встречаются и семейные случаи (Kuzniecky et al., 1994).
Некоторые редкие синдромы проявляются напоминающей пахигирию корой в сочетании с внемозговыми аномалиями: врожденный нефроз у мужских сиблингов (Robain и Deonna, 1983; Palm et al., 1986), семейная лимфэдема и агенезия червя мозжечка (Hourihane et al., 1993), врожденная короткая кишка (Nezelof et al., 1976), и семейная пахигирия с диссеминированной кальцификацией мозга и атаксией (Harbord et al., 1990).
Основной интерес при очаговой корковой дисплазии заключается в перспективах хирургического лечения. Этот вопрос будет обсуждаться в отдельной статье на сайте.
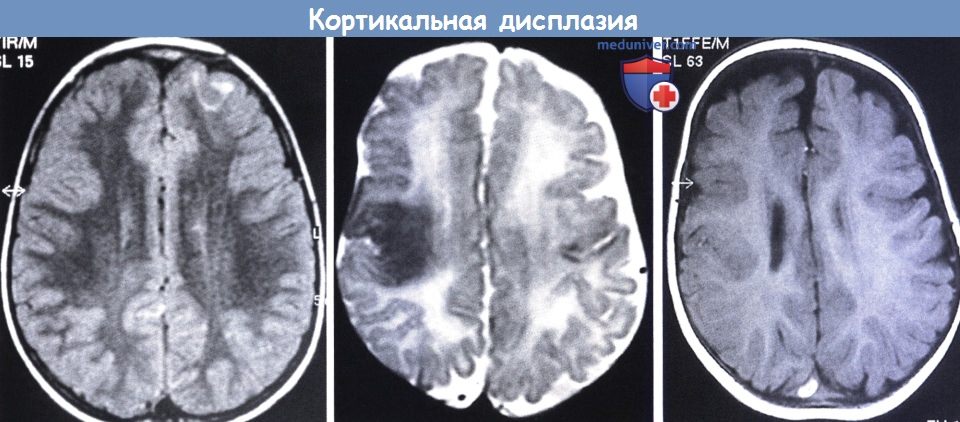
Т2-взвешенная МРТ: определяются области патологической коры в правой лобной доле с высоким сигналом в подлежащей аномальной коре.
После резекции патологического участка был достигнут контроль над судорогами, (в центре) МРТ:
(другой мальчик с судорогами) заметны диспластические участки в возрасте шести месяцев, которые в 18 месяцев стали более очевидными (справа).
— Вернуться в оглавление раздела «Неврология.»
Редактор: Искандер Милевски. Дата публикации: 29.11.2018