что лучше простатилен или простанорм
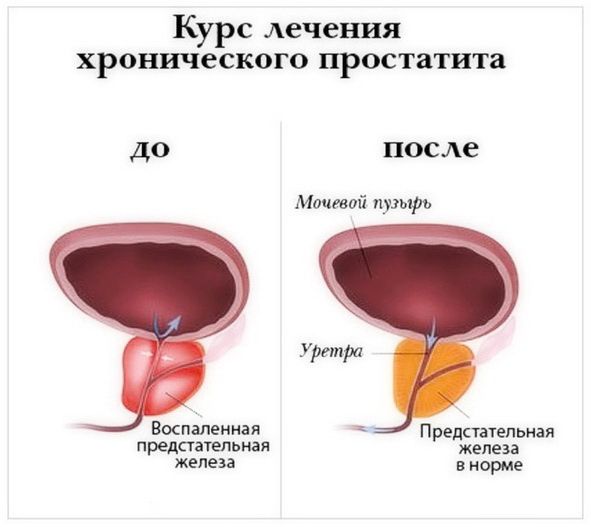
Эффективные лекарства от простатита у мужчин
Простатит неодинаково протекает у разных мужчин. Какие-то симптомы бывают более выраженными, какие-то отсутствуют. Большое значение имеет стадия болезни, наличие гиперплазии предстательной железы или аденомы. Врачи учитывают, впервые развилось воспаление или уже имеется стаж.
Подобрать лечение простатита у мужчин, найти самые эффективные средства для каждой стадии простатита может только врач-уролог, после обследования и получения результатов анализов.
Тем не менее ориентироваться в средствах для лечения простатита должен каждый, кто столкнулся с этой проблемой.
Виды лекарств от простатита у мужчин
Урологи применяют несколько групп препаратов.
Антибиотики борются с инфекцией в мочевом тракте, все прочие средства снижают воспаление, уменьшают отёк и боль, облегчают отхождение мочи, улучшают кровоснабжение половых и мочевыводящих органов.
Существует масса гомеопатических средств от простатита и потенции, производные интерферона, которые в статье не рассматриваются. Их польза не доказана в исследованиях.
Каким должно быть лучшее средство от простатита у мужчин
Лечение, назначенное врачом, должно достигать следующих целей:
Единственного препарата, который в полной мере отвечает всему перечисленному, нет. Поэтому урологи прописывают приём 2–3 препаратов, подобранных индивидуально в каждом случае. Лекарства сочетают с массажем, физкультурой, физиопроцедурами.
Для лечения простатита у мужчин самыми эффективными средствами считаются ректальные свечи, поскольку поставляют лекарство к железе, минуя печень и создают в тканях высокую лечебную концентрацию.
Топ-5 эффективных средств для лечения простатита
Эти препараты обладают комплексным действием, проверены в клинической практике.
Витапрост
Свечи и ампульный препарат экстракта простаты. Эффективен при остром и хроническом воспалении, поскольку в состав лекарства входит антибиотик.
Лонгидаза
Бактерицидным действием не обладает, назначается вместе с антибиотиком. Подходит в хронических случаях, когда уже появился воспалительный фиброз в органе, спайки, разрастание ткани простаты. Результативна при болезни Пейрони.
Простатилен
Инъекции и ректальные свечи. В сочетании с антибактериальным средством снимает воспаление, нормализует мочеиспускание, улучшает эрекцию.
Простамол Уно
Растительный препарат. Выпускается в капсулах. Уменьшает боли, восстанавливает ток мочевой струи, нормализует потенцию.
Простанорм
Лекарство из растительного сырья. Применяется больше для профилактики, продления ремиссии при хроническом процессе. Имеет небольшой антибактериальный эффект, убирает боль, стимулирует иммунитет, улучшает кровоснабжение железы и отток мочи.
При снижении тонуса мочевыводящей системы врачом по рецепту назначается Омник. В осложнённых случаях при аденоме простаты может потребоваться применение финастерида для регуляции баланса тестостерона.
Хорошо себя зарекомендовали как лекарства от простатита недорогие Ихтиоловые свечи, ампульный Простакор.
Недопустимо самостоятельное применение медикаментов без учёта бактериальной флоры и стадии болезни. Терапия острого простатита под присмотром врача убережёт от осложнений и перехода в хроническую форму.
Для назначения лечения обращайтесь к урологу клиники Dr. AkNer по телефону или через форму обратной связи. Звоните, опытный специалист выберет вам препараты и проконтролирует лечение до выздоровления.
Клинико-лабораторная эффективность монотерапии «Простатиленом®» (ректальные суппозитории) доброкачественной гиперплазии предстательной железы (ДГПЖ) с синдромом нижних мочевыводящих путей (СНМП)
И.В. Сорока, С.В. Петленко*
Научно-исследовательский институт скорой помощи им. И.И.Джанелидзе;
*Военно-медицинская академия им. С.М.Кирова
Скачать PDF
У больных доброкачественной гиперплазией предстательной железы с синдромом нижних мочевыводящих путей проведен курс терапии пептидным биорегулирующим препаратом «Простатилен®». Сравнительный анализ полученных данных свидетельствует, что по клинико-лабораторной эффективности монотерапия «Простатиленом ® » ДгПЖ практически не уступает комбинированному применению средств из группы двойных ингибиторов 5а-редуктазы и альфа-адреноблокаторов, которые в настоящее время считаются наиболее эффективными средствами лечения данных форм урологической патологии.
Эпидемиология доброкачественной гиперплазии предстательной железы, характеризуется развитием данной патологии в основном у лиц пожилого и старческого возраста. гистологически ДгПЖ представляет собой вялотекущий пролиферативно-воспалительный и склерозирующий процесс, который в сочетании с ассоциированной патологией других органов мочевыделения (старческая атония мочевого пузыря, стриктура уретры, недержание мочи в следствие слабости сфинктерного аппарата) приводит к выраженным расстройствам мочеиспускания, которые получили общее название «синдром нижних мочевыводящих путей» (СНМП). СНМП как самостоятельная нозологическая форма подразделяется на легкую, умеренную и тяжелую степень в зависимости от глубины нарушения уродинамических показателей.
Материалы и методы
Обследовано 24 пациента в возрасте от 50 до 85 лет с диагнозом доброкачественная гиперплазия предстательной железы, синдром нижних мочевыводящих путей. Критерием исключения из исследования было наличие хронических заболеваний требующих постоянного приема лекарственных средств, которые могут оказать влияние на течение урологической патологии (сахарный диабет, системные заболевания и т.д.). Кроме того критерием исключения служило повышение содержания простатаспецифического антигена (ПСА) в сыворотке более 4 нг/мл.
Прием препарата «Простатилен ® » осуществлялся по схеме, аналогичной той, которая была использована при лечении хронического простатита (по 1 свече на ночь в течение 10 суток). Всем обследованным в динамике двухкратно (до и через 3 недели после окончания лечения) выполнено углубленное клинико-лабораторное обследование, включающее оценку основных параметров, отраженных в «Рекомендациях совещания совета экспертов по лечению аденомы предстательной железы» [2008]. Полученные данные сравнивали с результатами первичного исследования пациентов, а так же материалами 2-х летнего ктамнестического наблюдения «CombAT» по комбинированному применению препаратов «Аводарт» и «Тамсулозин», которые в настоящее время считаются наиболее эффективными в терапии ДгПЖ.
Основные результаты исследования и их обсуждение
Таблица 1. Динамика клинических проявлений дизурии у пациентов с ДГПЖ на фоне лечения
* – достоверные изменения показателя по сравнению с результатами первичного обследования (р>0,05)
** – по данным CombAT исследования (2009г)
Полученные данные свидетельствуют, что после однократного курсового применения «Простатилен®» по эффективности устранения дизурических явлений, таких как снижение частоты мочеиспускания и повышение минимального объема мочеиспускания не уступает препаратам из группы двойных селективных ингибиторов 5а-редуктазы, а по снижению уровня остаточной мочи, даже несколько превосходит их. Комплексная терапия с применением «Аводарта» и «Тамсулозина» способствовала уменьшению объема остаточной мочи на 67%. При монотерапии «Простатиленом ® » в группе обследованных данный показатель в течение трех недель наблюдения снижался на 123%. По-видимому, основным механизмом действия всех исследованных препаратов, способствующих улучшению уроки- нетических параметров, в данном случае является повышение тонуса и стимуляция гладкой мускулатуры мочевого пузыря. Это предположение основано на анализе динамики клинических проявлений основного урологического заболевания, которая свидетельствует, что сокращение объема предстательной железы (Упж), вследствие ее склеротических изменений, у пациентов доброкачественной гиперплазией выражено в значительно меньшей степени, чем при простатите (табл.2).
Таблица 2. Изменение суммарного индекса IPSS и объема предстательной железы (V пж) у пациентов с ДГПЖ на фоне различных вариантов монотерапии
* – достоверные изменения показателя по сравнению с результатами первичного обследования (р>0,05)
** – по данным CombAT исследования (2009г)
Клинически значимое (статистически достоверное) изменение объема предстательной железы отмечалось только при использовании в качестве монотерапии препарата «Простатилен ® ». В группе сравнения (CombAT), несмотря на отсутствие статистически достоверных данных по уменьшению объема ПЖ, при ТРУЗИ-исследовании в 95% случаев отмечалось снижение плотности железы, а так же уменьшение количества и объема узлов склерозирования.
Качественная оценка уродинамики пациентов с ДГПЖ выявила позитивное влияние препарата «Простатилен®» (ректальные суппозитории) на характеристики мочесиспускания (рис.1).
Рис.1. Сравнительное влияние различных вариантов терапии на качественные характеристики уродинамики пациентов с ДГПЖ
До начала лечения у пациентов с ДГПЖ и СНМП был характерен резко выраженный прерывистый характер мочеиспускания, с низкими значениями максимальной и средней скорости мочевой струи и невысоким дебетом экскретируемой жидкости. Через три недели после курса терапии во всех группах отмечено клинически значимое улучшение уродинамики. наиболее выраженные позитивные изменения были получены в группе обследованных получивших курс «Простатилена®». У этой категории пациентов, отмечено восстановление непрерывности мочевой струи, что является показателем регресса патологических изменений предстательной железы и, что особенно важно, повышения сократительной способности m. detrusor urinae. «Аводарт» в комбинации с «Тамсулозином» так же способствовали улучшению характеристик мочеиспускания (снижение дискретности, усиление напряженности струи, повышение количества выделенной мочи), хотя они были менее выражены, чем на фоне монотерапии «Простатиленом ® ».
Рис.2. Динамика содержания сывороточного PSA у пациентов с ДГПЖ на фоне монотерапии «Простатиленом ® »
Анализ динамики количественных параметров мочеиспускания показал высокую лечебную эффективность использованных препаратов в отношении синдрома нижних мочевыводящих путей у пациентов с ДЕПЖ (табл. 3).
Таблица 3. Влияние различных вариантов терапии на количественные параметры уродинамики пациентов с ДГПЖ
* – достоверные изменения показателя по сравнению с результатами первичного обследования (р>0,05)
** – по данным CombAT исследования (2009г)
Наиболее выраженная положительная динамика объективных показателей уродинамики отмечена в группе пациентов, получивших свечи «Про- статилен». Математическая обработка данных показала. что у данной категории обследованных, наблюдается статистически достоверное улучшение всех основных показателей урофлоуграмм, характеризующих процесс мочеиспускания. Максимальная скорость (Qmax) мочеиспускания, характеризующая наибольшую сократительную способность m. detrusor urinae, после однократного курса препарата увеличипась в 2,84 раза. Величина средней скорости мочеиспускания (характеризует способность к продолжительному сокращению гладкой мускулатуры мочевого пузыря) возрастала в 1,7 раза. Одновременно с улучшением динамики мочевыведения отмечалось значительное повышение объема однократно выделяемой мочи, прирост которого у пациентов с ДГПЖ составил более 60% от первоначального значения. Кроме того, в процессе монотерапии у пациентов с Д1ПЖ препарат способствовал снижению уровня общего PSA на 32% (с 3,7 до 2,8 нг/мл), что свидетельствует о снижении риска развития злокачественного процесса предстательной железы у лиц пожилого возраста (рис.2).
Клиническую эффективность монотерапии ректальных суппозиториев «Простатилен®» в отношении купирования синдрома нижних мочевыводящих путей в целом можно считать сопоставимой с комбинированным применением препаратов из группы двойных ингибиторов 5а-редуктазы. Сравнительный анализ схем терапии ДГПЖ с СНМП показал, что пептидные препараты («Простатилен®») и селективные ингибиторы 5а-редуктазы примерно с одинаковой эффективностью статистически достоверно и клинически значимо повышали пиковые значения скорости мочевыведения (в 1,7 и 1,6 раза соответственно), существенно не влияя на средние показатели объемной скорости мочеиспускания. О позитивном влиянии препаратов на гладкую мускулатуру мочевого пузыря так же свидетельствует значительное увеличение объема однократно выводимой мочи.
Заключение
Интегральная оценка лечебного воздействия препарата «Простатилен®» (ректальные свечи), использованного в качестве монотерапии пролиферативно-склерозирующих (ДгПЖ) заболеваний предстательной железы с сопутствующими дизурическими нарушениями (СНМП), показала его высокую клинико – лабораторную эффективность в отношении данных нозологических форм заболеваний.
Полученные результаты свидетельствуют о том, что по эффективности нормализации показателей уродинамики и профилактики злокачественных новообразований ПЖ (снижение уровня PSA), препарат «Простатилен®» полностью сопоставим с комбинированным применением лекарственных средств из группы двойных ингибиторов 5а-редуктазы («Аводарт», «Дуастерид») и альфа-адреноблокаторов («Тамсулозин»), которые в настоящее время считаются наиболее эффективными средствами терапии доброкачественной гиперплазии предстательной железы (ДгПЖ) и синдрома нижних мочевыводящих путей (СНМП).
Современные возможности медикаментозного лечения доброкачественной гиперплазии ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2].
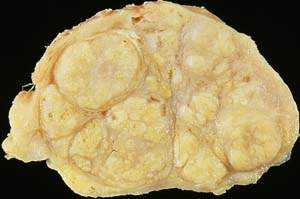 |
| Рисунок 1. Доброкачественная гиперплазия предстательной железы (макропрепарат) |
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2]. Около 80% мужчин старше 80 лет страдают этим заболеванием. Другая статистика свидетельствует, что из всех заболеваний, которым подвержены мужчины старше 50 лет, на долю доброкачественной гиперплазии простаты приходится 36% [1]. Эти сведения настолько общеизвестны, что ухудшение качества мочеиспускания часто рассматривается как естественное явление.
Клинически данное заболевание проявляется различными симптомами, связанными с нарушением пассажа мочи по нижним мочевым путям. При значительно выраженной инфравезикальной обструкции, как правило, прибегают к хирургическому вмешательству. Оперативное лечение по поводу ДГПЖ показано 30% больных в возрасте от 50 до 80 лет [4]. Однако в последние годы все большую популярность завоевывает медикаментозная терапия доброкачественной гиперплазии предстательной железы. Это, с одной стороны, объясняется вполне логичным желанием врача и пациента по возможности избежать операции, с другой — развитием представлений о патогенезе расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы.
До недавнего времени патогенез расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы рассматривали с позиции классических представлений о механической инфравезикальной обструкции и развитии вторичных структурно-функциональных изменений детрузора (компенсация, декомпенсация). За последние два десятилетия получены принципиально новые данные о природе повышенного внутриуретрального сопротивления. Его перестали отождествлять исключительно с механическим сдавлением шейки мочевого пузыря и задней уретры. Обнаружен динамический компонент обструкции, который состоит в повышении тонуса указанных анатомических структур за счет активности a-адренорецепторов. Появились также иные трактовки происхождения ирритативных симптомов. Их считают проявлением первичного нестабильного мочевого пузыря и не связывают напрямую с обструкцией [5].
Результаты нашей работы свидетельствуют, что при ДГПЖ клиническая симптоматика развивается вследствие недостаточности энергетического метаболизма и гипоксии детрузора в условиях повышенного уретрального сопротивления [3]. Об этом свидетельствуют:
Причины нарушений энергетического метаболизма и функций детрузора крайне многообразны. В частности, к таким нарушениям могут привести повышение активности симпатической нервной системы, расстройства органного кровообращения, авитаминоз (группа В), хронические заболевания дыхательной и сердечно-сосудистой систем, влияние приема ряда фармакологических препаратов, угнетающих дыхательную цепь, и, естественно, обструктивные нарушения уродинамики и т. д. Весьма важно, что нарушения гипоксического характера в гладкомышечной ткани могут иметь и первичный митохондриальный генез (первичные нарушения энергетического метаболизма детрузора [3].
Необходимо отметить, что у больных ДГПЖ в нижнем отделе мочевого тракта протекают два параллельных процесса — формирование уретральной обструкции и нарушение энергетического метаболизма детрузора (митохондриальная недостаточность).
Подобное представление патогенеза расстройств мочеиспускания открывает широкие возможности для фармакотерапии. Сокращения и расслабления детрузора можно достичь с помощью средств метаболической терапии, прямого улучшения снабжения детрузора кислородом и т. д. Наиболее значимые расстройства основных функций мочевого пузыря все же опосредованы расстройствами кровообращения. И если процесс обратим, то до или после хирургического вмешательства можно существенно влиять на функциональное состояние мочевого пузыря с помощью вазоактивных препаратов, к которым в первую очередь относятся a1-адреноблокаторы.
При определении критериев отбора пациентов для медикаментозной терапии ДГПЖ мы воспользовались рекомендациями IV Международного консультативного комитета по ДГПЖ.
Основу настоящего исследования составили собственные клинические наблюдения за 1724 пациентами (средний возраст 61,4 года), страдающими ДГПЖ и получавшими различные варианты медикаментозного лечения. Нами применялись препараты всех групп, использующихся в настоящее время для лечения ДГПЖ: a-адреноблокаторы, блокаторы 5-a-редуктазы, препараты растительного происхождения и их комбинации. Схемы проведенного лечения и характеристика групп пациентов приведены в табл. 1.
Из наиболее многочисленной и популярной сегодня группы препаратов для медикаментозного лечения ДГПЖ — селективных a-адреноблокаторов мы использовали альфузозин, теразозин, доксазозин и тамсулозин. Общее число пациентов, получавших a-адреноблокаторы, составило 1408. Финастерид был взят нами как классический представитель блокаторов 5-a-редуктазы. Из препаратов растительного происхождения мы использовали пермиксон и таденан.
В пяти группах общей численностью 1305 человек проводилась терапия селективными a-адреноблокаторами в течение длительного периода времени по стандартным схемам и в стандартных дозах. Результаты лечения приведены в табл. 2.
Улучшение качества мочеиспускания отметили в среднем 86,74% пациентов. Суммарный балл I-PSS сократился на 38,68% к окончанию первого года лечения и на 43,4% к окончанию курса терапии. Балл QOL уменьшился на 29,04% и 35,58% соответственно. Максимальная скорость потока мочи увеличилась на 45,25% к окончанию первого года лечения и стабилизировалась на достигнутом уровне. Количество остаточной мочи сократилось в среднем на 57,6%. Процент пациентов, по тем или иным причинам выбывших из исследования, был тождествен во всех группах и равнялся 14,38%.
Особо следует остановиться на препарате тамсулозин (омник, Yamanouchi) — пока единственном простатселективном a1А-адреноблокаторе на отечественном рынке. Этот препарат обладает рядом свойств, которые позволяют его использовать в различных функциональных тестах. Прежде всего это возможность назначения единой терапевтической дозы (один раз в сутки по 0,4 мг). А отсутствие выраженного влияния на артериальное давление и сердечную деятельность избавляет от необходимости титрования дозы. Мы согласны с рядом авторов, которые считают возможным применение коротких курсов терапии тамсулозином в качестве прогностических тестов эффективности лечения a1-адреноблокаторами, что может иметь решающее значение при выборе того или иного метода медикаментозного лечения ДГПЖ [4].
Части больных (группа А5) проведена проверка возможности разрешения острой задержки мочеиспускания (ОЗМ) приемом альфузозина по 5 мг два раза в сутки. Эта терапия проводилась пациентам с впервые возникшей ОЗМ и отсутствием симптомов нарушения мочеиспускания в анамнезе. Положительный эффект был достигнут у 8 из 14 пациентов (57,1%), которым параллельно приему альфузозина производилось кратковременное (трое суток) дренирование мочевого пузыря катетером. Единовременный прием суточной дозы альфузозина (10 мг) способствовал восстановлению самостоятельного мочеиспускания лишь у одного из четырех пациентов, которым проводилась подобная терапия. Вероятно, это объясняется гипотонией детрузора, усугубляющейся в ситуации длительного перерастяжения мочевого пузыря на фоне задержки мочеиспускания.
Для изучения эффективности и безопасности комбинированной медикаментозной терапии ДГПЖ препаратами разных групп, а также для уточнения целесообразности проведения терапии нами были созданы три группы.
В первой группе (К1) пациенты получали проскар по 5 мг/сут. параллельно с приемом теразозина по 5-10 мг/сут. Обращало на себя внимание значительное повышение показателей максимальной скорости потока мочи (+40%), характерное для группы монотерапии a-адреноблокаторами, и постепенное, на протяжении курса лечения, снижение объема предстательной железы (-20,4%), характерное для группы монотерапии финастеридом. Очевидно, что положительные изменения показателей мочеиспускания в этой группе являются следствием воздействия обоих препаратов. Тем не менее процент выбывших пациентов в этой группе был крайне высоким — 32,3%. Основной причиной прекращения комбинированной терапии ДГПЖ пациенты называли неприемлемо высокую стоимость лечения.
В третьей группе комбинированной терапии (К3) лечение проводилось финастеридом по 5 мг/сут. в сочетании с пермиксоном по 160 мг два раза в сутки. Через два года после начала лечения 50% пациентов покинули группу, приводя причиной отказа от дальнейшей терапии высокую стоимость лечения при отсутствии быстрого улучшения качества мочеиспускания. При сравнении полученных данных с результатами в других группах очевидно, что эффективность лечения в третьей существенно ниже.
Таким образом, эффективность медикаментозной терапии больных ДГПЖ при соблюдении показаний и противопоказаний к ее назначению, правильном выборе препарата и схемы его назначения высока и достигает в среднем 80,2%. При этом эффективность монотерапии a-адреноблокаторами составляет 86,7%, блокаторами 5a-редуктазы — 69,4%, препаратами растительного происхождения — 69,3% и при комбинированной терапии — 95,45%. Комбинированная медикаментозная терапия a-адреноблокаторами в сочетании с блокаторами 5a-редуктазы эффективнее монотерапии этими препаратами. С целью снижения стоимости лечения возможен переход на монотерапию блокаторами 5a-редуктазы после достижения выраженного регресса обструктивной симптоматики. Медикаментозная терапия a-адреноблокаторами является эффективным способом консервативного лечения острой задержки мочеиспускания. Терапия должна проводиться на фоне кратковременного (трое суток) дренирования мочевого пузыря уретральным катетером.
Литература
1. Гориловский Л. М. Эпидемиология и факторы риска развития доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 10-18.
2. Лопаткин Н. А., Перепанова Т. С. Клинический опыт лечения больных доброкачественной гиперплазией предстательной железы a1-адреноблокатором альфузозином // Урол. и нефрол., 1997, № 5, с. 14-17.
3. Лоран О. Б., Вишневский Е. Л., Вишневский А. Е. Лечение расстройств мочеиспускания у больных доброкачественной гиперплазией простаты a-адреноблокаторами. Монография. М., 1998.
4. Сивков А. В. Медикаментозная терапия доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 67-83.
5. McConnell J. D. Prostatic growth: new insights into hormonal regulation // Br. J. Urol. 1995. Vol.76.(suppl.1). P. 5-10.